技术干货 | In Vivo CAR药物:病毒载体技术的创新与挑战
2025-12-02 15:48:37 江苏谱新生物医药有限公司
概念与发展历程
In Vivo CAR
In Vivo CAR药物是一种颠覆传统细胞治疗模式的创新技术。与传统CAR-T疗法(需体外提取并改造患者T细胞)不同,其核心在于通过递送系统(如病毒载体或纳米颗粒)将CAR基因直接注入患者体内,在体内完成T细胞的基因编辑,使其表达嵌合抗原受体(CAR),从而靶向杀伤肿瘤细胞。
发展历程
早期探索:2021年,美国公司Umoja Biopharma通过慢病毒载体实现体内T细胞工程化,临床前数据显示其CAR-T细胞可抑制肿瘤生长。 技术突破:2022年,宾夕法尼亚大学团队利用mRNA-LNP(脂质纳米颗粒)技术,在动物模型中成功治疗心脏损伤,验证了mRNA在体内瞬时表达CAR的可行性。 国内进展:2023年,北京百替生物(BTBT)开发出“LINCMECAR”技术,通过纳米载体递送CAR基因药物,成为国内首个进入临床前研究的体内CAR疗法平台。
这一技术的优势显著:
治疗周期短:无需体外培养细胞,从数周缩短至几天; 成本低:生产工艺简化,预计成本仅为传统疗法的1/50-1/100; 适用性广:有望突破实体瘤治疗瓶颈,并减少免疫排斥风险。
生产工艺流程如下:
(1)载体设计与构建:选择靶向T细胞的病毒衣壳蛋白(如CD8特异性融合素),设计包含CAR基因和调控元件的慢病毒载体基因组。
(2)病毒包装:采用瞬时转染技术,将载体质粒、包装质粒和包膜质粒共转染至HEK-293T细胞中,利用PEIpro®或FectoVIR®-LV等转染试剂提高病毒滴度。
对于使用慢病毒载体生产的In Vivo CAR产品,滴度作为关键质量属性(CQA),一直困扰着研发人员对产品质量判断和产品工艺条件的优化。
对于滴度检测,以下是常用的检测方法:
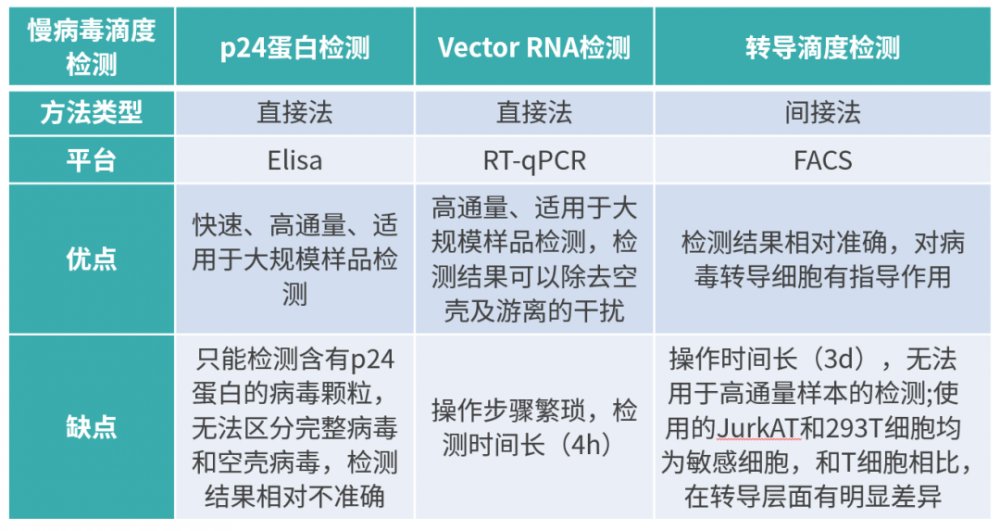
对于研究人员来说,使用RT-qPCR方法进行慢病毒的滴度检测,能更有效的帮助研究人员进行In Vivo CAR工艺条件优化。
为了帮助研究人员更好的进行In Vivo CAR滴度检测,谱新生物旗下品牌BlueKit®开发了Lentiviral Vector RNA Copy Number Detection Kit(货号:HG-VR001)用于慢病毒滴度检测,产品靶标设计位于LTR保守区,适用于目前全部的慢病毒载体骨架,在实验过程中设计了2次的DNA酶消化,有效避免了质粒DNA残留对检测结果的干扰。具体产品信息可点击下方阅读原文。
Umoja Biopharma(美国):采用慢病毒载体平台VivoVec,通过靶向CD8的包膜蛋白实现T细胞特异性转导,并结合RACR系统增强CAR-T细胞体内扩增能力。其临床前数据显示,单次给药即可在体内生成功能性CAR-T细胞。 Sana Biotechnology(美国):开发融合素(Fusogen)技术,利用靶向T细胞膜蛋白的融合素载体,直接将CAR基因递送至T细胞,避免病毒载体潜在的基因组整合风险。 Ixata(英国):结合慢病毒与LNP技术,通过纳米颗粒封装慢病毒载体,提高体内递送效率并降低免疫原性。
北京百替生物(BTBT):开发“LINCMECAR”平台,采用聚合物纳米颗粒包裹CAR基因,初步实现靶向肝癌的体内T细胞工程化,成本仅为传统疗法的1%。目前处于临床前研究阶段。 艾博生物:依托mRNA-LNP技术积累,探索瞬时表达CAR的体内疗法,但其病毒载体生产仍依赖进口慢病毒原料。 复星凯特与药明巨诺:虽以传统CAR-T为主,但通过引进海外技术(如复星凯特与Kite Pharma合作)逐步布局病毒载体本土化生产,计划2026年实现慢病毒载体国产化。
技术挑战
靶向性与安全性平衡:病毒载体易被肝脏捕获,导致脱靶效应和肝毒性。需通过衣壳工程化或靶向配体修饰提高特异性。
持久性与剂量优化:慢病毒介导的CAR表达为长期性,可能引发插入突变风险;而mRNA-LNP虽安全性高,但需频繁给药。
产业化前景
政策支持与成本降低:2025年起,中国对CAR-T用病毒载体实施零关税政策,推动进口原料成本下降50%-70%,加速本土工艺研发。
技术融合创新:CRISPR基因编辑技术与病毒载体的结合(如定点整合CAR基因)或成为下一代方向,可提高安全性和表达稳定性。
了解更多产品信息,可点击下方阅读原文。


相关产品信息与购买信息
电话咨询:400-900-1882 邮箱咨询:info@hillgene.com 表单咨询:扫描如下二维码


相关阅读
【相关产品】Lentiviral Vector RNA Copy Number Detection Kit
 你已选中了添加链接的内容
你已选中了添加链接的内容关于谱新

04-20 环亚生物
InnoQuant激光共聚焦全景玻片扫描在非小细胞肺癌肿瘤微环境研究中的应用04-20 环亚生物
拍出最真实最清晰的图片—InnoQuant助力生物组织荧光切片扫描和分析04-20 环亚生物
全景激光共聚焦扫描技术在生物学研究领域应用 ——荧光定量切片&芯片扫描学术讲座圆满落幕04-20 环亚生物
GLMY创想仪器丨河南铸锻年会展示优质光谱分析技术04-20
GLMY创想仪器丨亮相江苏东海高纯石英材料产业大会04-18
瑜伽裤有“毒”?Lululemon被曝添加“永久性化学品”:PFAS危害到底有多大?04-17
全自动DNA脉冲场电泳回收仪用于5' 转录组测序及CUT&RUN《Nature》-蚂蚁嗅觉基因选择性表达机制新发现04-17 环亚生物
超长测序文库新思路:Blue Pippin全自动大片段DNA脉冲场电泳回收仪用于Ultra Long 文库构建04-17 环亚生物
文献速递|Blue Pippin全自动DNA脉冲场电泳回收仪用于单分子蛋白组学识别技术开发04-17 APGBio
Pippin 系列全自动DNA片段回收仪用于GUIDE-seq2测序——《Nature》 CRISPR–Cas9 PAM变体研究04-17
展会预告 | 安东帕邀您共赴 Chinaplas 202604-17
免费试用70天!安东帕傅里叶变换红外光谱仪助力药企生产04-17 Anton Paar China
精酿人必看 | 如何让啤酒新鲜度“破局”?三大福利,抓紧来领!04-17 Anton Paar China
邀请函 | 密度黏度联合用户培训会@上海04-17 安东帕中国
展会邀请,欢迎理论指导04-17 上海棱光技术
GLMY创想仪器丨于杭州聚焦再生生物油脂高质量检测04-17
脂质研究必看:2400+产品目录,四大难题一网打尽04-16
第35届化学年会圆满落幕,Sigma-Aldrich®赋能化学,共启化学探索之旅04-16
与时俱进,与药典接轨:一文看懂离子对试剂怎么选04-16 Merck