“沉浸式”体验E&L背后逻辑,助力识别工艺风险(上篇)
2023-02-13 10:18:20, Amber Xi Merck工艺解决方案
E&L (Extractable和Leachable,即提取物和浸出物)研究在保障患者安全,确保上市药品的质量方面起着十分关键的作用,也是无菌药品相容性研究中一直被法规机构高度关注的重点。您还在为了“为什么要考虑E&L验证”而困惑吗?您还在为了“如何进行风险等级确认”而苦恼吗?您还在为了“如何选择模型溶剂进行E&L实验设计”而迷茫吗?您还在为了“安全性评估报告如何进行解读”而头疼吗?如果您也存在这样的疑惑,稍安勿躁,默克带您一起沉浸式体验,通过上下两个篇章深度剖析E&L背后的逻辑。
本期将从E&L验证的必要性,风险等级的确认以及默克提供的E&L验证策略入手,带您了解E&L,助您更早识别并降低工艺风险,助力广大客户通过国内外监管机构的申报要求。
更有安全性评估及实际案例分析,将于下周推送,欢迎持续关注!

可提取物和浸出物研究的必要性
我们都知道,在生产无菌药品时,为了保证药品的无菌性,节约厂房空间和降低生产成本,会考虑使用一次性系统组件代替传统的不锈钢组件,常见的一次性系统组件包含过滤器,搅拌袋,储液袋等,而这些组件中最核心的部分是膜材的构造。

图1:一次性系统组件膜材的制膜工艺
典型的膜材制备工艺中,以树脂等聚合物为原材料,通过添加不同的有机溶剂及其他材料,进行混合搅拌,最后通过铸造和表面修饰等工艺后形成最终满足我们用户需求的膜材。因此,有必要通过E&L的研究来定性定量分析潜在的浸出物,以确保一次性产品在实际应用过程中不会引起药品的质量问题。
无菌灌装后的药品,一般会通过冻干、复融、稀释后通过静脉注射等方式到达患者体内。因此,为了确保一次性产品在应用过程中不会引起药品的安全问题,E&L研究值得被关注,法规对此也提出了明确的要求。


图2:典型的单抗生产工艺流程
典型的单抗生产工艺如图,从细胞培养,细胞破碎,超滤、层析纯化,除病毒过滤,除菌过滤和无菌灌装,以上生产工艺步骤中通常会引入除病毒过滤器,除菌过滤器及无菌灌装等一次性系统组件来满足实际的工艺需求,然而这些一次性塑料组件在与药液接触过程中有可能会释放杂质进入药液。此外,特定工艺过程中控制的工艺温度、工艺时长及一次性组件使用前的灭菌工艺等因素相比于一次性系统组件出厂前的参数会更加苛刻,这些因素综合起来更加有可能进一步提高杂质释放的水平,因此E&L验证是非常重要的关注点。

面对一次性工艺的日益普及,为了确保药品的有效性和安全性,法规监管机构对E&L的要求逐步提高,主要可以参考欧盟GMP 附录1《无菌药品生产》2020年修订版[1],EMA颁布的《药品、活性物质、辅料和内包材无菌指南》[2],BPOG发布的一次性系统标准可提取物方案和最佳实践指南[3], USP665&USP1665 [4] [5],PDA 66号报告[6]和国家药监局参考USP665&USP1665发布的《化学药品注射剂生产所用的塑料组件系统相容性研究技术指南(试行)》[7],这些法规要求和通用指南为E&L在制药企业中的实施提供了非常完善的技术考量。

图3:E&L相关的通用参考指南

USP与BPOG风险评估策略介绍
一次性塑料组件通常会应用在不同的工艺位点,并且考虑到一次性组件材质和接触流体的差异化,E&L验证内容会基于风险高低有所区别。有的用户会考虑将所有一次性组件都进行E&L验证,这样的验证策略不仅会延长项目周期,同时也提高了项目成本。破除“内卷”,你需要了解E&L的研究是基于风险评估进行开展的。

风险评估应当充分考虑可提取物或者浸出物产生的可能性及持续存在的可能性,因此,USP665建议从接触时间,接触温度,接触流体的化学性质和材料反应性这四个维度进行风险等级的确认。工艺流体组分这个维度比较复杂,除了要考虑工艺流体pH, 工艺处方中的有机相含量外,表面活性剂(比如吐温20,吐温80),脂质体,血制品和蛋白含量均需纳入考虑。

图4:USP665 & USP1665 风险等级确认矩阵表
确定好以上4个维度的风险级别后,结合风险评估矩阵表,确认最终的工艺风险等级。某些特定情况,比如工艺中的过滤器在灭菌后有冲洗或者稀释等操作,这样的操作可以降低杂质水平,这种情况称为工艺清除因子;另一种情况,考虑到药品的临床使用情况(比如剂型:口服或者外用剂相比于静脉注射或者吸入剂型的风险要低;给药周期:小于7天;每日给药剂量:小于10 mL),这种情况称为临床消减因子。注意临床消减因子里的三个系数不能进行叠加,最多可以降低一个风险级别。结合工艺清除因子和临床消减因子这两个系数,最初评估的高风险可能被降低1个或者2个风险级别成为中风险或者低风险。

图5:USP665&USP1665 风险评估矩阵表
结合临床消减因子和工艺清除因子调整后的风险等级来制定合适的E&L研究方案。一般情况下,工艺风险级别越高,研究的范畴越广,研究越深入细致,相应的研究投入成本也越高。

图6:USP665&USP1665 基于风险确认研究范畴

BPOG也发布了基于风险的评估策略,BPOG的风险评估策略在USP的基础上增加了两个维度,分别是工艺位点和稀释因子。按照BPOG风险评估的策略,我们在确定各个维度的风险等级后,需要基于各个维度的加权系数及临床消减因子和工艺清除因子来确认最终的风险等级。
默克的Emprove®团队,基于BPOG和USP665的研究策略对大量SUS组件进行可提取物分析研究,积累了丰富的研究数据,可以方便我们用户更加迅速,更加便捷的获取E&L验证报告,助力我们用户加快药品的研发申报审评工作。
默克验证实验室的E&L验证策略主要是参考USP665&USP1665的指南要求进行设计的,同时也会引用Emprove®团队的E&L研究数据,综合出具基于用户特定工艺的E&L验证报告,符合法规要求的同时满足客户更加定制化的需求。

图7:默克基于风险的E&L验证策略

默克基于风险的E&L验证策略
可提取物是基于工艺流体的处方和pH,选择与工艺流体具有相似理化性质的模型溶剂,而且在更恶劣的工艺条件下开展的可提取物研究;浸出物则是选择工艺流体本身,且在工艺条件下开展研究。由于浸出物的量极小,受分离和检测方法的限制,很难被定量或定性。因此,应先获得最差条件下的可提取物数据,将其用于药品的安全性评估。由于可提取物反映了浸出物的最大可能,无论是否要做浸出物试验,可提取物的测试和评估都非常重要。因此,《除菌过滤技术及应用指南》[8]及PDA26号技术报告[9]中的当前要求都是先进行可提取物研究,如有必要再进一步研究浸出物水平。
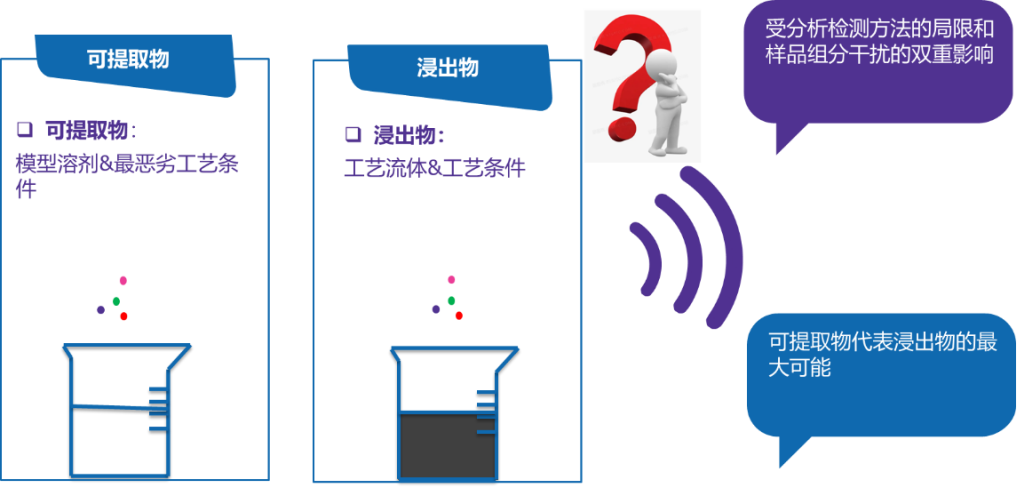
图8:可提取物和浸出物的定义
可提取物方案设计中,最核心也是最关键的因素是模型溶剂的选择。如果模型溶剂选择过于苛刻,导致的结果是可提取物含量偏高于实际水平,基于可提取物数据的安全性评估显示对病人健康安全有显著风险,导致药品申报工作受阻;如果模型溶剂选择过于温和,则研究结果无法代表实际的工艺状况,进而导致药品申报审评工作受阻甚至会影响药品上市后的用药安全。因此,模型溶剂的选择必须具有代表性,通常应具有与产品相同或相似的理化性质,如pH值、极性或离子强度等。默克在模型溶剂的选择方面,不仅参照法规的要求全面评估药品处方和pH,而且会结合实际方案的可行性研究,及实验人员操作上的安全性来制定合理的研究方案。
默克同时会兼顾批间差异及同一个批次重现性对可提取物结果的影响,采取至少2个批次,考虑使用最多次蒸汽灭菌循环、最多次伽玛辐射的次数和剂量、最高过滤温度和最长过滤时间等这些参数,设计可以覆盖最恶劣工艺条件的可提取物研究方案,使研究结果更能代表实际工艺条件。
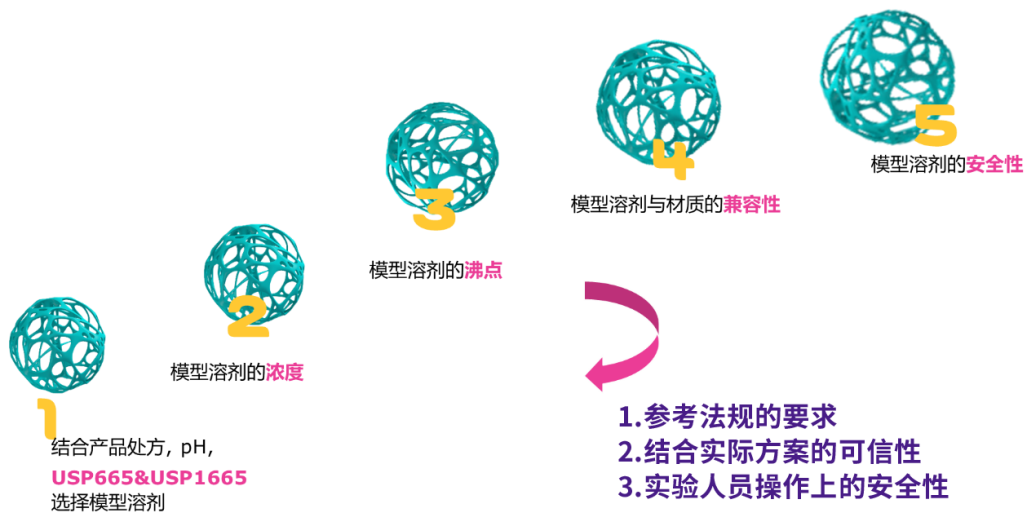
图9:模型溶剂的选择

图10:可提取物的关键影响因素
完成定制化的可提取物方案设计后,下一步是进行提取实验,提取后完成样品的准备和在线分离,最后对分离的化合物进行定性和定量分析。常见定性方法包括pH, 电导率,及FTIR。由于潜在浸出物或可提取物的含量普遍比较低,且混合物直接进行红外解析误差通常比较大,为了确保实验结果的准确性和灵敏度,默克采用RP-HPLC与FTIR两种分析方法结合的方式, 在一定程度上提高了对痕量杂质的鉴定灵敏度。常见的定量方法包括非挥发性残留物(NVR)、总有机碳分析(TOC)以及气相色谱-质谱(GC-MS)、液相色谱-质谱(LC-MS),电感耦合等离子体质谱仪(ICP-MS)。至于到底选择哪几种分析方法,需要取决于实际的药品特性和生产工艺的复杂性。

图11:可提取物的分析方法

本期,我们从产品本身,患者用药安全和法规角度综述了E&L验证的必要性;紧接着,我们从USP665,1665及BPOG的角度综述了风险评估的策略来确定风险等级,明确E&L研究范畴;然后我们介绍了默克的 E&L设计的研究思路。
下周我们会针对E&L数据安全性评估以及实际案例展开深度的解析与分析,欢迎各位持续关注!
如您对默克E&L验证服务感兴趣,
欢迎您扫描下方二维码与我们取得联系~

关于默克工艺解决方案
默克工艺解决方案,凭借可信赖的产品、丰富的生物制药工艺专业知识和卓越的法规支持,为生物制药客户提供全方位支持,以应对各种工艺挑战。
如需了解更多关于默克工艺解决方案,点击此处进入产品资料站。





04-22 荧飒光学
吉艾姆4月双展齐发 | 武汉科仪展+脂在浙里研讨会04-22
应用笔记 | 基于Flex自动化平台的多体液胞外囊泡分离及EV蛋白质组学分析流程04-21 肖伟弟 曾嘉明
CCMT2026开展即高能 | Equator-X™ 双模式测量仪引爆全场04-21
告别预测偏差!Percepta自建专属训练库,pKa预测更准更快04-21 ACDLabs 李丹
世界地球日,查看地球的【愿望清单】04-21
【前沿激荡,智汇北京】IGC 2026圆满落幕,益世科生物共绘细胞基因治疗新蓝图04-21
Turbiscan在陶瓷3D打印粘结剂分散稳定性表征中的应用及关键意义04-21 大昌华嘉
GranuCharge (粉体静电分析仪)用于研究湿度对粉末表面性能的影响04-21 大昌华嘉
生物打印鼻软骨的理想材料:GelMA水凝胶的力学与细胞外基质平衡新探索04-21 大昌华嘉生命科学
Biolin Theta系列接触角测量 | 如何在表面表征应用中使用接触角:前进角04-21 大昌华嘉
大昌华嘉科学仪器荣获Novasina 2025年度“成长与创新先锋奖”!04-21 大昌华嘉
会议预告|华大吉比爱邀您共赴第六届北京临床质谱论坛04-21 华大吉比爱
叮咚!您有一份来自地球的“绿色盲盒”待拆封04-21 安捷伦科技
聚焦小核酸与多肽前沿分析:第一届创新药物研发与质量评价技术交流会在沪圆满举办04-21 安捷伦科技
糖基化全流程质控:消耗品方案一站式解决04-21 安捷伦科技
药物分析排忧解难系列 | 自动柱前衍生化方案,完美应对样品复杂前处理04-21 安捷伦科技
“衣”路前行,“安”全守护 | 安捷伦 PFAS 解决方案守护运动健康04-21 安捷伦科技
零压力,低成本 | 安捷伦官方认证翻新仪器开启“以租代售”新模式04-21 安捷伦科技
ESCMID 2026 爆点 | MiSeq i100系列携6项病原精准测序应用数据亮相04-21