Microbiome | 单细胞转录+16s+代谢联合:浙大孙会增团队探究围产期奶牛过度脂解过程中肠道微生物与免疫抑制的关系
2023-05-25 19:47:08, 质谱创新组学 上海欧易生物医学科技有限公司
2023年3月,浙江大学乳业科学研究所孙会增课题组在Microbiome(IF:16.837)发表了题为“Gut microbiome is linked to functions of peripheral immune cells in transition cows during excessive lipolysis ”的研究成果,该研究运用单细胞转录组、16S扩增子测序、宏基因组学和靶向代谢组学研究方法,探究了围产期过度脂解奶牛的肠道微生物组与产后免疫抑制之间存在潜在联系,研究发现血浆中甘氨石胆酸(GLCA)、牛黄胆酸(TLCA)的减少可通过降低GPBAR1的表达,在过度脂解过程中促进单核细胞的免疫抑制。
中文标题:肠道微生物组与过渡期奶牛的外周免疫细胞功能有关脂肪过度分解期间
研究对象:粪便,血浆,单核细胞
发表期刊:Microbiome
影响因子:16.837
发表时间:2023年3月
运用生物技术:单细胞转录组、16S 扩增子测序、宏基因组学、靶向代谢组学
01
研究背景
围产期(分娩前后3周)是奶牛生命的关键阶段,随着采食量的减少和支持泌乳的能量需求增加,脂肪组织溶解过度。过度脂解通常伴随免疫抑制而发生,其中宿主代谢和免疫功能都会发生改变。然而,目前对过渡期(围产期)奶牛宿主代谢与免疫调节之间的关联和因果关系缺乏了解。本研究旨在使用16S扩增子测序、宏基因组测序、靶向代谢组学和scRNA-seq来分析肠道微生物组、代谢组和免疫细胞转录组,以发现过度脂解相关免疫抑制背后的机制。整合多组学结果数据有利于对过渡期奶牛过度脂肪分解过程中发生复杂过程的了解。
02
研究思路
03
研究方法
1. 实验分组
围产期荷斯坦奶牛(每组9个)过度脂解组(HNF),血浆非酯化脂肪酸(NEFA)浓度>750 μmol/L正常脂解组(LNF),血浆非酯化脂肪酸(NEFA)浓度<600 μmol/L
2.主要技术
2.1. 生理/病理分析:表型特征、血液参数、炎症生物标志物、氧化应激生物标志物
2.2 免疫细胞功能分析:单细胞转录组学
2.3 粪便微生物组分析:16S rRNA测序
2.4 粪便宏基因组分析
2.5 粪便/血浆靶向代谢组学:胆汁酸靶向代谢组学
04
研究结果
1. 过度脂肪分解影响围产期奶牛产后生理状态
通过分析血浆代谢参数、炎症和氧化应激的生物标志物,测量产奶量和体况评分(BCS)来评估过渡期奶牛的生理状况。在产前一周,低/正常脂肪分解(LNF)和高/过度脂肪分解(HNF)的奶牛之间,这些参数没有明显的差异。产后一周,HNF奶牛天冬氨酸转氨酶(AST)、β-羟丁酸(BHBA)、非酯化脂肪酸(NEFA)显著高于LNF奶牛。
2. 过度脂肪分解抑制免疫细胞功能
从单细胞中共确定了26个集群(C0-C25),将这些集群注释为10种主要的免疫细胞类型(图1A,B)。五个簇(C0、C1、C6、C8、C12)被注释为B细胞,C15被注释为浆细胞(PC)(图1B),C23被注释为循环B细胞(图1B),九个簇(C4、C7、C9、C10、C14、C16、C18、C22和C25)被鉴定为T细胞(图1B),C20被注释为NK细胞,C2、C3和C11被注释为中性粒细胞(NEU)。由于标记基因TGM3和CSF3R的高表达,单核细胞(MON)中确定了两个单核细胞(C5,C19),在C5中标志基因LYZ和CD14的较高表达表明含有CD14+MON细胞,标志基因FCGR3A和LYZ在C19群中的较高表达表明含有FCGR3A+MON细胞(图1B)。
与LNF奶牛相比,下调的DEGs主要富集在免疫细胞功能的生物途径上。在中性粒细胞(NEU)中下调的DEGs与中性粒细胞趋化作用、迁移、吞噬作用有关。MON中下调的DEGs与细胞迁移、增殖、吞噬作用有关(图1C)。

图1 | 外周免疫细胞的单细胞景观的构建
3. 过渡期奶牛在过度脂肪分解过程中粪便细菌群落发生变化
Alpha多样性分析显示,与LNF相比,HNF的Simpson指数降低(图2A)。Beta多样性分析显示,粪便细菌群落是基于脂肪分解而聚类(图2B)。在门水平上,HNF中厚壁菌门的相对丰度高于LNF,拟杆菌门和变形杆菌门的相对丰度低于LNF。在LNF和HNF牛之间有7个显著不同的科,Ruminococcaceae在HNF奶牛中丰度较高。

图2 | 使用 16S 扩增子测序过渡期奶牛的粪便细菌群落进行分析
4. 脂肪分解状态改变了过渡期奶牛的粪便宏基因组
Alistipes、Anaerotruncus sp.CAG、Firmicutes bacterium CAG和Treponema JC4在HNF中含量较高,其余17种细菌在HNF中含量较低(图3C)。在LNF和HNF之间有20个不同含量的古生物物种,与LNF相比,只有Thermoplasmata古菌在HNF中含量高(图3D)。Netshift分析显示共有14个驱动物种对与脂肪分解有关的微生物组有贡献(图3E)。HNF中与脂质代谢相关的途径“脂肪酸延长”和“类固醇降解”的相对丰度低于LNF。HNF奶牛的肠道微生物“次级胆汁酸(SBA)生物合成”途径的丰度显著高于LNF奶牛(图4B)。
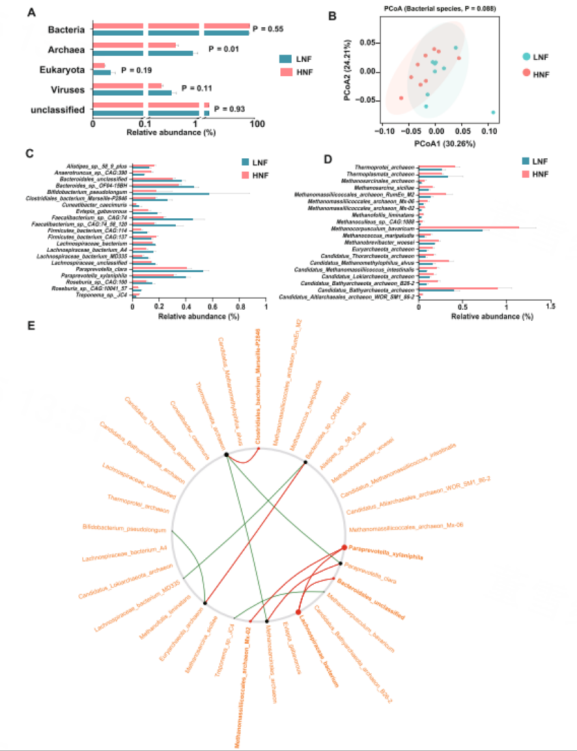
图3 | 使用宏基因组测序分析脂肪分解状态不同的过渡期奶牛粪便微生物组
5. 脂肪分解过度的过渡期奶牛的胆汁酸谱发生变化
粪便胆汁酸(胆汁酸)的靶向代谢组学分析显示,HNF的次级胆汁酸总量高于LNF。在胆汁酸中,HNF中的甘氨石胆酸(GLCA)、牛黄胆酸(TLCA)和甘氨鹅去氧胆酸(GCDCA)的浓度显著低于LNF组,3-脱氢胆酸(3-DHCA)和12-KLCA的浓度高于LNF(图4D)。
粪便中Treponema sp. JC4和甲烷串珠菌 Mx02的相对丰度与粪便中12-KLCA、3-DHCA、ApoCA、IsoLCA和LCA等胆汁酸的浓度呈正相关。拟杆菌属OF04-15BH、Paraprevotella clara和Paraprevotella xylaniphila的相对丰度与血浆中GLCA和TLCA的浓度呈正相关(图4E)。

图4 | 不同脂肪分解状态的过渡期奶牛粪便微生物组的KEGG途径
6. HNF奶牛单核细胞功能的抑制与胆汁酸代谢有关
胆汁酸受体是肠道微生物群和宿主免疫调节之间的连结之一。结果评估了胆汁酸受体基因(BARs)表达与免疫细胞功能之间的联系。MON中GPBAR1和NR1H3较高表达(图5B),HNF奶牛只有CD14+MON的GPBAR1表达量较低,而NR1H3在CD14+MON和FCGR3A+MON的表达量均低于LNF牛(图5C)。与BA调节有关的下调DEGs和单核细胞四种丰富的免疫功能(对细胞因子的反应、对病毒的反应、防御反应和1型干扰素)只在CD14+MON中呈正相关,而在FCGR3A+MON中不呈正相关(图5E)。

图5 | 胆汁酸与免疫细胞功能之间的关联
05
研究结果
脂质分解会导致围产期奶牛的免疫抑制,进而影响乳制品行业的生产健康。该研究结合了奶牛肠道微生物组、代谢组和宿主单细胞免疫转录组的研究,研究过渡期奶牛的过度脂肪分解。结果表明,脂肪分解过度的奶牛中次级胆汁酸和粪便微生物合成增加,单核细胞与与细胞迁移、吞噬作用、对细胞因子的反应的功能降低。推测由于肠道微生物组的组成和功能的改变,血浆中胆汁酸(GLCA、TLCA)的浓度降低,可激活免疫细胞上的GPBAR1,在过度脂肪分解过程中导致围产期奶牛的免疫抑制。研究揭示了脂肪分解过度的过渡期奶牛的肠道微生物组、胆汁酸代谢和免疫抑制之间的潜在联系。

文章推荐
文章通过单细胞转录组、16S扩增子测序、宏基因组学和靶向代谢组学研究方法,探究了围产期奶牛的肠道微生物组和过度脂解相关免疫抑制背后机制的联系,揭示过度脂肪分解的奶牛微生物组相关的病理变化。
参考文献
本文章出处:DOI: 10.1186/s40168-023-01492-3
小鹿推荐
关注
鹿明生物提供优质的空间代谢组服务
空代仪器平台
已搭建2套AFADESI-MSI质谱成像系统+1套Waters DESI-MSI质谱成像系统
项目执行
已落地执行项目百余项、检测组织样本类型20+;
定性算法经过多维校准
定性结果同时考虑物质表达空间情况、加和离子及同位素峰表达强度相似性、同位素表达空间分布相似性、非靶向质谱数据和空代自建数据库进行校准。
项目实测结果
可实现定性代谢物数量:1000-3000个代谢物
无偏好性检测代谢物::70%为700Da以下的小分子物质,30%为脂质类物质,更加适合代谢组学研究方向;
精彩合集,欢迎收藏
|代谢组学项目文章合集
|鹿明蛋白/代谢文献分享合集
|空间代谢组学专辑
|4D蛋白质组学专辑
|云平台&生信宝典
|多层组学项目文章合集
|中医药研究
|数据“库”系列专题
猜你想看


07-01 英斯特朗
连载 | 药物一致性评价与粒度分析(三)07-01 欧美克仪器
【仪器百科】LS-909丨干湿二合一激光粒度分析仪07-01 欧美克仪器
标准物质解决方案 | PFASs(全氟及多氟化合物)06-29
第九期阿尔塔有约 | 环境专题【新污染物:PFAS】技术研讨会精彩回顾及提问解答06-29
“绿色技术范式”,分析化学未来发展方向——访中国分析测试协会副理事长、辽宁省分析科学研究院原院长刘成雁教授06-29 转载仪器信息网
华西医院-标准型数显脑立体定位仪、双通道体温维持仪、体式显微镜安装完成06-29 迈越生物
科鉴检测助力2家仪器企业获得首批产品可靠性认证证书06-28 科鉴检测
德国耶拿:锂电池生命周期分析解决方案06-28 德国耶拿
AI已来!生命科学本科教学如何紧跟技术浪潮06-28 Opentrons
盛瀚售后,五星级服务的秘诀是什么?06-28 SHINE
专为汽车制造商打造的柔性解决方案——实现制程控制06-28
西北工业大学-脑立体定位仪安装完成06-28 迈越生物
会议邀请 | 第九届海上检验医师论坛06-28
卓立要闻 | 创新发展ing…6月卓立“大事小情”速览06-28 光电行业都会关注
打造信任合作伙伴!2024年度卓立汉光客户满意度调查开启06-28 光电行业都会关注
如何挑选适用于三阶光学非线性的测量系统?Z扫描测量系统来助力!06-28 光电行业都会关注
招聘启事—中国科学院沈阳自动化研究所微纳光学测量表征技术课题组06-28 光电行业都会关注
谱育科技作为主要完成方 荣获2023年度国家科学技术进步一等奖和二等奖06-28 点击关注→
仪器原理丨顶空仪与吹扫捕集仪科普小知识06-28 天美色谱