ISO 10993-18:2020:简化医疗设备材料的化学表征
2026-04-22 10:23:57, ACDLabs Advanced Chemistry Development, Inc. (ACD/Labs)

医疗设备在生产、包装或储存过程中,不可避免会存在可提取物与可浸出物(以下简称E&Ls)。E&Ls分析是保障医疗产品安全的核心环节,它旨在解决两个关键问题:“药品包装或医疗设备可能释放出哪些物质?”以及“这些物质是否会对患者造成危害?”
E&Ls研究需进行严谨设计与风险管理,且必须具备科学依据,研究时需综合考量设备类型、设备应用场景、接触时长等因素。因此,近年来监管机构对E&Ls相关研究的关注度持续提升,这一趋势也在意料之中。
相关法规对医疗设备上市前审批、设备备案、标签标识、不良事件报告、电子签名等全流程均作出规范。尽管针对医疗设备的监管指南数量众多,但内容往往存在模糊性,导致科研人员难以确定自身是否已满足全部监管要求。


对于预充式注射器、皮肤贴剂、植入物等各类医疗设备而言,适用的指南通常不止一项。大多数产品需要满足多项监管要求,且根据设备的使用方式和使用地区不同,这些要求往往存在重叠。
ISO 10993系列标准是生产商、供应商及实验室的重要参考依据,它聚焦医疗设备生物学评价,适用于与人体直接或间接接触的设备,助力确保所用材料对患者安全无害。
ISO 10993-1将生物学评价纳入更全面的风险管理流程。其最新版本ISO 10993-1:2025与ISO 14971标准的衔接更为紧密,倡导并强化基于设备预期用途,采用系统化方法识别、评估和管控生物学风险。

本文重点介绍 ISO 10993-18:2020。该更新版标准替代了2005年版本,其中优化了化学表征流程的流程图,并提供了更清晰、更全面的定义,以加深对分析测试的理解。
ISO 10993-18:2020的核心要点包括:在实际临床使用条件下测定可提取物与可浸出物,并利用该数据评估材料生物相容性。
可提取物与可浸出物 (E&Ls) 的
化学表征
ISO 10993-18:2020是一套用于医疗设备表征的标准。该指南分为多个章节,首先阐述化学表征流程。
化学表征研究的整体设置可概括为三个步骤:提取、检测、鉴定与定量。
提取
提取试验旨在评估医疗设备及其材料可能产生的影响。ISO 10993-18:2020标准为选取最适宜的提取条件提供了指导。
提取条件的选择取决于医疗设备的类型及其具体应用场景。虽然有时需要采用较为苛刻的提取条件,但必须把握好精细的平衡:不应选用过于剧烈的条件,以免改变可提取物的组成特征。
提取方式主要包括:
强化提取条件:相较于临床实际使用条件,可促使更多化学成分释放的提取条件。
穷尽提取:采用多步提取,直至单次提取步骤中获得的提取物量低于首次提取量的10%。
模拟使用条件:采用模拟临床实际使用方式进行的提取。
确定提取类型后,还可进一步确定提取溶剂、温度、时间等其他试验条件。
检测
ISO 10993-18:2020指南给出了相关建议,以帮助选用最合适的分析技术。针对不同化合物,所需的分析方法也各不相同。下图列出了针对特定类别化合物的推荐分析技术。

其它需要考虑的因素包括:
分析技术的应用方式
筛查法:对提取物中所有潜在化合物进行全面筛查。
靶向法:针对已知目标物进行检测,实现低定量限 (LOQ) 与高准确度。
化合物类别:为覆盖从挥发性到非挥发性等所有类别化合物,通常需要采用多种分析技术联用。
可电离物质:对于电离效率低的化合物,可能需要使用高灵敏度仪器进行检测。
综合考虑以上所有因素,即可选用并应用最合适的分析技术,确保对所有化合物实现充分提取与有效检测。
用于E&Ls鉴定和定量的解决方案
对检测结果达到或超过毒理学阈值的化合物,需进行针对性的鉴定与定量分析。
ACD/Labs公司的MS Structure ID Suite等软件,依托分析化学技术,简化、自动化并高效化医疗设备中可提取物与可浸出物的化学表征流程。该软件可帮助科研人员快速识别谱图中的离子、归属碎片离子,并可靠地验证结果。所有检测数据均会采集并存储于统一数据库中,便于查阅与追溯。
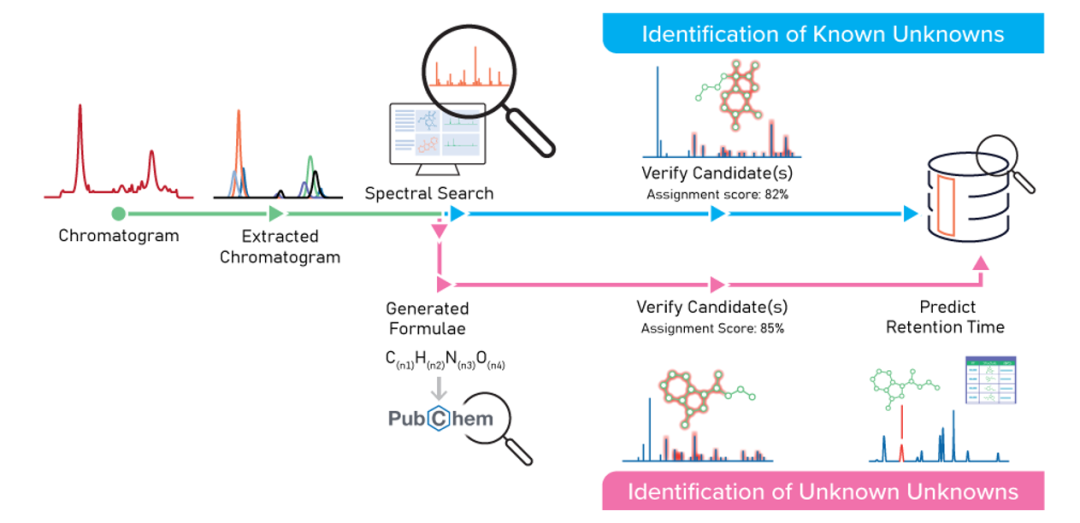
下图所示工作流展示了美敦力公司如何运用ACD/MS Structure ID Suite加速可提取物与可浸出物的化学表征。
待分析物完成鉴定后,下一步即为确定含量。科研人员可建立校准曲线并对分析物进行定量计算。下图展示了MS Structure ID Suite中的定量分析工作流程。

MS Structure ID Suite能够助力加快组分鉴定速度、提升鉴定结果的可信度、提高定量分析准确性,从而保障医疗设备的使用安全。
鉴定等级
ISO 10993-18:2020要求在化学表征报告中注明E&Ls的鉴定等级,但想要通过权威对照物质对每一个鉴定结果进行确证是不现实的。为充分完成E&Ls的鉴定与报告,需要建立并采用置信度分级。按置信度由高到低可分为:确证鉴定、高度可信鉴定、初步鉴定、推测鉴定、未鉴定。置信等级越高,用于毒理学评估时的不确定性就越低。
最高置信等级(确证鉴定)仅在满足以下三项标准时方可使用:
与谱图库中质谱图的匹配度足够高
在所用仪器上对该化合物的保留时间进行验证
使用权威对照品测定保留时间与质谱图
当报告的化合物浓度接近其每日允许暴露量时,采用确证鉴定尤为重要。
分析评估阈值的确定与毒理学风险评估
所有上市产品均需开展毒理学风险评估 (TRA),并向监管机构提交相关报告。进行毒理学风险评估时,必须考虑允许限度与分析评估阈值 (AET),相关流程还需符合其他ISO标准要求(尤其是ISO 10993-17)。
ISO 10993-18:2020标准体系中包含详细建议与指南,可辅助确定分析评估阈值。AET基于给药剂量与给药途径计算得出,是判定某一化学物质是否存在毒理学风险的基准。
该阈值需根据设备用途、接触方式及接触时长,为每种化学品单独设定。凡检测浓度达到或超过此阈值的化合物,均需进行鉴定、定量,并提交报告用于毒理学评估。此阈值通过剂量阈值 (DBT)、提取体积以及测试设备数量共同计算得出。
剂量阈值 (DBT) 根据化学品类型,通过以下两种方式确定:
安全关注阈值 (SCT):低于该阈值时,可浸出物的剂量极低,其致癌或非致癌毒性带来的安全风险可忽略不计。
毒理学关注阈值 (TTC):化学物质暴露量低于该水平时,对人体健康风险不显著。
设定并满足分析评估阈值要求,是监管申报流程的重要环节,也是保障医疗设备安全性的必要条件。
医疗设备的安全性评估
医疗设备的评估工作需要化学表征与毒理学评估相结合。化学表征用于对化合物进行痕量检测与定量分析,而毒理学则用于判断这些物质是否会对患者构成风险。
ISO 10993-18:2020将这两部分内容整合统一,为分析测试提供了更清晰的指导,并与其他ISO标准实现了更好的衔接。
点此了解阿斯利康如何管理E&Ls数据:

点击文末
阅读原文
即可阅读原文章
04-22
会议预告|华大吉比爱邀您共赴第六届北京临床质谱论坛04-21 华大吉比爱
叮咚!您有一份来自地球的“绿色盲盒”待拆封04-21 安捷伦科技
聚焦小核酸与多肽前沿分析:第一届创新药物研发与质量评价技术交流会在沪圆满举办04-21 安捷伦科技
糖基化全流程质控:消耗品方案一站式解决04-21 安捷伦科技
药物分析排忧解难系列 | 自动柱前衍生化方案,完美应对样品复杂前处理04-21 安捷伦科技
“衣”路前行,“安”全守护 | 安捷伦 PFAS 解决方案守护运动健康04-21 安捷伦科技
零压力,低成本 | 安捷伦官方认证翻新仪器开启“以租代售”新模式04-21 安捷伦科技
ESCMID 2026 爆点 | MiSeq i100系列携6项病原精准测序应用数据亮相04-21
还有人不知道吗?代谢组才是多组学联用的灵魂04-20
【星品周 | 好礼翻倍】外泌体富集及miRNA提取攻略04-20
InnoQuant激光共聚焦荧光扫描仪助力组织切片全景扫描和分析04-20 环亚生物
InnoQuant激光共聚焦全景玻片扫描在非小细胞肺癌肿瘤微环境研究中的应用04-20 环亚生物
拍出最真实最清晰的图片—InnoQuant助力生物组织荧光切片扫描和分析04-20 环亚生物
全景激光共聚焦扫描技术在生物学研究领域应用 ——荧光定量切片&芯片扫描学术讲座圆满落幕04-20 环亚生物
ESCMID 2026爆点|tNGS四连杀:泌尿手术、耐药结核、血液肿瘤、HIV全覆盖04-20
GLMY创想仪器丨河南铸锻年会展示优质光谱分析技术04-20
GLMY创想仪器丨亮相江苏东海高纯石英材料产业大会04-18
多组学技术赋能青年科研力量,加速科研源头创新与转化04-17
DRAGEN v4.5支持因美纳全新TruPath Genome与5碱基检测方案,驱动生殖系、肿瘤学及多组学研究洞察04-17 因美纳
