热力全开:蛋白质热稳定实验技巧与问题排查全解析(上篇:原理和实验)
2025-01-21 12:30:08, TAS 马克 赛默飞世尔科技生命科学产品

蛋白热稳定性实验(Protein Thermal Shift, PTS)技术,也被称为差示扫描荧光法(Differential Scanning Fluorimetry,DSF),原理是在特定染料环境中蛋白质构象随着温度递增发生改变,通过qPCR仪器检测荧光信号的变化,测定蛋白质熔解温度(Tm),达到评估蛋白质的热稳定性的目的。PTS技术以其操作简单、灵敏度高、高通量等特点,广泛应用于蛋白质稳定性研究、蛋白结构和构象分析、蛋白-配体相互作用研究以及蛋白质稳定剂、抑制剂、辅助因子的筛选。与传统方法(圆二色谱(CD)、差示扫描量热法(DSC)或等温滴定量热分析(ITC))相比,PTS技术需要的蛋白量更少,优化步骤更为简便。赛默飞提供了一套完整的PTS实验工作流程,包括反应试剂盒、qPCR仪器和数据分析软件包。本文将详细阐述PTS实验的设计、操作步骤、数据分析及问题排查。

在PTS实验中,通过添加对蛋白质疏水基团具有高亲和力的荧光染料,监测荧光信号随温度变化的情况。当蛋白质保持折叠状态时,疏水基团折叠在蛋白内部,因此荧光信号较低;而随着蛋白质受热变性,其构象发生变化,疏水基团暴露,染料与其结合,从而使荧光信号增强。通过分析荧光信号与温度变化的关系,我们可以得到熔解曲线,并从中计算出Tm值(玻尔兹曼Tm或者导数法Tm)。Tm值的变化反映了不同条件下或者不同蛋白质稳定性的差异(图1)。
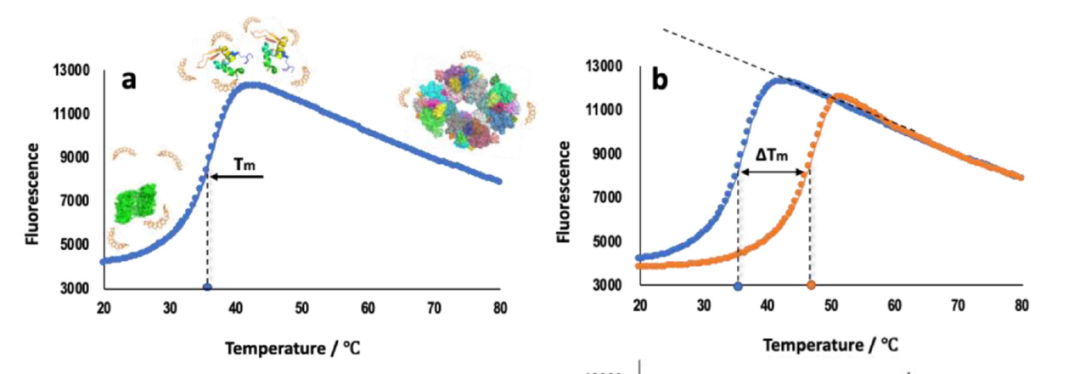
(图1 引自:Kai Gao et al. Biophysical Rev (2020) 12:85–104)

01 | 试剂盒的选择 |
针对PTS实验,赛默飞提供了两款试剂盒供您选择:Protein Thermal Shift™ 启动试剂盒(货号: 4462263)和Protein Thermal Shift™ 染料试剂盒(货号: 4461146)。启动试剂盒除了包含染料和缓冲液外,还包含了对照蛋白和对照配体,非常适合初次进行PTS实验的研究人员。试剂盒中的对照蛋白和配体不仅有助于熟悉实验流程,还可以作为阳性对照,帮助排查实验中可能出现的问题。
02 | 蛋白类型的选择 |
在进行PTS实验前,评估您感兴趣的蛋白质是否适合使用这种方法至关重要。以下是一些考虑因素:
热稳定性:确定蛋白质是否合适热稳定性实验。如果蛋白质的熔点(Tm)超过98℃,可能无法产生明显的熔解阶段,您可能需要考虑其他方法来检测蛋白质的稳定性。
疏水性:蛋白质在天然状态下是否具有外部疏水基团,如有较多的外部疏水基团,可能导致背景信号过高;相反,如果蛋白质没有足够的内部疏水基团,您可能会观察到较低的荧光信号。
结构域和寡聚体:多结构域或形成寡聚体的蛋白质可能在熔解曲线中显示多个熔解阶段。可以考虑单独获取包含活性位点的结构域,或筛选缓冲液/添加剂以确定蛋白质的热稳定性。
下面列出了一些不适合PTS实验的蛋白质类别:
膜蛋白:膜蛋白通常具有复杂的结构,包括多个跨膜区域和亲水/疏水结构域等。大多数膜蛋白缺失可以和PTS染料结合的游离硫辛酸基,无法得到预期的实验结果。
有聚集倾向的蛋白:高温下易形成聚集体,可能会干扰荧光信号的检测。
含铜蛋白质:可能与实验中使用的染料发生反应,影响荧光信号。
高自发荧光的蛋白质:可能会与染料信号产生干扰,影响结果的准确性。
容易降解的蛋白质:在实验过程中可能会发生降解,无法获得准确数据(影响结果的可靠性)。
需要还原剂稳定的蛋白质:依赖的还原剂如DTT,可能与染料发生反应,干扰实验结果。
在进行PTS实验前,了解蛋白质的物理化学特性和稳定性非常重要。如果蛋白质属于上述任何一种类型,可能需要考虑使用其他技术,如圆二色谱(CD)、差示扫描量热法(DSC)或等温滴定量热分析(ITC)来评估其热稳定性。
03 | 对于可以用于PTS 实验的蛋白,请注意以下几个方面: |
a. 样品纯化:确保蛋白质样品具有高纯度(90%以上),无聚集和降解。通常采用色谱法进行纯化,并使用SDS-PAGE或动态光散射等方法验证样品的纯度和均一性;
b. 样品浓度:测定蛋白质的准确浓度,通常采用紫外吸收法(如280 nm处的吸光度)或Bradford、BCA等蛋白定量试剂盒;
c. 蛋白状态:蛋白质样品应该在其天然状态下稳定,没有发生变性或不适当的修饰;
d. 样品储存:蛋白样品应在低温(如-80 °C)储存,避免反复冻融。
04 | 缓冲液选择 |
在PTS实验中,选择合适的缓冲液对于确保蛋白质的稳定性和实验的准确性至关重要。以下是一些关于缓冲液的选择和优化建议:
a. 缓冲液类型:根据蛋白质的等电点和稳定性选择适合的缓冲液。测试过可适配PTS染料的缓冲液包括HEPES、Tris、KPO4(磷酸钾)、柠檬酸钠(C6H5Na3O7)缓冲液以及甘氨酸盐酸盐(C2H5NO2.HCl)缓冲液。
b. pH优化:缓冲液的pH需要精心调整,以确保蛋白质在实验条件下稳定。PTS实验在pH 2.0 – 9.0的范围内都能得到结果,但是对于大多数蛋白质而言建议使用中性pH(6.8-7.4之间)。
c. 离子强度:离子强度对蛋白质的稳定性和折叠状态有显著影响。可以通过添加盐类来调整离子强度,但需注意过高的盐浓度可能导致蛋白质聚集。
d. 避免高粘度:高粘度的缓冲液成分可能会增加背景荧光,从而影响实验结果的准确性。因此,应避免使用高粘度的缓冲液成分,如高浓度的甘油。

对于每一个反应,建议做4个复孔
1 | 将Protein thermal shift 染料从1000 ×稀释至8 ×,需确保每次实验都使用新鲜稀释的染料,避免使用剩余或新旧混合的稀释染料。稀释用的缓冲液可以是试剂盒里带的缓冲液,也可以是实验中待筛选的缓冲液。染料稀释之后,建议观察其是否有沉淀、聚集等异常情况(会影响实验效果)。 | ||||||||||
2 | 将96孔板/8联管放置于冰上,根据下面的加样顺序配制体系(以20微升反应体系为例) | ||||||||||
注意: a. 蛋白热稳定性实验推荐的反应体积是10 μL- 50 μL,可以根据实验条件进行选择。 b. 建议在实验的最后步骤中加入PTS染料。应先将蛋白质与配体进行孵育,以减少染料与折叠状态的蛋白质之间可能发生的相互作用,同时降低染料与配体在结合到折叠蛋白质时的竞争效应。通过这种方式可以有效地减少背景噪声,例如,防止染料促进原本不结合的配体与蛋白质的结合,以及避免染料引发的配体与蛋白质的非特异性聚集。 c. 染料的终浓度可在1 × - 20 ×之间进行优化。 | |||||||||||
3 | 对于PTS实验,我们建议您准备对照组: a. 无蛋白对照(NPC):仅包含缓冲液、水和染料的反应体系。如果NPC孔位荧光信号高,可能表明孔位或反应体系受到污染,或者染料和缓冲液/耗材发生了相互作用。 b. 仅配体对照(LOC):仅包含配体、缓冲液、水和染料的反应体系。如果LOC孔位的熔解曲线与NPC孔位明显不同,可能表明配体与染料发生了相互作用。如果配体与染料结合,可能会掩盖蛋白质与染料的相互作用,从而影响结果的准确性。 | ||||||||||
4 | 体系配制完成之后,将每孔反应体系上下吹吸10次以充分混合,然后 1000 rpm 离心 1分钟,放置于冰上等待上机。 | ||||||||||

推荐使用Applied Biosystems™ 的qPCR 仪器(7500/7500 Fast(V2.0.4之后版本,其中V2.4版本的数据不能直接导入PTS二级分析软件,可以用V2.3软件打开分析保存之后再导入)、QuantStudio系列(QS1、QS1 Plus、3、5、6Flex、7Flex、6Pro、7Pro、QSDX、QS12K)qPCR仪器、ViiA7(V1.0之后版本)、StepOne/StepOne Plus(V2.1 之后版本))进行蛋白熔解曲线实验,后续生成的.eds数据可以直接导入二级分析软件(Protein Thermal Shift Software)进行数据分析。本次以QS5仪器使用为例,介绍如何进行实验设置,如果您使用的是ABI其他型号的仪器,可以参考Protein Thermal Shift™ studies USER GUIDE中其他类型仪器的设置方法,文本链接如下:
(https://www.thermofisher.cn/TFS-Assets/LSG/manuals/MAN0025600_Protein_Thermal_Shift_UG.pdf)
1 | 双击桌面图标,开启 QuantStudio Design & Analysis Software,或从开始菜单> All Programs > Applied Biosystems > QuantStudio Design & Analysis Software开启软件。 |
2 | 进入主界面后,点击“ Create New Experiment”(图2)。  图2 |
3 | 在“ Properties”界面设置实验属性(图3): a. 输入实验的名称; b. 选择仪器型号; c. 选择仪器的Block(加热模块)类型; d. 选择实验类型为:“Melt Curve” e. 选择实验试剂类型:“Other” f. 选择运行模式(Run mode):“Standard” 。  图3 设置完成之后,点击“Next” 进行程序设置。 |
4 | 程序设置(图4) 设置如下反应条件: Step 1——25 ℃(升降温速率设置为 1.6 ℃/s)——2 min Step 2——99 ℃(升降温速率设置为 0.05 ℃/s)——2 min 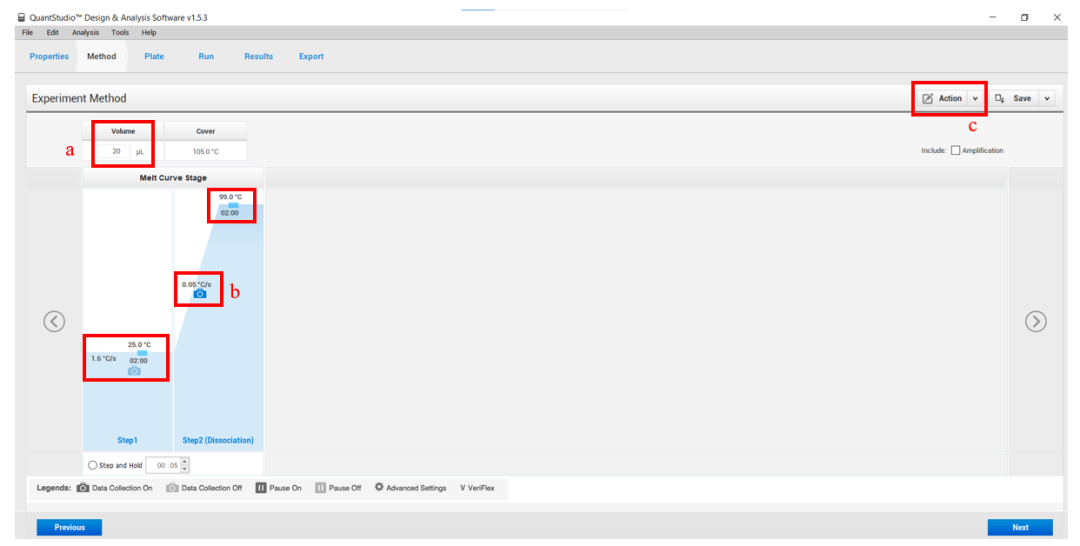 图4 注:如果您的蛋白有较低的熔解温度,可以把初始温度从25 ℃设置为4 ℃;(a)反应体积根据实际情况填写;(b)25 ℃~95 ℃升温过程中需要采集信号,请确保荧光采集信号呈现为打开状态(照相机颜色为深蓝色)。 反应条件设置之后,点击“Action”(c)> “Optical filter settings”设置信号采集通道(QS5-96 well型号仪器,在melt curve filter处将默认的X1-M1取消勾选,改为勾选“X1-M3”,然后点击 “Close”即可 图5)。如果是ABI其他型号的仪器,请按照Protein Thermal Shift™ studies USER GUIDE中对应机型设置。  图5 |
5 | 设置布板信息 程序设置之后点击“Next”即可进入布板界面(Plate),在“Quick setup”界面把参比荧光(Passive reference)改为“None”,在“Advanced setup”界面把Targets的报告基团“Reporter”设置为“ROX”,淬灭基团“Quencher”设置为“None”,然后在对应的孔位、勾选Target和Sample信息即可保存、运行实验(图6)。  图6 针对于QS5 仪器,点击运行之后,软件上会弹出提示:“Start Run Validation: The filter set has not been selected for following target: ROX (x4-m4). Do you want to proceed?”(图7),选择 Yes 继续实验即可。 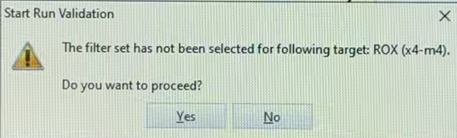 图7 |
综上,我们介绍了蛋白热稳定性实验的原理、样本准备、体系配制以及上机操作等。下期我们将给您带来数据分析以及问题排查等相关内容,敬请期待。如果您在实验中遇到问题,欢迎致电4008208982-2-2,我们技术支持团队将竭诚为您服务。
参考文献:
Kai Gao et al. Biophysical Reviews (2020) 12:85–104
Taiasean Wu et al. STAR Protocols 4, 102688, December 15, 2023
Applied Biosystems. Protein Thermal Shift™ studies USER GUIDE
Taiasean Wu et al. https://doi.org/10.1101/2023.01.23.525251, Posted January 28, 2023.
Katarzyna A et al. Anal. Chem. 2010, 82, 3796–3802

04-23 Dr. Dai
MSTD系列显微镜专用电动滑台:显微镜下图像分毫必现04-23 光电行业都会关注
展会回顾|“融两业共生之力 筑湾区超级枢纽”2026大湾区创新生态大会04-22 谱临晟
荧飒光学践行企业社会责任,赋能光电人才高质量培养04-22 荧飒光学
天平安装丨现场直击地震对天平的影响,几十台天平瞬间“跳动”?04-22 小普
报名通知丨英斯特朗塑料力学测试高阶培训研讨会04-22 英斯特朗
成都科林分析邀您共赴TFF·2026酒类风味分析与感官评价暨创新技术论坛,期待与您相遇!04-22
吉艾姆4月双展齐发 | 武汉科仪展+脂在浙里研讨会04-22
应用笔记 | 基于Flex自动化平台的多体液胞外囊泡分离及EV蛋白质组学分析流程04-21 肖伟弟 曾嘉明
CCMT2026开展即高能 | Equator-X™ 双模式测量仪引爆全场04-21
告别预测偏差!Percepta自建专属训练库,pKa预测更准更快04-21 ACDLabs 李丹
世界地球日,查看地球的【愿望清单】04-21
【前沿激荡,智汇北京】IGC 2026圆满落幕,益世科生物共绘细胞基因治疗新蓝图04-21
硬核方案护航核安全|衡昇质谱斩获核材料检测装备大奖04-21
会议预告 | 英盛生物邀您共赴2026第六届北京临床质谱论坛!04-21
Turbiscan在陶瓷3D打印粘结剂分散稳定性表征中的应用及关键意义04-21 大昌华嘉
GranuCharge (粉体静电分析仪)用于研究湿度对粉末表面性能的影响04-21 大昌华嘉
生物打印鼻软骨的理想材料:GelMA水凝胶的力学与细胞外基质平衡新探索04-21 大昌华嘉生命科学
Biolin Theta系列接触角测量 | 如何在表面表征应用中使用接触角:前进角04-21 大昌华嘉
大昌华嘉科学仪器荣获Novasina 2025年度“成长与创新先锋奖”!04-21 大昌华嘉
