Microbiome | 16S+代谢组学助力中农科及青岛农大探究小肠粘膜炎病理机制发微生物一区顶刊
2022-04-19 00:34:04, 多层组学定制服务 上海欧易生物医学科技有限公司

前言
2020年8月欧易/鹿明生物合作客户中国农业科学院及青岛农业大学等实验团队在Microbiome发表的题为 “Microbiota from alginate oligosaccharidedosed mice successfully mitigated small intestinal mucositis ”的研究成果,通过LC-MS非靶向代谢组、16s微生物多样性、转录组等多种检测手段发现了海藻酸钠寡糖(AOS)通过增强细胞连接、恢复小肠功能以及改善可能有助于基因表达的转录因子来改善busulfan干扰的肠细胞膜;AOS改善血液代谢,以支持小肠功能的恢复。
中文标题:藻酸盐寡糖化小鼠的微生物群成功减轻了小肠粘膜炎
研究对象:小鼠
发表期刊:Microbiome
影响因子:14.650
发表时间:2020年8月
合作单位:中国农业科学院与青岛农业大学
运用欧易/鹿明生物技术:LC-MS非靶向代谢组学(由鹿明生物提供技术支持)、转录组、16S微生物多样性检测等;
研究背景
肠道粘膜炎症是用抗癌药物如白消安(busulfan)、5-氟尿嘧啶或FOLFOX化疗的副作用。由于胃肠道(GI)起着至关重要的作用,如:保护机体免受病原微生物的侵害,营养物质的消化/吸收、粘液和激素分泌等。
尽管已经提出了许多方法,如应用益生元、益生菌、硒、挥发油等来减少化疗引起的肠道粘膜炎,但进展甚微。海藻酸钠寡糖(AOS)是从海藻酸钠降解中得到的天然产物,含有聚甘露糖醛酸、聚古罗糖醛酸和杂合褐藻寡糖3种成分,被认为有抗氧化、抗炎症、抗细胞凋亡及增殖的作用。AOS通过增强细胞连接、恢复小肠功能以及改善可能有助于基因表达的转录因子来改善busulfan干扰的肠细胞膜;AOS改善血液代谢,以支持小肠功能的恢复。随后还发现,AOS可能通过增加“有益”肠道微生物和减少“有害”肠道微生物而有益于肠道微生物群。
据报道,肠道微生物群影响我们健康的许多方面,因为它提供营养和维生素,对抗病原体,维持上皮粘膜的内稳态,并支持人体免疫系统。它也被应用于许多疾病模型和临床试验中,治愈率非常高,副作用很少。FMT(粪便移植)已经被证明可以有效地控制肠道微生物群,改善化疗引起的粘膜炎。
研究思路
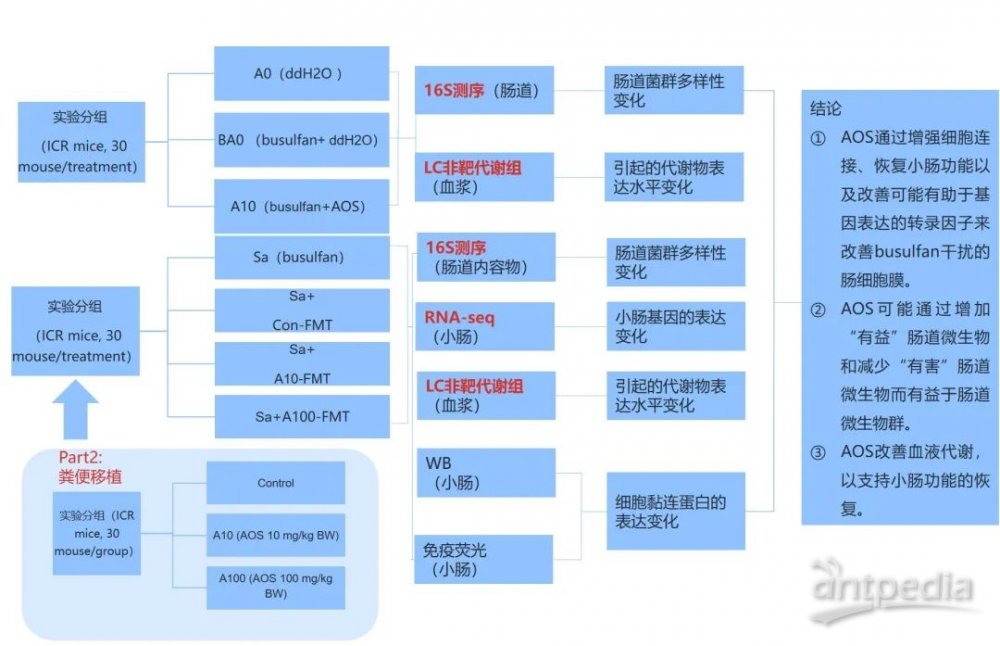
研究结果
1.AOS有益于肠道菌群
研究发现AOS减轻了抗癌药物busulfan诱导的小肠细胞膜的损伤,特别是细胞连接和微绒毛;同时,AOS支持血液代谢来帮助小肠恢复。这是因为肠道微生物群可以代谢营养物质,也可以调节肠道代谢物来影响血液代谢组分。
在本研究中,作者探讨了busulfan和/或AOS治疗后肠道菌群的变化,分为3组:(1)A0(ddH2O);(2)BA0(busulfan+ddH2O);(3) BA10(busulfan+AOS)。通过PCoA分析(PCoA;图1a)可以清楚地区分三种处理之间细菌组成的差异。在属水平上,BA10组中的乳酸杆菌的比例显著增加。LEfSe分析评估了这些处理之间不同菌属的差异,拟杆菌科在BA10中富集,表明AOS可以增加“有益”肠道微生物群(图1c,d)。
另一项研究表明,经过5周的AOS给药期后,AOS增加了“有益菌”,如拟杆菌、乳酸杆菌,而减少了“有害菌”如脱硫弧菌科。血液代谢物和肠道菌群之间有很好的相关性(图1e),将微生物分为两大类,代谢物分为三大类。结果表明AOS治疗有利于肠道菌群进而改善小肠功能。

图1 | AOS给药后小肠肠道菌群变化及菌群与代谢物的相关性分析
(a)不同处理条件下肠道菌群的PLS-DA分析;
(b)在门级水平上的菌群丰度差异;
(c和d)LEfSe和LDA分析;
(e)LEfSe和LDA分析;
2. A10-FMT/A100-FMT对小肠功能的改善更为显著
AOS有益于肠道微生物群进而改善busulfan引起的小肠功能损伤,该研究探讨了FMT对小肠功能的有益改善作用。分别从AOS(10 mg/kg或100 mg/kg)或ddH2O处理组中收集肠道微生物群(图2a)。同时,A10-FMT和A100-FMT通过增加Vil1的蛋白表达水平来恢复小肠功能(图2b)。
为探讨A10FMT/A100-FMT改善小肠功能的机制,采用RNA-seq分析对小鼠小肠进行基因表达谱分析。与Sa相比,Con-FMT中166个基因下调表达,308个基因上调表达;A10-FMT中179个基因下调表达,540个基因上调表达;A100-FMT中267个基因下调表达,572个基因上调表达(图2c)。这些差异表达基因的KEGG信号通路分析结果表明:在这三个比较(Sa vs Con FMT;Sa vs A10-FMT;Sa vs 与A100-FMT)中,最显著富集的信号通路是NOD-like receptor signaling pathway、antigen processing and presentation、cell adhesion molecules (CAMs),提示FMT可能有利于小鼠肠道的免疫功能(图2d-f)。
图2 | 小肠的转录组测序分析结果
(a)粪便移植的实验设计流程图;
(b)免疫荧光检测结果;
(c)不同比较组中的差异表达基因聚类结果;
(d-f)差异表达基因的pathway富集分析结果;
此外,多重富集分析(Metascape)结果表明,常见功能群与细胞防御有关(图3a,b),最特异的功能在Sa vs A10-FMT显著富集,包括能够帮助小肠功能恢复的细胞粘附分子、消化和吸收(图3a)。结果表明,A10-FMT对小肠功能的改善最为有利,即AOS 10mg/kg是改善小肠的最佳浓度。由于“CAM”在RNA-seq数据中富集,因此在小肠样本中测定了重要的细胞粘附分子的蛋白表达水平。重要细胞连接分子ZO1、Cx37、连环蛋白、E-cad(E-cadherin)和claudin的蛋白水平在Sa组最低,在Con-FMT中较高,在A10-FMT和A100-FMT中最高(图3c)。转录因子SOX4、GATA4和KLF7的蛋白质水平在Sa中最低,而在A100-FMT中最高(图3e)。同时,p-PTEN和Bcl-xl的蛋白水平表明,Sa和Con-FMT的凋亡水平较高,而A10-FMT和A100-FMT的凋亡水平较低(图3f)。结果表明:A10-FMT和A100-FMT比Con-FMT更有益于busulfan受损的小肠。

图3 | 多重富集分析及细胞黏连蛋白表达分析
(a)多重富集分析结果;
(b)Circos plots展示不同比较组之间的关联;
(c-f)细胞黏连蛋白的免疫荧光及WB结果;
3. A10-FMT/A100-FMT对肠道菌群的益处更大
通过16S rDNA来分析FMT通过肠道菌群改善小肠功能的作用。A10FMT和A100-FMT组的“有益菌”拟杆菌水平较高,而Sa和Con FMT组中“有害菌”厚壁菌的水平升高(图4b);“有害菌”Akkermancia只存在于Sa组。此外,A10-FMT和A100-FMT的拟杆菌/厚壁菌比率高于Sa或Con- FMT(图4c),这表明A10-FMT和A100-FMT对肠道微生物群的益处比Con-FMT更大。LEfSe分析进一步探讨四组之间菌群差异(图4d,e),Leuconostocaceae在A100-FMT中富集,表明A100-FMT增加了有益菌。FMT研究中的A10-FMT/Sa和AOS直接处理研究中的BA10/BA0的比率在“门”水平上显示出相似的趋势(图4f),这表明这两个研究中的微生物有很好的相关性。
图4 | FMT处理后肠道菌群的变化
(a)不同处理组中肠道菌群的PLS-DA分析;
(b)门水平上的菌群丰度差异;
(c) Bacteriodetes to Firmicutes比率在不同比较组中的分布统计;
(d-e)LDA和LEfSe分析;
(f)在门水平上不同菌群的不同组中的比率统计以分析其表达相关性;
4. A10-FMT/A100-FMT比Con-FMT更能恢复血液代谢
肠道微生物群在营养物质的消化和吸收中起着至关重要的作用,从而影响血液代谢,因此利用LC-MS非靶向代谢组学研究FMT对血液代谢的影响,并分析了血液代谢物与肠道菌群之间的相关性。Con-FMT、A10-FMT和A100-FMT显著改变血液代谢物,在Sa vs Con-FMT、Sa vs A10-FMT和Sa vs A100-FMT中,分别有131、132和129种代谢物发生显著变化(图5a-c)。值得注意的是,Sa vs A10-FMT和Sa vs A100-FMT的53个常见代谢物具有相似的趋势(图5j),这表明A10-FMT和A100-FMT可能以相同的方式影响血液代谢物。30个代谢物在control vs Sa, Sa vs A10-FMT, and Sa vs A100-FMT共有,其中15个代谢物被busulfan (in control vs. Sa)诱导显著增加,而A10-FMT和A100-FMT使其显著减少(Sa vs A10-FMT和Sa vs A100-FMT;图5k),表明,A10-FMT和A100-FMT对血液代谢组产生了显著改善。这30种代谢物中大部分是脂类分子,在小肠功能中起着重要作用,这表明A10-FMT/A100-FMT在血液中恢复了那些被busulfan扰乱的代谢物。

图5 | FMT处理后血浆代谢物的变化
(a-c)不同处理组中差异代谢物的聚类分析结果;
(d-f)不同处理组中的OPLS-DA分析;
(g-i)不同处理组中差异代谢物的相关性分析;
(j-k)不同处理组中共有代谢物的表达聚类分析;
显著变化代谢物的KEGG代谢通路分析表明:choline metabolism in cancer、glycerophospholipid metabolism、retrograde endocannabinoid signaling、linoleic acid metabolism、glycosylphosphatidylinositol (GPI) anchor biosynthesis这些通路在Sa vs Con-FMT、Sa vs A10-FMT和Sa vs A100-FMT共同富集(图6a-c)。fat digestion and absorption、cholesterol metabolism、carbohydrate digestion and absorption、vitamin digestion and absorption 在A100-FMT中特异性富集(图6a-c)。这些途径反映了A10-FMT和A100-FMT在改善小肠功能方面的优势。用Spearman相关系数分析血液代谢物与肠道菌群的相关性(图6d),结果表明:血液代谢物分为两组(上下);大部分代谢物在control vs Sa中增加,而A10-FMT和A100-FMT使其减少。菌群也被分成两大类(左和右),上簇中的代谢物与右簇中的微生物呈正相关,而下簇中的代谢物与左簇中的微生物正相关。Lactobacillales与上簇代谢产物呈正相关,这表明“有益菌”乳酸杆菌有助于血液代谢产物的恢复。同时,Mycoplasmatales与下簇代谢物呈正相关,这表明“有害菌”支原体不能协助血液代谢物的回收。提示A10-FMT和A100-FMT可改善小肠功能和肠道菌群,恢复血液代谢。

图6 | FMT处理后血浆代谢物的代谢通路分析及相关性分析
(a-c)不同处理组中差异代谢物的代谢通路分析;
(d)代谢物与肠道菌群的相关性分析;
研究结论
在目前的研究中,AOS-dosed的FMT通过调控基因表达和提高细胞连接蛋白来明显改善小肠。AOS-dosed的FMT通过增加“有益菌”Leuconostocaceae和促使血液代谢组学的恢复来发挥其肠道菌群的优势。FMT从一个具有优良微生物的供体诱导了小肠功能的恢复。表明AOS处理的肠道微生物群供体可用于预防化疗药物或其他因素在受体中引起的小肠粘膜炎。
小鹿推荐
本文通过LC-MS非靶向代谢组、16s微生物多样性、转录组等多种检测手段发现了海藻酸钠寡糖(AOS)是从海藻酸钠降解中得到的天然产物,AOS通过增强细胞连接、恢复小肠功能以及改善可能有助于基因表达的转录因子来改善busulfan干扰的肠细胞膜;AOS改善血液代谢,以支持小肠功能的恢复;AOS可能通过增加“有益”肠道微生物和减少“有害”肠道微生物而有益于肠道微生物群。AOS-dosed的FMT证明可以有效地控制肠道微生物群,改善化疗引起的粘膜炎。
.
文末看点|lumingbio
欧易/鹿明生物推出的16s+代谢组学的多层组学研究思路继本篇文章前已先后助力了浙江工业大学、中国农科院、青岛农业大学等在微生物一区顶刊Microbiome、医学一区顶刊GUT发表文章。
鹿明生物“组学发文快”豪礼促销16S微生物多样性+LC-MS+GC-MS 1100元/样~快点咨询当地工程师或者扫码咨询小鹿皆可得到快速回复~
详情请戳:
项目文章PBP | 浙江工业大学傅正伟运用GC-MS非靶向代谢组学和16S探究水稻根际微生物群落影响
项目文章 | 恭喜中国农科院及青岛农业大学团队继GUT后又喜发微生物顶刊Microbiome。
长按咨询16S+双平台代谢促销活动
扫码观看16S+代谢医口线上课
预告:4月12日,鹿明生物携手布鲁克·道尔顿带来“单细胞蛋白质组研讨暨新品发布会”,隆重推出鹿明生物基于4D蛋白组平台的单细胞蛋白质组技术服务,基于该技术可针对单细胞、微量单类群细胞、微量穿刺样本、激光显微切割及其他珍稀样本的研究提供强大的分析工具,带来极微量样本检测更高深更稳定更精准的分析结果。

猜你还想看
◆项目文章 | 恭喜青岛农大科学家多层组学文章喜登Gut
◆项目文章 | 运用16S+代谢组学揭示乳果糖缓解盐敏感型高血压的作用机制
◆Hepatology | 运用16S+靶向代谢组学可区分重度饮酒和酒精性肝炎患者
◆16S+代谢组学助力发文医学一区行业顶刊《Gastroenterology》
06-18 TESCAN中国
解决临床创新“卡脖子”难题,丹纳赫重磅推出医院创新转化解决方案!06-18
徕卡精准空间生物学解决方案 第三弹06-18 郑晓业、童昕
618 嗨购一起“徕” | 网上商城活动来袭!06-18 徕卡显微系统
【培训活动】显微镜成像高阶培训系列(一) 共聚焦多维度成像技术解决方案06-18 徕卡显微系统
【展会】第十五届中国医师协会骨科医师年会06-18 徕卡显微系统
【直播预告】第十届电子显微学网络会议06-18 徕卡显微系统
【案例研究】双视野光片显微镜,适用于类器官及胚胎06-18 徕卡显微系统
议程确定|第四届锂离子电池热测试主题研讨会06-18
文献解读|安徽理工大学马衍坤教授团队《煤炭学报》:震动载荷多次作用下烟煤孔裂隙结构演化特征试验研究06-18 纽迈分析
中国的新质生产力正在服务全球市场!GE医疗北京基地CT交付量达3.5万台/套06-17
兰格ACHEMA 2024展会回顾:探寻精密流体传输市场新机遇06-17
宝英科技推出VOCs治理设施精细化管理实施方案,助力重点行业企业绿色升级06-17 宝英科技
赛默飞X先锋“肽”势:多肽药物研发与创新研讨会06-17
一省检验检测行业营收突破160亿元!06-17
仪器租赁 | 沃特世 液质联用,月租金52000元起06-17
不同行业实验室“以旧换新”,涉及哪些仪器设备?06-17
目标!检验机构总营收超100亿!06-16
一张“A4纸”售价高达万元,这家第三方检测公司是怎么做到的?06-15
GLMY创想仪器丨参加东北地区铸造年会06-15 国产精密仪器厂家