器官芯片模型中血管生成的 3D 图像分析与表征
2020-12-13 14:23:15, 美谷分子仪器 美谷分子仪器(上海)有限公司


导言
血管生成是由预先存在的血管所形成和重塑的新血管及毛细血管的生理过程。这可以通过血管和毛细血管的内皮细胞出芽或分裂来实现。血管细胞通过降解细胞外基质对适当的刺激做出反应,随后诱导内皮细胞增殖和迁移 1,2。
细胞经历过这些过程后,形成一个包含腔的管,一个动态的空间,促进血液流动和氧、二氧化碳、一氧化氮和营养物质的交换。血管生成是生长发育、伤口愈合和肉芽组织形成的重要过程。血管生成生长也会支持肿瘤细胞在健康组织中的侵袭,在癌症研究中通常被量化监测。当血管芽向血管生成刺激源延伸时,内皮细胞利用黏附分子进行纵向迁移。这些芽随后形成环状,利用迁移至此的细胞形成一个完整的血管腔。出芽过程在体内以每天几毫米的速度进行着,并使新的血管能够跨越间隙生长。
许多抗血管生成药物已被开发于癌症治疗,而促血管生成分子则可能在再生应用中具有潜力。
迄今为止的体外实验仅模拟了血管生成机制的某些方面,包括划痕实验、博伊登室和管形成实验。


主要特点
• 可视化血管生成出芽和三维重构
• 对血管生成进行定量评估,包括芽的数量、总体积和平均荧光强度
• 使用 OrganoPlate® 芯片板获得与生理相关的数据
MIMETAS 的科学家开发了先进的、更具生理相关性的模型,其中包括在促 / 抑制 - 血管生成因子条件下,包埋进细胞外胶质基中主血管的实际生长和出芽。这些诱因既可以通过灌注泳道加入,也可以通过一个共培养装置由组织直接分泌出来。
高内涵成像可以进行可视化血管生长结构、三维重构,并能进行血管生成和新血管萌发相关的复杂分析。在这里,我们描述了一种可获得血管生成相关的多维量化结果的成像分析方法,以用于疾病表型和复合效应的比较研究。


方法

细胞模型
3D 血管生成模型是在 MIMETAS OrganoPlate 3-lane3,4 细胞芯片板上构建而成。OrganoPlate 3-lane 板是基于 384 孔板上设计而成的,每个微流控单元由 3x3 个孔组合而成,整板共 40 个单元 ( 图 1 )。

图 1 OrganoPlate 3-lane 芯片板示意图
每一个微流控单元包含了三个泳道。胶原 -I 细胞外基质(ECM)胶被填埋入中间的泳道内。被称为“ 相导 ”(phaseguides)的小型压力屏障将 ECM 凝胶定型,防止其流入邻近的灌注泳道。接着,将内皮细胞 ( 原代细胞系,iPSC 诱导 ) 种到灌注泳道上方,并附着于 ECM 胶上。灌注开始时将 OrganoPlate 放置在摇床上,当细胞增殖时,它们形成内皮微血管。在血管形成后,在母体内皮血管的另一侧的底部灌注泳道中加入一系列促血管生成因子。由此产生的血管生成的化合物梯度会诱导血管生成芽。血管新生芽培养 0-4 天,然后固定,并进行定量分析比对。可以在附录中找到三维血管生成模型的示意图。

成像
血管细胞和芽用 4% 甲醛固定,用抗 VE-cadherin 的一抗结合样本,再用二抗 Alexa488(绿色)进行染色标记。肌动蛋白丝用 ActinRed ™ ReadyProbes ™试剂(红色)染色,细胞核用 Hoechst(蓝色)染色。细胞用ImageXpress® Micro 共聚焦高内涵成像系统 (Molecular Devices) 进行成像。细胞图像使用共聚焦模式(60 µm pinhole 转盘),在 10x 或 20x 水镜下进行成像。20x 成像中,采集了 45-58 层的 z-stack 图层图像,每层 2-4µm 间距。对于 10x 物镜,采集了 15-25 层图层,每层4-6 µm 间距。细胞核用 DAPI 通道,血管生成的芽用 FITC 通道,分别在 100 ms 和 400 ms 曝光时间下采集图像。

图像分析
图像分析使用了 MetaXpress 高内涵成像分析软件中的 Custom Module Editor 客制化分析功能。细节在结果部分做了详细描述。简单来说,使用了 Neurite Outgrowth 模块对延伸的血管芽进行识别,使用 Count Nuclei 模块进行细胞核表征。然后用“ 最佳匹配连接 ”功能将物体在三维空间的 z 平面之间进行连接。二次分析则是在 Excel 软件中完成的。
使用 MetaXpress 软件中的 3D 自定义模块分析图像。分析方法的展示需要用到 Custom Module Editor (CME) 和3D 图像分析能力。自定义模块包含了几个步骤,首先用Neurite Outgrowth 模块识别出每张图中的血管芽,处于 3D 空间中不同 Z 层面的物体利用“ 最佳匹配连接 ”选项进行三维拼接。随后血管芽的数量,以及它们的体积和荧光强度值都能在分析中获得。
细胞核的计数是可选项,无论是每张图的总细胞核数量,还是每个芽的细胞核数量都可以被定量。在分析过程中使用的感兴趣区域图层只包括位于凝胶泳道内的物体,而不包括内皮细胞管通道内的物体。用这种方法可以只计算血管生成芽,而不计算上泳道的细胞。所开发出的自定义分析模块在 20x 和 10x 图像中都可以应用。或者,图像分析也可以在 2D 最大值投影图像上进行分析。
对于芽的长度评价,略有不同的是,在 CME 中使 用“Fibers”应用模块来进行分析 ( 未显示 )。


结果
时间依赖的血管生成过程模型在 OrganoPlate 3-lane 中进行建模。血管内皮细胞被种于上泳道中,三天左右形成血管。该模型包括内皮细胞在上层泳道或同时在上层和底层泳道中生成的血管,或者在中间的胶原蛋白胶质层(图 1)。底部泳道添加生长因子可以促进在胶原蛋白中生成血管新生芽,并能进行成像和分析(图 2)。

图 2 器官芯片板中血管生成芽的图像。培养 1 天和 4 天后形成的新生芽的最大投影图像。注意图像上部的管状血管细胞。血管新生芽从上管进入含有胶原蛋白的泳道,向含有生长因子的下线延伸。核染色 (Hoechst) 为蓝色,VE-cadherin 为绿色,肌动蛋白为红色。
如图22 所示,图像以 10x 或 20x 进行展示。使用一颗 20x 水镜成像时,可以看到细胞在固体基质中非常锐利和高分辨率的图像。用 10x 物镜成像虽然少了部分细节,但是拍摄速度会更快,因为每个孔只需要拍摄一个视野和更少的图层数量。更重要的是,感兴趣区域可以将原有血管和新生血管有效区分开来。血管新生芽的代表性图像如图 2 所示。

图 3 A. 成像原图及使用 CME 编辑后的图层。利用 Neurite Outgrowth 模块在每层 z-image 中识别出单个的芽和核,然后利用“ 最佳匹配连接 ”函数将每个图像中的对象进行三维连接。该分析能够识别芽的总数量,总体积,平均强度,以及核计数。B. 用 MetaXpress软件实现血管生成芽的三维可视化。C. 每幅图像中的对象通过“ 最佳匹配连接 ”功能进行三维连接。分离的芽和核显示为假色。D. 使用“Find Nuclei”模块对每幅图像中的细胞核进行识别,然后使用“connect by touching”选项对目标进行连接。
图 3 描述了使用“ 最佳匹配连接 ”功能进行图像分析的过程,包括平面分割和三维特征连接。
观察到芽的数量和体积随时间而增加,细胞或核的数量也在增加 ( 图 4-5 )。

图 4 随着时间的推移,器官芯片板内的血管新生萌发 (RFP- HUVECs)。从左至右,在底部泳道用血管生成混合物分别刺激 0、1、2、3、4 天,形成血管生成芽。样本染色为肌动蛋白 ( 红色 ) 和 VE-cadherin ( 绿色 )。用 Hoechst 染核。
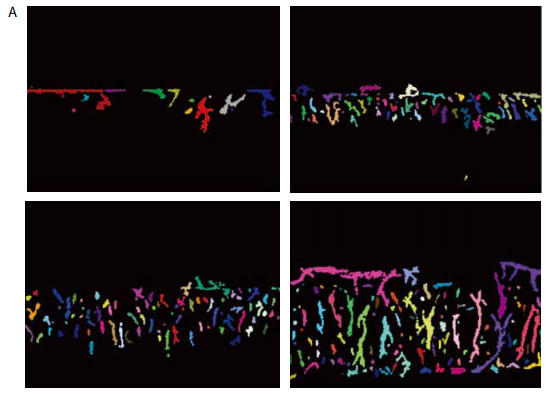

图 5 血管生成的定量评估。例如连续四天在 3D 胶原蛋白中的血管新生芽生长状况。柱状图显示了血管生成芽的定量测量。实验进行了三次,误差条代表 STDEV。
整块板的图像分析自动执行,无需用户干预。如果染色强度显著不同,可能需要在实验之间额外调整图像强度阈值。另外使用 Power Core 软件对分析也是必要的。
图 6 演示了自定义模块编辑(CME)用于分析的工作流程。

图 6 Customer Module Editor。展示自定义模块编辑器的分析步骤。


结论
从血管生成等复杂生物过程的表型变化中获得定量数据具有非常重要的意义。三维生物模型提供了一个更好的代表复杂人类生物学的方法,而复杂的三维结构的图像分析是具有挑战性的。
我们开发和优化了一套完整的成像和分析方案,能够在 MIMETAS 平台上进行血管生成芽的拍摄、可视化及定量分析。成像方案是基于 ImageXpress Micro 共聚焦系统和 MetaXpress 软件开发的,以提供成像和分析的集成式工作流程。将该系统与可扩展的器官芯片平台的功能相结合,为疾病建模和化合物筛选解锁新的表型效应的定量表征。


附录
Customer Module Editor
图像的 3D 分析使用了 MetaXpress 6.6 软件。为了在 3D 维度下定量分析出新生芽的数量,使用了 MetaXpress 软件中的 Customer Module Editor 进行客制化分析。简单来说,每一层图像中的 FITC 通道都使用了的高斯拟合进行展示。虽然血管芽通过 Neurite Outgrowth 识别分析模块进行对象分割。在拍摄过程中使用 Region Mask 工具 * 来创建中间胶质层区域,再利用“Keep Marked Objects”进行血管芽识别。因为“Keep Marked Objects”是一个基于对象选择的方式,选中区域在之外的对象也会被选中。
另外,也可以使用逻辑操作步骤“AND”进行区分,保留 Region Mask (Region Mask AND Neurite Outgrowth objective) 内的血管芽,而不使用“Keep Marked Objects”。最后,采用“ 最佳匹配连接 ”算法对各平面上的节点进行三维连接。可输出的测量值包括体积、直径和强度。为了提高分析速度,使用 MetaXpress® PowerCore ™ 高通量分布式图像分析软件对整个平板进行分析加速。
* 在图像获取期间使用自定义创建区域 journal 创建用户定义的区域,该区域仅包含微流控单元的中间凝胶泳道。该 journal 将定义的区域转换为用于下游分析的图像图层。
3D 血管生成模型的建模

OrganoPlate 3-lane 无膜血管新生芽的形成。A. OrganoPlate 板的底部,由 40 个微流控芯片组成。B. 每一个芯片由三个泳道组成:位于中间的凝胶层,以及左右两个相邻泳道。相导材料可防止成形的凝胶流入相邻两个泳道内。C. 血管生成芽的形成示意图。

参考文献
1. Birbrair A, Zhang T, Wang ZM, Messi ML, Mintz A, Delbono O (January 2015). “Pericytes at the intersection between tissue regeneration and pathology”. Clinical Science. 128 (2): 81–93. oi:10.1042/CS20140278. PMC 4200531. PMID 25236972.
2. Birbrair A, Zhang T, Wang ZM, Messi ML, Olson JD, Mintz A, Delbono O (July 2014). “Type-2 pericytes participate in normal and tumoral angiogenesis”. American Journal of Physiology. Cell Physiology. 307 (1): C25-38. doi:10.1152/ajpcell.00084.2014. PMC 4080181. PMID 24788248
3. van Duinen, V., Zhu, D., Ramakers, C. et al. Perfused 3D angiogenic sprouting in a high-throughput in vitro platform.Angiogenesis 22, 157–165 (2019).
4. Trietsch SJ et al (2013) Microfluidic titer plate for stratified 3D cell culture. Lab Chip 3(18):3548–3554.
*想要获取更多资料欢迎留言咨询

每周五下午 5 点与您相见
好玩的、划算的、有用的、前沿的
帮助您获取生命科学研究及药物研发全方位的解决方案
产品覆盖微孔板检测分析、高通量筛选、
高内涵成像、高效克隆筛选等。

我知道你在看哟

04-22 荧飒光学
吉艾姆4月双展齐发 | 武汉科仪展+脂在浙里研讨会04-22
应用笔记 | 基于Flex自动化平台的多体液胞外囊泡分离及EV蛋白质组学分析流程04-21 肖伟弟 曾嘉明
CCMT2026开展即高能 | Equator-X™ 双模式测量仪引爆全场04-21
告别预测偏差!Percepta自建专属训练库,pKa预测更准更快04-21 ACDLabs 李丹
世界地球日,查看地球的【愿望清单】04-21
【前沿激荡,智汇北京】IGC 2026圆满落幕,益世科生物共绘细胞基因治疗新蓝图04-21
会议预告|华大吉比爱邀您共赴第六届北京临床质谱论坛04-21 华大吉比爱
叮咚!您有一份来自地球的“绿色盲盒”待拆封04-21 安捷伦科技
聚焦小核酸与多肽前沿分析:第一届创新药物研发与质量评价技术交流会在沪圆满举办04-21 安捷伦科技
糖基化全流程质控:消耗品方案一站式解决04-21 安捷伦科技
药物分析排忧解难系列 | 自动柱前衍生化方案,完美应对样品复杂前处理04-21 安捷伦科技
“衣”路前行,“安”全守护 | 安捷伦 PFAS 解决方案守护运动健康04-21 安捷伦科技
零压力,低成本 | 安捷伦官方认证翻新仪器开启“以租代售”新模式04-21 安捷伦科技
ESCMID 2026 爆点 | MiSeq i100系列携6项病原精准测序应用数据亮相04-21
高效+精准,VA-5000 让实验室气体分析从此不同!04-21 HORIBA
突破制药检测瓶颈,欧美克NS-180Z系列纳米粒度及电位分析仪重磅登场04-21 欧美克仪器
NS-180Z Pro丨纳米粒度电位分析仪04-21 欧美克仪器
【每天学点粒度知识】动态光散射测量粒径应用案例04-21
还有人不知道吗?代谢组才是多组学联用的灵魂04-20