反相色谱肽分离系统研究第五部分:肽分析方法开发的筛选策略
2024-06-26 13:52:36, ACD/Labs阎作伟 Advanced Chemistry Development, Inc. (ACD/Labs)




阎作伟 编译
肽分析方法开发的
筛选策略
反相色谱肽分离系统研究第五部分

本文是反相色谱肽分离系统研究第五部分,编译者本以为系列文章已经结束,后经友情提示还有第五篇文章在2022年发表。本文介绍了一种简单快速的反相UHPLC方法开发筛选策略,用于肽类药物的纯度测定。该方案一共使用五种不同的色谱柱和六种挥发性或非挥发性流动相(即30种组合)进行筛选。该方法开发策略已被证明在识别产生互补选择性和提供良好峰形的条件方面非常有效。除了具有不同疏水特性外,还使用带不同电荷(正负)的色谱柱与pH值范围为2.3至5.1的流动相结合。pH 值为 2.3 的新型离子对/离液试剂六氟磷酸铵是一种非常有用的流动相添加剂,因为它具有出色的互补分离和良好的峰形。甲磺酸被证明是普遍使用的三氟乙酸的良好替代品,三氟乙酸未能对所研究的肽产生最佳分离,这凸显了筛选不同流动相添加剂的重要性。六氟磷酸铵和甲磺酸均未对C18色谱柱的稳定性产生不利影响,或表现出任何不可逆的吸附/记忆效应。在流动相pH循环中,任何固定相均未显示出pH滞后效应。新型流动相添加剂六氟磷酸铵和甲磺酸没有发现重大问题,但建议在确定长期常规使用之前谨慎使用。
预计后期还有第六篇文章,真是读者的福音。
一引言
为了最大限度地提高在复杂混合物中分离目标肽的概率,有必要选择具有互补色谱选择性的色谱柱和流动相。本系列文章的论文I和II描述了一种肽反相柱表征方案,该方案基于在pH 2.7和6.5色谱条件下下测定9种合成肽(即[Ile27]-牛胰高血糖素样肽-2 {[Ile27]-牛GLP-2}的片段)的8个选择性值。选择性值(delta值)有助于基于肽探针与固定相表面的疏水性、静电性、氢键和芳香族相互作用来区分色谱柱。然后,在论文III中扩展了该方案,通过主成分分析(PCA)的化学计量工具,根据其色谱选择性差异将43个不同的反相色谱柱表征为不同的子集。论文IV报告了新一代C18固定相(即Ascentis Express C18)上51种流动相组合(即pH 1.8 - 7.8、盐类型、离子强度、离子对试剂和离液/向液添加剂)的表征,然后扩展到其他反相材料。
基于之前的工作,作者选择了6种色谱柱和8种流动相组合物(包含挥发性和非挥发性缓冲液/添加剂),这些组合物在选择性和良好的峰形方面存在很大差异,可用于开发基于肽的药物的纯度方法,即样品由高水平存在的肽和低水平存在的许多相关肽杂质组成(通常为多肽原料药的0.05-1%)。对于这种类型的样品,重要的是具有高离子强度的流动相,以防止过载产生非常宽/不对称的主峰,从而导致紧临洗脱峰的遮蔽。药品的质量控制通常使用LC-UV,因此在本文的范围内包含非挥发性盐。
该研究评估了这些不同的色谱柱和流动相添加剂组合作为创新和快速梯度反相LC方法开发平台的一部分,以使用自动色谱柱和流动相切换技术分离肽杂质。使用人血管紧张素I (1 kDa)、牛GLP-2 (1–15) (2 kDa)、蜂毒肽(3 kDa)、牛胰岛素(6 kDa)及其相关杂质以及牛GLP-2 (1–15)及其四种非对映异构体的合成混合物,评估所选色谱柱和流动相添加剂的成功与否,这些非对映异构体对应于基础序列中单个氨基酸的外消旋化。使用评分系统评估每种样品的八种流动相添加剂和六种色谱柱组合的色谱性能,该系统基于主组分周围设定的保留窗口内分离的峰数和峰形。对排序顺序的评估有助于减少色谱柱和流动相添加剂组合物的数量,而这些添加剂组合物对于保持分离目标组分的高概率是必要的。
此外,作者还报告流动相添加剂(即甲酸/甲酸铵、乙酸/醋酸铵和六氟磷酸铵 [六氟磷酸钾])浓度的优化,以最大限度地减少噪声、漂移和腐蚀,同时保持良好的色谱峰形。使用加速储存条件评估了长期使用新型流动相添加剂(即甲磺酸和pH值为2.3的六氟磷酸钾)对C18色谱柱寿命和LC组分相容性(即柱筛板和金属LC管、聚四氟乙烯[Teflon]管和聚醚醚酮[PEEK]转子密封件)的影响。评估使用含有NaCl的低pH磷酸盐缓冲液代替硫酸铵,硫酸铵以前已经纠正了在用硫酸盐缓冲液分析某些肽时观察到的不良峰形。研究pH 2.3下甲磺酸和六氟磷酸钾对六个固定相的离子对记忆效应。还研究了6个不同色谱柱的pH滞后(即在pH 3→7→3之间循环)效应。将普遍使用的三氟乙酸(三氟乙酸)用于肽分离与本文评估的流动相分离结果进行了比较。在仔细考虑了所获得的选择性结果以及使用这些新型流动相添加剂的实际因素后,提了一种重新定义梯度反相方法的开发策略。
二实验
2.1. 化学品和固定相
水、乙腈(MeCN)和所有流动相添加剂(如表1所述)均为LC-MS或HPLC梯度级,由Sigma Aldrich(英国普尔)提供。二甲基亚砜(DMSO)由Fisher Scientific(英国赫默尔亨普斯特德)提供。牛胰岛素、人血管紧张素I和蜂毒肽由Sigma Aldrich(英国普尔)提供。由Apigenex(捷克共和国布拉格)提供的[lle27]-牛GLP-2肽全部单独溶解在DMSO/水(8:2 v/v)中,浓度为0.25 mg/mL。肽氨基酸序列、分子量和估计的pI见表2。将溶液储存在−20°C。论文I-IV中提供了肽反相色谱柱/流动相表征方案中使用的每种肽的碱基序列。

表1

表2
通过在37°C下分别将牛胰岛素和牛GLP-2(1-15)置于20mM氢氧化铵(pH 10.8,1mL / mg肽)18小时和41小时,降解(即杂质水平分别增加约24%和11%)。然后通过添加等体积的 20 mM 乙酸来中和溶液,最终浓度为 1 mg/mL。不使用时,样品储存在-20°C。血管紧张素I和蜂毒毒素按原样使用,因为两者都含有许多相关杂质,因此不需要强制降解。为简单起见,本文的后续部分省略了肽来源的生物体名称。表3中提供了每种固定相的简要说明。每种离子对试剂都使用新的色谱柱,以避免因离子对试剂的吸附而产生色谱柱记忆效应的可能性。

表3
2.2. 液相色谱和实验设置
如表1所述,为流动相A和B制备预混流动相。对于非挥发性流动相添加剂,流动相B由MeCN/水(8:2 v/v)组成,以防止任何沉淀问题。梯度标准化如下:60 min内5%至80%B,在梯度顶部等度保持3 min,然后在0.1 min和12 min重新平衡(相当于约10个色谱柱体积)中恢复到原始条件。柱温为45 °C,流速为0.3 mL/min,检测波长为215 nm(带宽8 nm),参考波长为360 nm(带宽100 nm),采样率为12.5 Hz。水峰保留时间值被用作死时间标记。采用可变进样体积产生约1.5 AU.%的主峰高度,面积比值定义为目标杂质峰的面积除以所有杂质的面积加上主组分的总和。
使用岛津Nexera X3 UHPLC系统(德国杜伊斯堡)进行液相色谱分离,该系统配备两个二元泵(LC-40AD)、脱气机(DGU40S)、带冷却功能的自动进样器(SIL-40)、柱式烘箱(CTO-40C)、二极管阵列检测器(SPD-M30A)、180 μL混合器、六位色谱柱切换阀和通信总线模块(CBM-40Lite)或Nexera-i LC-2040 HPLC系统。滞留体积分别为440μL和502μL。
2.3. 加速色谱柱稳定性研究
在80 °C下,将三根新的Ascentis Express C18(2.7 μm,150 × 2.1 mm)色谱柱暴露于0.5% v/v 三氟乙酸在MeCN/水(5:95,v/v)中,0.5% v/v 甲磺酸在MeCN/水(5:95,v/v)和100 mM 六氟磷酸铵在MeCN/磷酸盐缓冲液中pH 2.3(5:95,v/v)和100 mM 六氟磷酸钾的单独条件下。在 108 次进样过程中监测σ-cresol(1 μL 0.1 mg/mL 溶液在 MeOH/水 20:80 v/v)中的保留时间(15 分钟运行时间 x 108 次进样相当于约 5000 柱体积)。采用220 nm(带宽8 nm)的紫外检测,参考波长为360 nm(带宽100 nm)。
2.4. 腐蚀研究
2.4.1. LC筛板
316不锈钢筛板(直径1/4英寸×0.03英寸厚度,2μm孔径,VWR国际有限公司,英国雷丁)和钛筛板(直径3/8英寸×0.04英寸厚度,2μm孔径,Restek Thames,Buckinghamshire,UK)用水和EtOH洗涤,并暴露于各种流动相组合物(即,对应于流动相A和B)中7天(每1 mL流动相)。去除筛板,溶液在氮流的帮助下蒸发至干燥。将残留物溶解在 2% v/v 硝酸水溶液 (1 mL) 中,并进一步稀释,然后通过 ICP-MS(Agilent 7500a,Cheadle,Cheshire,UK)分析铁、钛、铬和镍。
2.4.2. LC管
316不锈钢(VWR International Ltd) 和 MP35NR 合金 (Waters A/S, Taastrup, Denmark) HPLC管(20 mm长,0.025''''外径x 0.007''''内径,事先用水和EtOH洗涤)暴露于流动相条件下,在60°C下连续搅拌30天;0.1% v/v 甲磺酸 水溶液、0.1% v/v 甲磺酸 MeCN / 水溶液 (8:2 v/v)、20 mM 六氟磷酸铵溶于磷酸盐缓冲液 pH 2.3 103 mM 总离子强度和 20 mM 六氟磷酸铵pH 2.3 溶于 1:1 v/v MeCN/磷酸盐缓冲液中。用水和EtOH洗涤管材,并在60°C下干燥,然后称重以评估体重减轻或增加和显微镜检查。
2.4.3. 聚四氟乙烯管
在将 10 升 0.1% v/v 甲磺酸 的 MeCN/水 (8:2 v/v)、0.1% v/v 甲磺酸 的 MeCN 溶液或 20 mM 六氟磷酸铵的 pH 值为 2.3 之前和之后,评估拉伸强度,用于以大约 0.5 mL/min 的速率将 HPLC 储液槽沉降片连接到泵头,持续 14 天。拉伸试验使用机电驱动的 50 kN Instron 机器(Instron,High Wycombe,UK)进行。
2.4.4. PEEK转子密封件
将PEEK转子密封件(Waters A/S,Taastrup,丹麦)暴露于0.1%v/v 甲磺酸的MeCN/水(8:2 v/v)、0.1% v/v 甲磺酸的MeCN或MeCN/水(8:2 v/v)的搅拌溶液中(室温下30天)。使用Duramin A300硬度计(Struers Inc,Cleveland,USA)进行硬度测量,该硬度计装有维氏压头,施加的载荷为1 kgf。
2.5. 软件和计算
岛津LabSolution软件(5.86版,德国杜伊斯堡)用于液相色谱仪控制和数据处理。主成分分析(PCA)使用SIMCA(版本14.1,Sartorius UK Ltd,Surrey,UK)和Origin(版本OriginPro 2017,OriginLab,Northampton,MA,USA)进行。使用通用蛋白质/质量分析Windows(GPMAW)软件(版本9.51,Lighthouse Data,Odense,Denmark)计算肽探针的净电荷。使用BufferMaker(版本1.1.0.0,ChemBuddy,BPP Marcin Borkowski,Poland)进行流动相计算。
三
结果与讨论
3.1. 色谱柱选择的基本原理
根据先前的结果,选择了6个选择性差异较大的色谱柱。固定相的负/正电荷特性取决于流动相pH值,是导致带电肽保留和选择性的主要因素,而配体官能团则不那么重要。先前已经证明,所选色谱柱在低pH值下表现出以下负电荷或正电荷/反相特性:Zorbax 300 SB-C18(非封端二氧化硅基)低负电荷/中等反相特性, Ascentis Express 联苯(封端二氧化硅基)低负电荷/中等反相特性, Acquity BEH C8(封端乙基桥式二氧化硅杂化技术)无电荷/中等反相特性, Acquity CSH 氟苯基(无封端、低水平正表面电荷、乙基桥接二氧化硅杂化技术) 低正电荷和负电荷(取决于流动相 pH 值)/低 反相特性, Luna Omega PS C18(二氧化硅表面少量正电荷) 低正电荷/高反相特性, Atlantis Premier BEH C18 AX(大量带正电荷的配体, 乙基桥接二氧化硅杂化技术)高正电荷/高反相特性。
3.2. 流动相选择的基本原理
选择pH值范围为3.6至7.0的20 mM离子强度挥发性流动相组合物,因为pH值是控制保留和选择性的主要操作参数。pH 值为 2.3 的离子对试剂甲磺酸和六氟磷酸铵(也是一种离液试剂)被纳入其中,因为它们已被证明表现出较大的选择性差异 。通过将六氟磷酸钾的水溶液在热空气流(300°C)中干燥10分钟,其中90%的理论固体被回收,证实了六氟磷酸钾的非挥发性。三氟乙酸被认为是肽分析的默认添加剂,因此被纳入对照。选择了pH 2.3和3.1的100 mM离子强度非挥发性磷酸盐基流动相,因为这些流动相已被证明可产生良好的峰形,并且是低紫外波长检测的首选流动相。
3.3. 流动相添加剂成分的优化
对流动相储层A和B中甲酸/甲酸铵pH 3.6和乙酸/乙酸铵pH 5.1的浓度进行优化,以产生平坦的基线,同时保持良好的峰形,从而提高信噪比,从而提高定量水平(LOQ)。在流动相A和B中,甲酸/甲酸铵pH 3.6的离子强度必须从20 mM降低到10 mM,以降低噪声,从而达到可接受的LOQ水平≤0.1%面积/面积和峰形(表1)。对于8:2 v/v MeCN/水(流动相B)中的三氟乙酸,将水(流动相A)中的含量从0.1% v/v降低到8:2 v/v MeCN/水中的0.09% v/v,以获得更平坦的基线。酸/碱的质量非常重要;建议使用HPLC梯度级组分和较短的流动相保质期。总离子强度为 100 mM 且非挥发性六氟磷酸铵为 20 mM,GLP-2 的拖尾因子最低,峰宽最窄 (1–15),参见补充材料 1。六氟磷酸铵的低水平被认为是有利的。
3.4. 色谱柱和流动相的初步筛选
起初,在所有六柱和八流动相组合上筛选降解的GLP-2(1-15)和胰岛素样品,以评估色谱柱/流动相组合的色谱选择性的多样性。此外,还评估了该方法开发策略分离 GLP-2 的四种非常相似的非对映异构体杂质 (1–15) 的能力(即,总共评估了 6 × 8 = 48 个组合 x 3 个样品 = 144 个色谱图)。通过对每张色谱图进行手动分级,确定每个样品的最佳流动相/色谱柱组合。对某一肽样品的每张色谱图进行1至5的排序,其中5表示最佳分离。排名标准基于高于一定水平(例如0.1%面积/面积)的杂质峰的数量。排名靠前的组合(即排名4和5)因主分量与相邻峰之间的峰值拖尾过多以及分离度差而受到惩罚,减去1个排名。GLP-2 的排名分类和标准示例见图 1 (1–15)。由于不同的肽样品表现出不同程度的降解、主峰和相邻峰之间的分离度以及主峰的不对称性,因此对不同样品使用的排名标准略有不同。每个肽样品的详细排名标准在补充材料 2 中进行了描述。
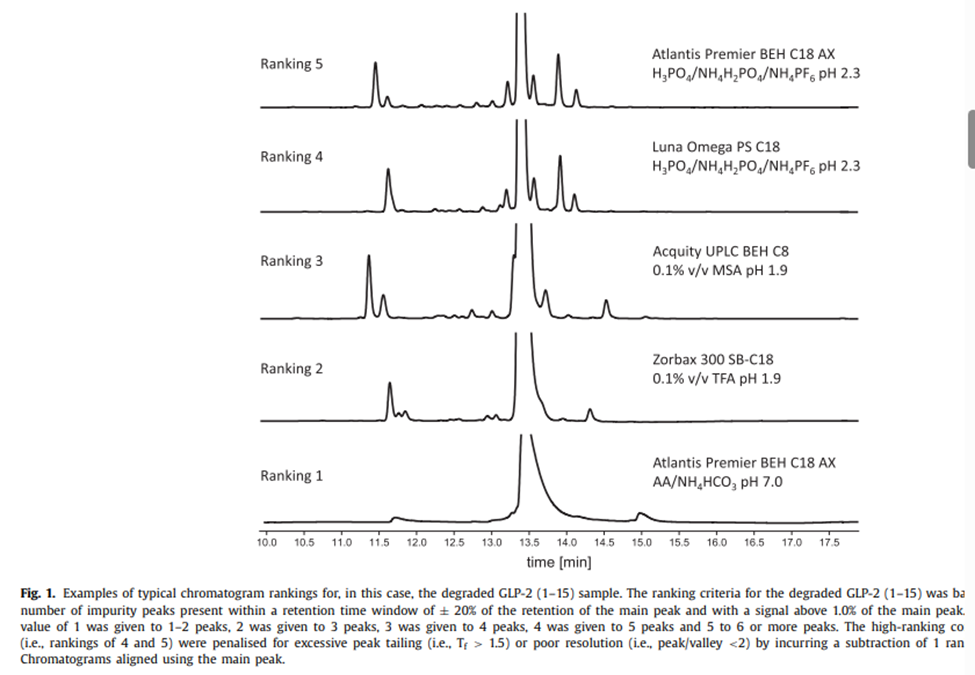
图1
然后进一步评估从初始筛选活动中减少的最有希望的色谱柱/流动相组合的数量,以分离人血管紧张素I和蜂毒肽及其相应的合成相关杂质。Ascentis Express 联苯和 Luna Omega PS C18 色谱柱以及 乙酸/碳酸铵pH 7.0 流动相由于在初始筛选中产生的排名较低,因此被排除在额外筛选之外。乙酸/碳酸铵pH 7.0流动相在诺和诺德的方法开发筛选中也产生了较低的成功率。观察到乙酸/碳酸铵pH 7.0流动相的pH值在室温下储存在部分盖好的烧瓶中时迅速增加,这是由于蒸发损失了二氧化碳(+0.9 pH单位/24小时,持续48小时)。因此,需要每天更换该流动相。在中等pH值下观察到较差的色谱性能是由于在该pH值下带负电荷的固定相表面导致与带正电荷的分析物产生不必要的二次静电相互作用。尽管由于潜在的腐蚀/材料不相容性问题,甲磺酸的性能与三氟乙酸相似,但甲磺酸也被排除在外(参见第3.9节)。然后,如上所述,对额外的48个色谱图(4个×6 = 24个组合×2个样品)重复排序。
图2总结了所有不同色谱柱/流动相/多肽组合的排名。Acquity BEH C8 和 Atlantis Premier BEH C18 AX 结合 0.1% 三氟乙酸的平均排名最高(即 3.8),可被视为良好的仿制药组合。然而,为了实现血管紧张素 I、GLP-2 (1-15) 和胰岛素样品的最佳性能和最大排名,还需要其他组合。

图2
3.4.1. 降解的GLP-2 (1–15)
评分排序工作表明,在所选色谱柱和流动相的组合下,色谱选择性具有高度的多样性。Acquity BEH C8色谱柱与H3PO4/NH4H2PO4/六氟磷酸铵pH 2.3、Atlantis Premier BEH C18 AX与H3PO4/NH4H2PO4/六氟磷酸铵pH 2.3或H3PO4/NH4H2PO4/NaCl pH 2.3相结合,根据所采用的 标准产生了最佳分离结果(即排名 5,见图 2 和图 3)(见补充材料 2)。结果表明,在pH 2.3的流动相中加入离子对/离液试剂六氟磷酸钾的分离效果有所改善。流行的离子 对添加剂0.1% 三氟乙酸pH 1.9在所有检查的色谱柱中仅产生2至3的排名,并且未能分离出靠近主峰洗脱的主要杂质,见图3。

图3
3.4.2. 降解的胰岛素
与GLP-2(1–15)结果类似,Acquity BEH C8色谱柱与H3PO4/NH4H2PO4/六氟磷酸铵pH 2.3或H3PO4/NH4H2PO4 pH 3.1相结合,可对降解的胰岛素样品进行最佳分离(见图2和补充材料3)。再一次,流行的流动相添加剂三氟乙酸未能分离出靠近主峰的丰富杂质洗脱。与其他肽样品相比,乙酸/碳酸铵pH 7.0流动相对胰岛素样品产生了相对较高的分离(见图2)。
3.4.3. GLP-2 (1–15) 和四种非对映异构体外消旋产物
降解的样品最好在低pH值下具有中性至高阳性特性的固定相上分离,无论是否使用离子对试剂。相比之下,GLP-2 (1–15) 的非对映异构体外消旋产物(即 [DHis 1]、[D-Asp 3]、[D-Ser 5] 和 [D-Ser 7] 异构体)(见表 2)的分离最好使用具有混合模式特性的固定相(即疏水配体和带正电或带负电的基团,具体取决于流动相 pH 值)。以下色谱柱/流动相组合的排名值较高,Atlantis Premier BEH C18 AX的pH值为0.1%,AA/NH4AA的Zorbax SB-C18的pH值为5.1,Acquity CSH氟苯基的FA/NH4FA的pH值为3.6,H3PO4/NH4H2PO4/NaCl的pH值为2.3,甲磺酸 pH值为0.1%(图2和图4)。

图4
后两个色谱柱不是封端的,因此具有显着的负面特征(即硅醇的可及性)。Acquity CSH氟苯基具有较低的表面阳性特性,但在较高pH值下具有较高的硅醇活性。Atlantic Premier BEH C18 AX 在 2 – 7 的 pH 值范围内具有高度的正电荷。不同的固定相和流动相组合产生不同的洗脱曲线,如图4所示。这再次凸显了筛选不同的固定相和流动相组合的必要性。
3.4.5. 蜂蛋白
由于该肽的高碱性(pH 2.3 和 5.1 时的总电荷分别为 +5.3 和 +5.0),与 甲酸/甲酸铵pH 3.6 和 乙酸/乙酸铵pH 5.1 相比,三氟乙酸的应用改善了峰形(见图 2 和补充材料 5)。Acquity BEH C8(中性)和Atlantis Premier BEH C18 AX(阳性特征)色谱柱与离子对试剂三氟乙酸相结合,获得了最高等级(即5)/最佳分离效果。流动相乙酸/乙酸铵pH 5.1导致所有色谱柱的峰形较差。这很可能是由于带正电的肽和固定相的部分解离的硅醇基团之间的二次静电相互作用。
3.5. 不同色谱柱和溶剂组合保留的比较
如图5所示,不同色谱柱和流动相组合之间的保留率差异相对较大。绘制不同色谱柱和流动相组合的GLP-2(1-15)、胰岛素、血管紧张素I和蜂毒肽相对于含三氟乙酸的Acquity BEH C8的平均保留率。大多数色谱柱和流动相组合的相对保留率在±20%以内。在 乙酸/碳酸铵pH 7.0 下,特别是与 Acquity CSH 氟苯基和 Ascentis Express 联苯色谱柱(-56 和 -47%)结合使用时,观察到的保留差异最大。这些信息对于色谱柱和流动相筛的设计非常重要。基于使用含三氟乙酸的Acquity BEH C8检测梯度的保留率,可以改变Acquity CSH氟苯基色谱柱上的筛选梯度,以实现足够的保留。
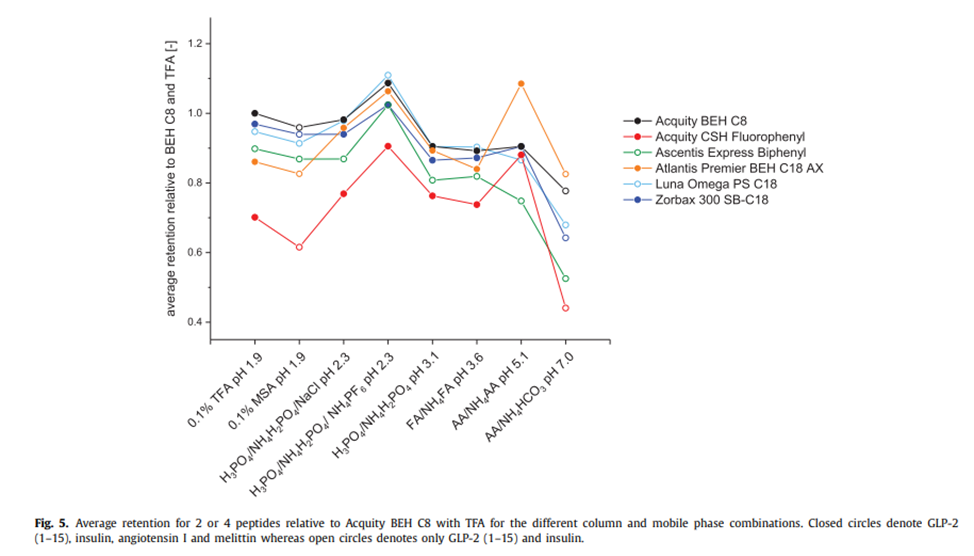
图5
3.6. 方法开发策略的基本原理
结果表明,只需五根色谱柱和六种流动相相结合,即可为分析人员提供足够的色谱选择性差异和可接受的峰形,从而产生分离所有目标组分的高概率。在大多数配备色谱柱和流动相切换阀的商用HPLC和UHPLC仪器上,可以很容易地评估这种设计空间(即流动相和固定相组合)。
3.6.1. 色谱柱
结果表明,疏水性和离子性(即正/负电离官能团)特性之间比例不同的有限色谱柱可提供足够的选择性差异,以最大限度地实现靠近主组分洗脱的杂质的分离。建议在方法开发策略中采用以下类别的色谱柱。
高正电荷/高反相特性
反相/阴离子交换混合模式相(即Atlantis Premier BEH C18 AX或等效物),除了其反相行为外,还具有显着的阴离子交换特性。
低正电荷/高反相特性
低带正电荷的表面 C18 柱(即 Luna Omega PS C18、Agilent Advance Bio Peptide Plus、Acquity CSH C18 带电表面 C18 或等效物),除了其 反相行为外,还具有低阴离子交换特性。
中性/中等反相特性
新一代C8或C18色谱柱(例如,Acquity BEH C8或C18或同等产品),具有极低的硅醇活性。随后表明,在研究的肽中,来自不同制造商的 C8 和 C18 材料之间的选择性/保留率差异很小。
低正电性、低负电性/低反相特性
带正电荷和带负电荷的色谱柱(即以 Acquity CSH 氟苯为典型)具有反相行为。表面正电荷和负电荷的程度由流动相pH值和非封端二氧化硅表面的电离决定。
低负电性/中等反相特性
具有显着硅醇活性的相,以 Zorbax 300 A° SB-C18 为典型,它是一种相对较宽的孔隙二氧化硅,与具有二异丁基保护基团的 C18 配体键合,该相不封端。据称,笨重的侧基会阻止分析物进入二氧化硅表面的电离硅醇基团,然而,在实践中,这并不总是被观察到。Zorbax 300 A° SB-C18相的Tanaka表征参数具有1.00的总硅醇活性(αB/P @ pH 7.6)值,而六个新一代C18相的平均值为0.26(范围0.18 – 0.32),表明Zorbax 300 A° SB-C18相具有显着的硅醇活性。
3.6.2. 流动相添加剂
研究结果表明,在pH值、离子强度和离子对特性方面变化的流动相范围有限,将赋予互补的选择性,并产生可接受的峰形。建议在方法开发策略中使用以下类别的流动相添加剂。
挥发性MS兼容流动相添加剂
选择了10 mM离子强度的甲酸/甲酸铵pH 3.6和20 mM离子强度的乙酸/乙酸铵pH 5.1,因为它们之前已被证明可以产生可接受的峰形并提供不同的选择性。
挥发性MS兼容流动相离子试剂
0.1% v/v 甲磺酸 和 三氟乙酸,然而,初步结果可能表明前者对 316 不锈钢的腐蚀性更强,这可能需要对某些 LC 组件进行修改以长期使用。此外,有间接证据表明,它也可能对LC中的PEEK组件有害。然而,本研究未观察到甲磺酸对PEEK转子密封件的任何影响。甲磺酸已成功用于液相色谱系统的常规使用,其中所有PEEK成分均已去除。一种假设是从PEEK中去除增塑剂,使其更容易受到旋转阀中纯粹力的磨损。作者建议在进一步的工作完成之前,对长期使用甲磺酸采取谨慎的态度,因为不同制造商的液相色谱系统之间接液部件的成分可能不同。由于甲磺酸显示出与三氟乙酸相似的结果,因此在确定长期使用甲磺酸的有效性之前,使用三氟乙酸被认为是明智的。然而,与三氟乙酸相比,甲磺酸具有某些优势,因为它在低波长梯度色谱过程中产生的UV基线漂移降低,梯度色谱中对大型混合器的要求较低,并且由于没有氟化,因此具有更好的环境认证。
非挥发性UV兼容流动相添加剂
100 mM离子强度H3PO 4 / NH4H2PO4 / NaCl pH 2.3和H3PO4 / NH4H2PO4 pH 3.1。尽管在当前研究中,pH 7的排名通常低于其他流动相,但它可能在选择性方面存在重要差异,因此值得纳入流动相筛选中。由于碳酸盐缓冲液的稳定性有限,最好使用 NH4H2PO4/(NH4)2HPO4 缓冲液。
非挥发性紫外兼容离子对试剂
在初始方法开发筛选方案中,建议使用 H3PO4/NH4H2PO4/六氟磷酸铵pH 2.3 来检测杂质。尽管作者未能观察到 pH 值为 2.3 的 六氟磷酸铵对液相色谱组分和色谱柱的任何不利影响,但建议应监测其使用,直到收集到足够的“实时”数据以证明它适合常规长期使用。
3.7. 建议的方法开发策略
3.7.1. 筛选柱和流动相条件
拟议的筛选策略包括评估六种MS和非MS兼容流动相容添加剂(不包括流动相2和8,见表1)与五种不同的色谱柱(不包括联苯色谱柱)。液相色谱条件的唯一区别是,对于非MS兼容的筛选,流动相B由8:2 MeCN/水组成,以防止缓冲液沉淀,而对于MS兼容筛选,流动相A和B相对于添加剂是匹配的。根据超过一定百分比面积/面积杂质水平的分离峰数、主峰周围的分离度和峰形来选择最佳色谱柱/流动相添加剂组合。如果观察到H3PO4/NH4H2PO4/NaCl pH 2.3是最佳流动相,则可能值得研究使用硫酸铵代替NaCl,因为它可以为某些肽提供略有不同的选择性或峰形改善。如果没有获得足够的分离度,可以进行筛选不同的有机改性剂,如异丙醇和MeOH代替/或与MeCN组合。由于粘度高,异丙醇通常与MeCN结合使用,例如20/60/20 v/v/v 异丙醇:MeCN:water。通过检查筛选色谱图,可以选择两种互补的液相色谱条件,这些条件可以构成二维LC-MS峰纯度分析的基础。这将在随后的论文中报告[D.R. Stoll, M.R. Euerby, S.M.C. Buckenmaier, P. Petersson, unpublished results]
3.7.2. 保留时间建模/优化、验证和耐用性测试
一旦选择了合适的色谱柱/流动相组合,就可以通过基于三次温度和三次梯度输入运行(即9次实验)生成梯度时间与温度保持模型来进一步优化该方法。生成一个综合模型(即对所有感兴趣的峰进行建模),这将有助于预测最佳条件。或者,生成一个简单的模型(即,仅对主成分加上第一个和最后一个峰进行建模)来识别提供可接受保留的条件。后一种方法的优点是不需要任何峰跟踪。然后可以随后对这些条件进行调查,以确定最佳条件。
优化方法的稳健性最初可以从保留模型中评估。例如,梯度斜率和温度的微小允许变化对分离标准的影响可以在计算机模拟中快速进行,为系统适用性调整提供图形(计算色谱图)和数值(δtR/δ%MeCN 和 δtR/δT)指导。如果该方法看起来是稳健的,则可以使用简化的因子设计和ICH指南通过实验确认该方法的验证。
3.8. 使用甲磺酸和六氟磷酸钾的色谱柱性能/寿命研究
在80 °C的高温和8.25 mm/sec的线性流速下,具有代表性的新一代反相色谱柱(即Ascentis Express C18色谱柱)暴露于甲磺酸和六氟磷酸钾(使用的典型浓度的五倍)时,与含有三氟乙酸的“金标准”流动相相比,其寿命更长。每项研究都使用了新的色谱柱。通过降低σ-cresol的保留因子(即,由于C18相/封端的损失而导致的疏水保留损失)作为通过色谱柱的流动相的柱体积数的函数来评估色谱柱的稳定性。在相同浓度下,0.5% v/v 甲磺酸 对 C18 相的侵蚀性略高于 三氟乙酸。观察到 pH 值为 2.3 的 100 mM 六氟磷酸铵对 C18 相的侵蚀性低于 0.5% v/v 三氟乙酸。因此,从色谱柱寿命的角度来看,0.1% v/v 甲磺酸和20 mM 六氟磷酸钾的固定相降解不应明显超过0.1% v/v 三氟乙酸(图6)。
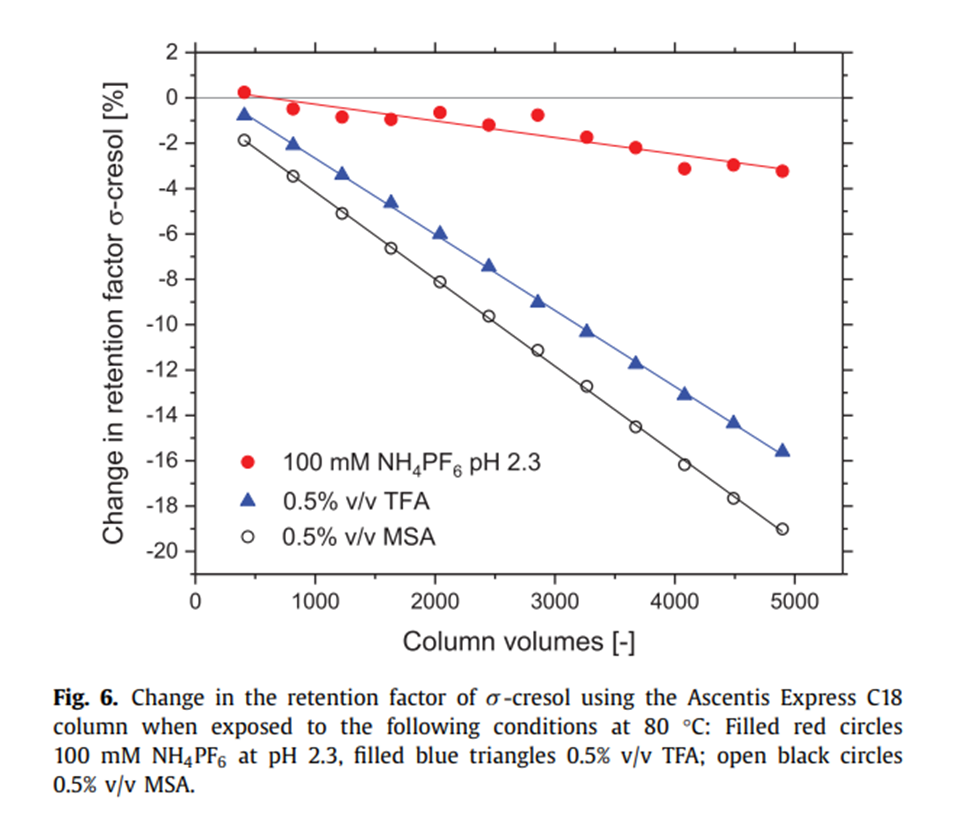
图6
3.9. 流动相添加剂长期暴露于“可润湿”液相色谱组分的评估
对所选流动相添加剂对常见“可湿性”液相色谱组分寿命的影响进行了初步研究。甲磺酸和六氟磷酸钾可能与某些LC组件不相容,因为前者先前已被证明会促进不锈钢的腐蚀,而后者在某些条件下会形成氟离子。
3.9.1. 316不锈钢和钛部件的潜在腐蚀
使用诱导耦合等离子体光谱(ICP)评估流动相添加剂(见表1)在加速储存(60°C,持续7天)时促进腐蚀(即从各种LC组分中提取金属)的倾向。柱状筛板被选为具有代表性的液相色谱组分,因为它们具有较大的表面积,添加剂可以与之接触,从而引起腐蚀。图7突出显示,唯一的潜在问题可能存在于80%MeCN/水和0.1% v/v 甲磺酸,而MeCN或水中的甲磺酸出人意料地未能引起这种效果。这些发现已经得到独立证实,并将在随后的论文中报告[J. Bischof,C. Smith,未发表的结果]。先前已经证明,在某些条件下,甲磺酸可能会促进不锈钢的腐蚀。所有其他添加剂的金属萃取水平与常规使用的流动相组合物相似,例如600 mM NaCl pH 2.4。所有类别中提取的主要金属是铁,其次是镍、铬,然后是锰。

图7
从筛板中提取的钛含量(<1200 ppb)远低于从不锈钢筛板中提取的金属(图7)。在pH 2.3下使用NaCl代替Na2SO4未能促进不锈钢筛板的腐蚀增加(通过HCl的形成 ),正如铁的提取所证明的那样,证实了其适用于LC流动相。将不锈钢316和MP35N合金(即镍-钴-铬-钼合金)HPLC管暴露在以动相条件下,在60 °C下连续搅拌30天;0.1% v/v 甲磺酸 水和 MeCN/水 (8:2 v/v)、20 mM 六氟磷酸铵溶于 pH 2.3 和 1:1 v/v MeCN/PO4 缓冲液中的溶液。在暴露于流动相添加剂之前和之后,没有观察到管路的显着重量差异或微观变化。
结果表明,氯化钠可以成功地代替硫酸铵,硫酸铵由于“盐析效应”而促进不良峰形。NaCl的腐蚀性已被证明与通常使用的流动相相当,并且它还具有比硫酸盐更易溶解的优点。
3.9.2. 甲磺酸和六氟磷酸钾在PEEK组件上的兼容性
PEEK转子密封件暴露于0.1% v/v 甲磺酸的水溶液或8:2 v/v MeCN/水溶液中(即在室温下30天,动态条件)对其硬度没有影响。在没有甲磺酸的情况下暴露于8:2 v / v MeCN /水时,也获得了类似的结果。
3.9.3. 甲磺酸 和 六氟磷酸铵在聚四氟乙烯组件上的相容性
众所周知,特氟龙的机械强度可能会受到某些化学物质的影响。然而,在暴露于10升0.1% v/v 甲磺酸在MeCN/水(8:2 v/v)和MeCN或20 mM NH4PF 6,pH 2.3,室温下14天并无明显变化
3.10. 与 三氟乙酸相比,甲磺酸和六氟磷酸铵对不同固定相化学的离子对记忆效应的评估
使用典型的洗涤条件(即20色谱柱体积的50:50 v / v MeCN /水),某些离子对试剂可能难以从反相固定相中去除,因为它们容易吸附在色谱柱上。这可能导致色谱柱在暴露于不同流动相条件后的选择性变化。通过评估肽反相色谱柱表征选择性值(即7个值,,使用流动相H3PO4/NH4H2PO4/NaCl pH 2.3)在色谱柱暴露于含有离子对试剂的流动相并洗涤色谱柱之前和之后,监测由离子对试剂的吸附引起的固定相表面化学变化。在所有情况下,甲磺酸、六氟磷酸钾和三氟乙酸在评估的六根色谱柱中的任何一根上均未观察到可检测到的记忆/吸附效应(即δ值±0.003)。
3.11. pH滞后效应
在低pH和中等pH之间循环后固定相“缓慢平衡”的现象是筛选方案中使用的色谱柱的不良特征[10]。为了评估为筛选方案选择的色谱柱是否存在这种现象,作者评估了肽反相色谱柱表征方案的选择性值(即七个值,使用流动相H3PO4/NH4H2PO4/NaCl pH 2.3)在pH循环之前和之后(pH 2.3 → pH 3.6→pH 7.0→pH 2.3)。在每种pH条件下,通过用20个柱体积的1:1 v / v MeCN /水冲洗色谱柱。未检测到任何色谱柱的“缓慢平衡”证据(即δ值±0.002),仅仅Luna PS C18和氟苯基相相关的选择性值(即δ值0.004),其变化非常小。
四结论
通过在自动方法开发筛选方案中筛选具有不同电荷/反相特征比的五根色谱柱,结合六种不同的流动相组成(pH 2.3至5.1),可以实现高概率分离肽杂质。在大多数配备柱和流动相开关阀的商用HPLC和UHPLC仪器上,可以很容易地评估筛选设计空间(即流动相和固定相组合)。使用非挥发性或挥发性添加剂,在低pH值下具有中性或高正电荷的C8或C18色谱柱上,最好分离胰岛素、GLP-2(1-15)和血管紧张素I杂质的降解产物。在pH 2.3下使用离子对/离液试剂,为两种降解样品提供了出色的分离和峰形。高碱性蜂毒肽样品表明需要离子对试剂,如三氟乙酸。
相反,观察到具有显著电负性(即硅醇可及性)的固定相,以 SB-C18 和 CSH 氟苯基相为代表,在较高 pH 值下分离了 GLP-2 的非对映异构体 (1–15)。六氟磷酸钾和甲磺酸等新型流动相添加剂的使用不会影响C18色谱柱的稳定性。所有流动相均与典型的液相色谱仪器材料(即316不锈钢和MP35N R、钛、PEEK和聚四氟乙烯)兼容。当它们暴露于 316 不锈钢和钛筛板时也是如此,然而,在 8:2 v/v MeCN / 水中,0.1% v/v 甲磺酸 导致在加速储存时提取出异常高水平的铁、镍和铬。目前正在对这一异常结果进行进一步调查。由于某些金属可能会对某些分析物的色谱性能产生不利影响,因此建议对此进行研究。如果这是一个值得关注的问题,则使用生物惰性液相色谱系统与二氧化硅或PEEK内衬色谱柱以及PEEK、钛或涂层不锈钢筛板相结合。
色谱柱上未观察到pH 2.3 → pH 7.0 → pH 2.3 之间的 pH 循环产生pH 滞后效应。离子对添加剂六氟磷酸钾、甲磺酸和三氟乙酸未能证明在用1:1 v / v MeCN /水洗涤后评估的反相柱上有任何记忆效应/吸附。虽然新型流动相添加剂六氟磷酸钾和甲磺酸尚未发现重大问题,但作者建议在确定其长期常规使用之前要谨慎。
提倡使用筛选一系列不同的流动相添加剂,并结合少量具有不同电荷/反相特性的固定相。最佳流动相/固定相组合将 取决于所研究肽的物理/化学性质。这些结论是基于有限数量的肽及其相应的杂质,但是,相信这些发现也适用于其他肽。常用的离子对添加剂三氟乙酸未能在所有研究的肽中产生最佳分离效果,这凸显了在方法开发筛选方案中评估其他流动相添加剂的必要性。
ACD/Labs CN
微信号|ACDLabsCN
07-01 英斯特朗
连载 | 药物一致性评价与粒度分析(三)07-01 欧美克仪器
【仪器百科】LS-909丨干湿二合一激光粒度分析仪07-01 欧美克仪器
标准物质解决方案 | PFASs(全氟及多氟化合物)06-29
第九期阿尔塔有约 | 环境专题【新污染物:PFAS】技术研讨会精彩回顾及提问解答06-29
“绿色技术范式”,分析化学未来发展方向——访中国分析测试协会副理事长、辽宁省分析科学研究院原院长刘成雁教授06-29 转载仪器信息网
华西医院-标准型数显脑立体定位仪、双通道体温维持仪、体式显微镜安装完成06-29 迈越生物
科鉴检测助力2家仪器企业获得首批产品可靠性认证证书06-28 科鉴检测
德国耶拿:锂电池生命周期分析解决方案06-28 德国耶拿
AI已来!生命科学本科教学如何紧跟技术浪潮06-28 Opentrons
盛瀚售后,五星级服务的秘诀是什么?06-28 SHINE
专为汽车制造商打造的柔性解决方案——实现制程控制06-28
西北工业大学-脑立体定位仪安装完成06-28 迈越生物
会议邀请 | 第九届海上检验医师论坛06-28
卓立要闻 | 创新发展ing…6月卓立“大事小情”速览06-28 光电行业都会关注
打造信任合作伙伴!2024年度卓立汉光客户满意度调查开启06-28 光电行业都会关注
如何挑选适用于三阶光学非线性的测量系统?Z扫描测量系统来助力!06-28 光电行业都会关注
招聘启事—中国科学院沈阳自动化研究所微纳光学测量表征技术课题组06-28 光电行业都会关注
谱育科技作为主要完成方 荣获2023年度国家科学技术进步一等奖和二等奖06-28 点击关注→
仪器原理丨顶空仪与吹扫捕集仪科普小知识06-28 天美色谱