除菌过滤指南解读课堂|(十)过滤系统灭菌的注意事项
2023-02-15 14:20:57, 刘秋琳 Merck工艺解决方案
跟着刘老师一起解读指南
(十)过滤系统灭菌的注意事项
“
《指南》中提及“使用前,除菌过滤器必须经过灭菌处理(如在线或离线蒸汽灭菌,辐射灭菌等)。”那么在采用上述各种方法灭菌时需要注意哪些问题呢?
”在线或离线蒸汽灭菌时,很多因素造成了过滤系统灭菌的复杂性,例如,塑料组分传热能力较差;滤器上存在的大量的微孔会造成“气体陷阱”;另外蒸汽穿透滤器的路径非常曲折;最后,达到灭菌温度时,过滤器材料可能出现不稳定的情况等。因此采用任何一种灭菌方法都要经过严格的过滤系统灭菌验证。
1.灭菌器灭菌
常见的灭菌器灭菌对滤器有如下几种包装情形:
无论选择哪种包装形式进行灭菌器灭菌, 应保证滤器有完整的屏障既能防止微生物污染又能使蒸汽穿透,从而对过滤器进行彻底灭菌。滤器的进口端和出口端都应能透气,这样在灭菌过程中的不同阶段就不会产生较大压差,使滤器损坏。灭菌过程必须要考虑滤器生产商提供的灭菌相关参数。温度过高可能导致过滤器上的高分子聚合物材质不稳定,并可能影响滤器的物理完整性或者增加可提取物水平。
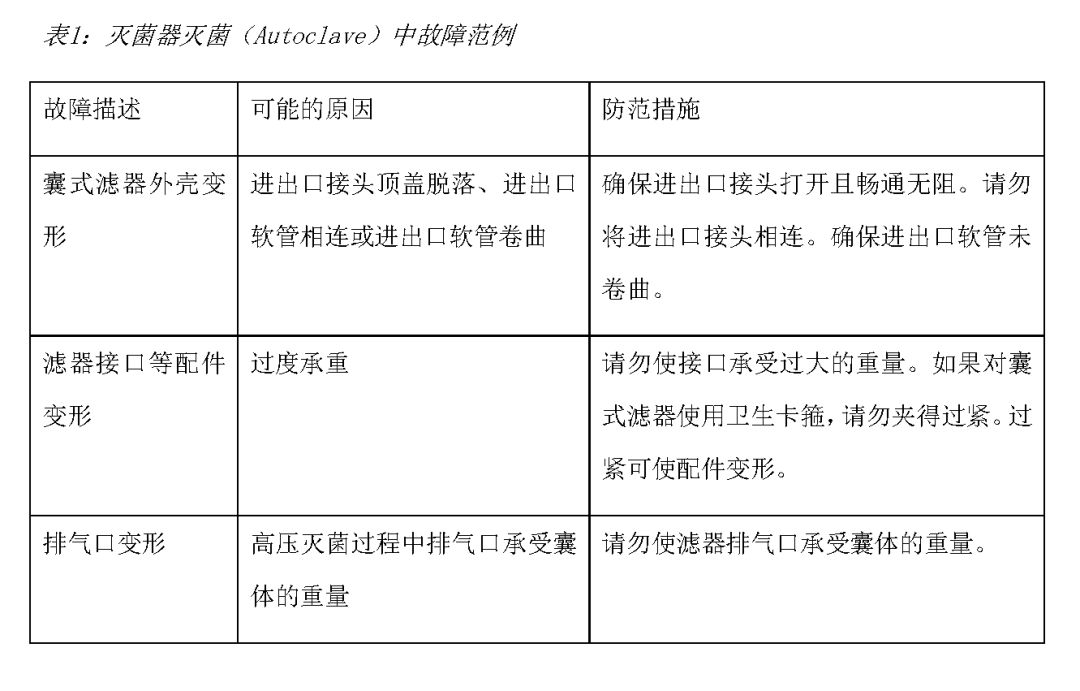
灭菌器灭菌常见问题故障排除
如果滤器发生损坏,按照如下表格以查明导致滤器损坏的可能原因。该表列举了在离线灭菌器灭菌(Autoclave)程序中可能遇到的一些问题的可能原因和解决方法。
2.在线蒸汽灭菌
在线蒸汽灭菌(SIP)是一种对安装在工艺管道中的过滤器、阀门、罐体等组件进行整体灭菌的一种方法。该方法易于重复且易于实现自动化操作,与灭菌器灭菌方法相比,减少了灭菌后各组件进行连接时可能存在的无菌风险,因此广泛地应用于无菌制药生产企业。
SIP 系统设计概述
图2为用于在线蒸汽灭菌的过滤系统装置的简图。该简图包括滤器、滤器壳体、阀门、压力表和/或温度表。
设计 SIP 系统时应注意以下内容:
(1)排气
理想的排气系统是蒸汽从系统高点进入,而空气从低点排出,如图2所示,因为空气(分子量为29g/mol)重于蒸汽(分子量为18g/mol),所以可自然下沉到低点。如果因实际情况不得不将蒸汽从低点引入系统,其流速也应足够将所有空气排出系统。如果系统中存在一端封闭的盲管(如压力表等),应尽量减短盲管长度至其直径的6倍以下,同时应安装排气口防止蒸汽灭菌过程中空气阻塞在这些部分。
(2)排除冷凝水
在蒸汽管线上每隔一定距离、阀门上游、通常关闭的阀门处、滤器套筒壳体的上游侧以及任何垂直管道的底部,都应安装排水阀或疏水阀,以便在升温过程中顺利排除冷凝水,以及防止系统冷却过程中对冷凝水的虹吸。水平管道应向下倾斜一定角度(如1:100),防止冷凝水积聚。如果系统的水平管道存在变径,则应保证变径前后底部管道处于同一水平线(如图3所示),以便冷凝水能够顺利排除而不存在“台阶”。
(3)热电偶放置
将热电偶放置在系统中加热最慢或最冷的点,通常为离蒸汽源最远的排放点。灭菌验证过程中,通过将热电偶完全覆盖整个系统来测定出系统在灭菌过程中温度最低的点。
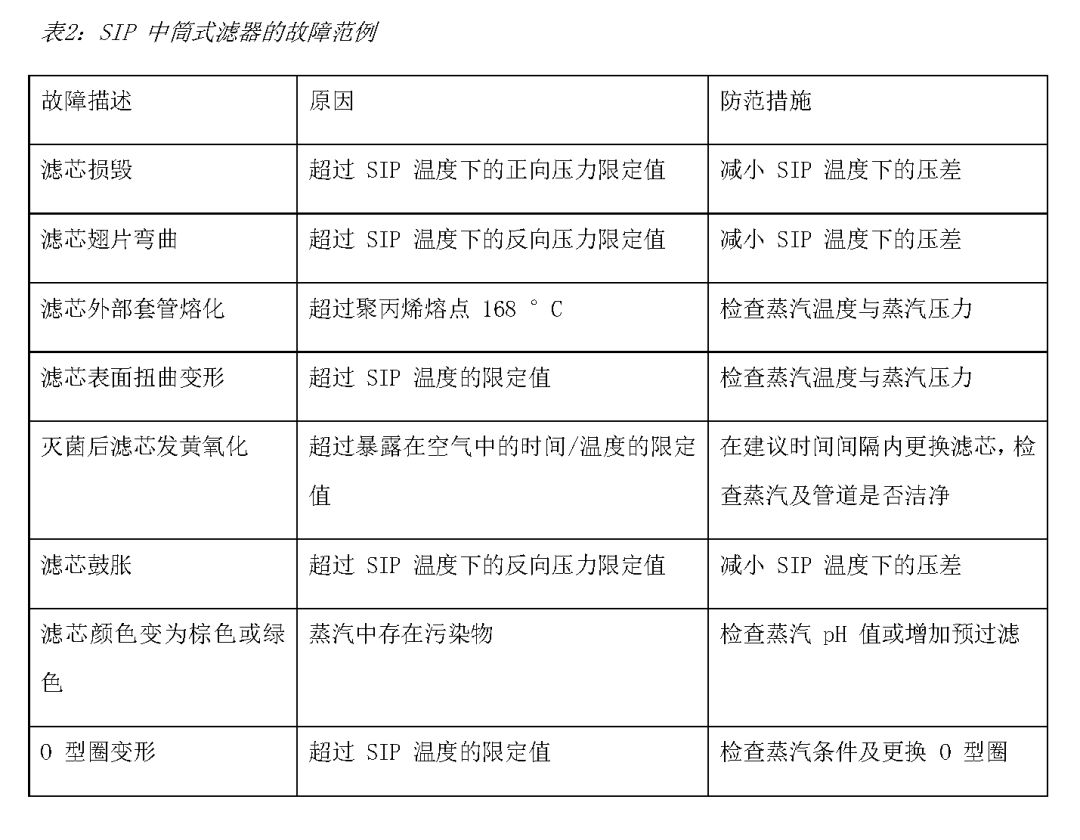
SIP 灭菌常见问题及故障排除
SIP灭菌经常出现的问题是造成滤芯损坏,如下图4示例:
如果滤器发生损坏,检查下表2以查明导致损坏的可能原因。该表列举了在 SIP 灭菌过程中一些问题的可能原因和解决方法。
3.辐照灭菌
对于除菌过滤应用会用到一次性使用的袋子、软管及所连接的滤器等,可采用辐照灭菌的方式,通常的辐照灭菌工艺采用伽玛射线和电子束灭菌。采用辐照灭菌法灭菌的无菌物品其SAL应<10^6。射线辐照灭菌所控制的参数主要是辐照剂量(指灭菌物品的吸收剂量)。该剂量的制定应考虑灭菌物品的适应性及可能污染的微生物最大数量及最强抗照射力,事先应验证所使用的剂量不影响被灭菌物品的安全性、有效性及稳定性。
辐照灭菌有众多优势,如较高的无菌保证等级,无残留气体或化学的灭菌组分,过滤器保持干燥,减小了包装组份对灭菌过程的干扰等。然而,这种方法也存在一些不足:如一些高分子聚合物材料中的某些组分不适合辐照灭菌,灭菌后的过滤器有效期有限等。已被辐照灭菌过的过滤器、袋子及软管等,由于累积剂量效应的缘故,通常不会采用多次伽马射线灭菌。
往期回顾:
除菌过滤指南解读课堂|《除菌过滤技术及应用指南》发布
除菌过滤指南解读课堂|(一)如何在过滤工艺开发时进行过滤系统的选择和设计?
除菌过滤指南解读课堂|(二)对过滤器供应商进行管理时要注意哪些要素?
除菌过滤指南解读课堂|(三)两个除菌过滤器串联就是冗余过滤吗?
除菌过滤指南解读课堂|(四)过滤器的性能确认可以替代过滤工艺验证吗?
除菌过滤指南解读课堂|(五)什么是验证主计划?
除菌过滤指南解读课堂|(六)什么时候应当进行除菌过滤工艺验证?
除菌过滤指南解读课堂|(七)除菌过滤工艺验证分项解析
除菌过滤指南解读课堂|(八)什么情况下需要进行过滤工艺再验证?
除菌过滤指南解读课堂|(九)如果进行过滤器的变更应当做哪些评估?
下期预告:
什么时候进行完整性测试?完整性测试失败了怎么办?
*更多产品信息,请咨询默克当地销售
*技术咨询:021-61433900
关于默克工艺解决方案
默克工艺解决方案是默克生命科学三大事业部之一,致力于为生物制药、化学制药企业提供产品开发、商业化生产所需全系列工具,已成为预过滤、无菌过滤、除病毒过滤、超滤、层析纯化、一次性生产、培养基、生物反应器、缓冲液、药用原辅料、工程技术及验证领域的全球领导者。默克工艺解决方案的成功源于对高质量产品、先进监管技术的不懈追求以及致力于帮助客户实现其需求的精神。
默克工艺解决方案领英官方账号已上线,
07-01 英斯特朗
连载 | 药物一致性评价与粒度分析(三)07-01 欧美克仪器
【仪器百科】LS-909丨干湿二合一激光粒度分析仪07-01 欧美克仪器
标准物质解决方案 | PFASs(全氟及多氟化合物)06-29
第九期阿尔塔有约 | 环境专题【新污染物:PFAS】技术研讨会精彩回顾及提问解答06-29
“绿色技术范式”,分析化学未来发展方向——访中国分析测试协会副理事长、辽宁省分析科学研究院原院长刘成雁教授06-29 转载仪器信息网
华西医院-标准型数显脑立体定位仪、双通道体温维持仪、体式显微镜安装完成06-29 迈越生物
科鉴检测助力2家仪器企业获得首批产品可靠性认证证书06-28 科鉴检测
德国耶拿:锂电池生命周期分析解决方案06-28 德国耶拿
AI已来!生命科学本科教学如何紧跟技术浪潮06-28 Opentrons
盛瀚售后,五星级服务的秘诀是什么?06-28 SHINE
专为汽车制造商打造的柔性解决方案——实现制程控制06-28
西北工业大学-脑立体定位仪安装完成06-28 迈越生物
会议邀请 | 第九届海上检验医师论坛06-28
卓立要闻 | 创新发展ing…6月卓立“大事小情”速览06-28 光电行业都会关注
打造信任合作伙伴!2024年度卓立汉光客户满意度调查开启06-28 光电行业都会关注
如何挑选适用于三阶光学非线性的测量系统?Z扫描测量系统来助力!06-28 光电行业都会关注
招聘启事—中国科学院沈阳自动化研究所微纳光学测量表征技术课题组06-28 光电行业都会关注
谱育科技作为主要完成方 荣获2023年度国家科学技术进步一等奖和二等奖06-28 点击关注→
仪器原理丨顶空仪与吹扫捕集仪科普小知识06-28 天美色谱