知名药企对高度唾液酸化双抗样本的icIEF检测方法优化
2022-12-09 01:25:35, ProteinSimple ProteinSimple
双特异性抗体的诞生
1960年,在一篇Science论文中,纽约罗斯威尔公园纪念研究所的Nisonoff及其合作者首次提出了双特异性抗体(Bispecific Antibodys)的原始概念。[1]之后,随着抗体工程和抗体生物学领域的里程碑进展,构建双特异性抗体的概念和技术不断创新(图1),导致了今天所看到的100多种双特异性抗体建造模式(formats),其中,约四分之一已发展成技术平台,并由生物技术公司和制药公司商业化,用于生产新型疗法。

图1(来自网络)
截至目前,已有20多个不同的商业化技术平台可用于双特异性抗体的开发,超过85个双特异性抗体处于临床开发阶段。
双抗研发需要检测电荷异质性
与单抗类似,双抗通常由修饰的重链和轻链组成,通过链内和链间二硫键共价组装成对称或不对称的Y形结构。[1]基于复杂的生化结构以及生产工艺,双抗的生产和储存过程中,也可能产生大量的修饰和降解,如氧化脱酰胺、糖基化、二硫键修饰、序列变异等。因此,抗体药物电荷异质性检测是整个生产工艺的关键质量属性(CQA)。
图2
Maurice采用的全柱成像毛细管等电聚焦(icIEF)是电荷变异体检测的金标准,已录入新版中国药典。icIEF方法除了高分离效率外,分离运行时间短,样品处理量高的特点在原料药和制剂开发中显著缩短了工艺优化和包装材料相容性等研发时间。
高度唾液酸化修饰给icIEF检测
带来难度
由于肝细胞高表达的去唾液酸糖蛋白受体可防止对抗体的识别,增加蛋白质的唾液酸修饰可维持药物进入血液循环,进而降低注射或治疗性蛋白的临床给药频率。百时美施贵宝(BMS)研究人员的bsAb-1就是这一类高度唾液酸化的双特异性抗体。
但对这一类高度异质性修饰的蛋白样本,他们发现通过icIEF方法的分析也会有一些困难。因此,研究人员报道了首次采用酶促脱唾液酸化的方法(加入神经氨酸酶)来改善使用icIEF方法对该双特异性抗体的分析检测。[3]
酶促脱唾液酸化优化了检测方法
研究人员首先优化了蛋白质样品缓冲液(MM)中的pI marker、尿素和L-精氨酸这3种成分浓度。
①图2A显示尿素浓度对bsAb-1的icIEF分离的影响; 尿素从上到下的浓度为3M、2.5M和2M。从谱图上看,最终尿素的浓度为2.5M时,达到了最佳的分离效果。
②图2B显示精氨酸浓度对bsAb-1的icIEF分离的影响; L-精氨酸(Arg)浓度自上而下:0 mM,2.5 mM,5 mM。
③表1显示的是经研究人员优化后的样品缓冲液配比。
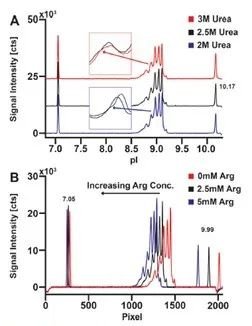
图2

表1
优化L-精氨酸和尿素浓度属于常规的方法优化,但酶法脱唾液酸化需考虑其他因素,例如在此过程中的关键问题是样本脱唾液酸化是否完全。
①图3A显示了不同孵育时间后不同电荷变异体的剩余百分比。实际上,在37°C下30分钟后样本已完成脱唾液酸化,这导致酸性物质相对减少,碱性物质相应增加。同时生成的电荷异变体水平在孵育长达24小时期间都保持稳定。
②图3B说明了采用优化后的缓冲溶液配比,经酶处理后的icIEF电荷变异体的图谱,并与未酶化的样品进行了比较。

图3
方法鉴定
参照预先定义的内部标准,研究人员统计了该方法的线性回归、重复性和LOQ的结果。结果显示该方法符合内部标准,可以用于针对bsAb-1抗体在0.1–1 mg/ml浓度下的电荷变异体检测。表2展示了线性回归的结果,样本采用0.1, 0.25, 0.4, 0.55, 0.7, 0.85以及1 mg/ml的阶梯浓度。R2的数值达到了接受标准,即需要主峰>0.98以及酸峰和碱峰>0.95。
表2
表3展示了标准差的结果。在做6次重复的情况下,酸峰的RSD% 为1.8、碱峰3.0、主峰7.8、均满足了接受标准。研究人员测得LOQ 为 0.1 mg/ml, LOD为0.05 mg/ml。

表3
参考文献
[1] Labrijn A F , Janmaat M L , Reichert J M , et al. Bispecific antibodies: a mechanistic review of the pipeline[J]. Nature Reviews Drug Discovery, 2019, 18(8):1-24.
Janmaat M L , Reichert J M , et al. Bispecific antibodies: a mechanistic review of the pipeline[J]. Nature Reviews Drug Discovery, 2019, 18(8):1-24.
[2] Peters B , Bautista J , Slaney T R , et al. Enzymatic removal of sialic acid enables iCIEF stability monitoring of charge variants of a highly sialylated bispecific antibody[J]. Electrophoresis: The Official Journal of the International Electrophoresis Society, 2022(9/10):43.
谢谢阅读
关于我们
ProteinSimple是美国纳斯达克上市公司Bio-Techne集团(NASDAQ:TECH)旗下行业领先的蛋白质分析品牌。我们致力于研发和生产更精准、更快速、更灵敏的创新性蛋白质分析工具,包括蛋白质电荷表征、蛋白质纯度分析、蛋白质翻译后修饰定量检测、蛋白质免疫实验如Western和ELISA定量检测蛋白质表达等技术,帮助疫苗研发、生物制药、细胞治疗、基因治疗、生物医学和生命科学等领域科学家解决蛋白质分析问题,深度解析蛋白质和疾病相互关系。
联系我们
地址:上海市长宁路1193号来福士广场3幢1901室
电话:021-60276091
热线:4000-863-973
邮箱:PS-Marketing.CN@bio-techne.com
网址:www.bio-techne.com
06-06 Unimicro
Nature 发文! 如果有一天,线粒体也能被移植……06-06 小 M
实验操作 | 小白第一课!基础细胞培养方法及步骤06-06 小 M
科研助攻 | Nature Review:癌症治疗抗体药物最新综述06-06 小 M
端午礼遇 | 玩游戏,选周边,宠粉福利,只 "粽" 意 你~06-06 小 M
发货通知 | MCE 中国祝大家端午安康06-06 小 M
“岛津森林”项目06-05 医疗中心
浙江以检测赋能新质生产力06-05
2025版《中国药典》收官在即,变化要点有哪些?要注意哪些方面?06-05
吸附管采集固定污染源废气中的VOCs时的采样流量要求?06-05 检测家
内卷加剧,检测机构如何破局应对?06-05
【人民日报国际】在收获与播种交织的芒种中国时刻,张轶昊谈创新。06-05
德国元素耗材之星 | 固体压样器/液体封样器06-05
夏日焕新 谱写新章 | 德米特第四届“互动日”惊喜而至06-05
祝贺嫦娥六号月背采样成功 | 盘点标乐助力月球样品分析06-05
2024年德国元素巡检活动 | 第一站:成都站!免费申请06-04
会议通知|第一届小动物活体成像技术前沿与应用网络研讨会06-04
蛋白质组学从发现组学跃入临床怀抱的跨越之旅06-04
内毒素检测的思考 - 采用药典方法同时减少鲎试剂的使用06-04 Sievers分析仪
检测家十周年特惠 | 赛默飞、岛津、沃特世 系列产品租六送一!06-04