红树植物榄李中新型鞣花酸内酯Lumnitzeralactone的结构破译
2025-12-09 15:04:13, CHEMICO Advanced Chemistry Development, Inc. (ACD/Labs)


从印度尼西亚红树林植物榄李(Lumnitzera racemosa Willd.)的抗菌活性提取物中,分离获得一种新型鞣花酸衍生物类天然产物lumnitzeralactone (1)。该化合物具有质子缺陷型结构及高度复杂的稠合芳香环体系。
通过综合波谱分析技术,包括高分辨质谱(HRMS)、一维1H/13C核磁共振(NMR)及二维NMR实验(含1,1-ADEQUATE与1,n-ADEQUATE),结合计算机辅助结构解析(基于ACD/Structure Elucidator的CASE系统)、密度泛函理论(DFT)计算以及两步化学合成实验,明确了其化学结构。
研究进一步提出了该化合物可能通过红树林共生真菌参与的生物合成途径生成。
红树林植物是一类耐盐的木本植物,广泛分布于热带和亚热带海岸线1,2。它们与微生物、真菌、其他动植物共同构成红树林群落(mangal)2。目前公认的真正红树林物种约有75种,分属11科3–5。榄李(Lumnitzera racemosa Willd.)属于主要分布于(亚)热带地区的使君子科(Combretaceae),其分布范围从东非海岸延伸至印度-西太平洋地区6及马来群岛2。
该植物在传统医学中应用广泛,常用于治疗:
蛇咬伤
风湿病
皮肤过敏
哮喘
糖尿病
作为血液净化剂使用2,7–10
其嫩枝汁液与老树皮汁可用于治疗真菌感染引起的皮肤病、疱疹、瘙痒和鹅口疮6,11–13。
研究表明,榄李提取物及其成分具有多种生物活性,包括:
抗菌6,14–16
抗凝血17
抗炎18
抗癌17,19,20
抗血管生成18
抗氧化17,20
保肝21,22
降压23
降血糖24
抗病毒作用16,25–27
其提取物中报道的主要次生代谢产物包括:
鞣质17,20,23
黄酮10,17,18,20,22
酚类17,18,20,21
生物碱21
萜类6,17,20,21
没食子酸及其衍生物(如可溶性鞣质、鞣花酸及其衍生物3,3′,4-三-O-甲基鞣花酸)被证实是其主要活性成分之一1,6,8,18,22,这类成分在使君子科及榄李中普遍存在。近期研究发现,三萜酸是使君子科中具有抗菌活性的成分28,其抗金黄色葡萄球菌作用可能与表儿茶素的协同效应有关28。
值得注意的是,红树林植物的活性成分并非全部来源于植物自身,许多成分由共生微生物(包括多种内生真菌)产生6,29–31。尽管同种真菌可能存在于不同宿主植物,但同种红树林的不同个体未必携带相同的微生物群落32,33。微生物多样性差异可能受物种组成、环境条件(如降水量、潮汐淹没频率、盐度、淡水流量、土壤类型和日照时长)影响,且宿主特异性并不严格32。
在近期一项代谢组学研究中,我们系统分析了榄李根部提取物中鞣花酸衍生物的组成特征8。本研究在此基础上,首次从榄李中分离、解析并化学合成了新型鞣花酸衍生物lumnitzeralactone (1),并对其抗菌活性及可能由真菌参与的生物合成途径进行了探讨。
在先前对印度尼西亚红树林植物榄李(L. racemosa)和滨海榄李(L. littorea)共31份风干根部样本提取物进行的LC-MS分析中,我们鉴定并分离出一系列结构新颖的硫酸化天然产物及非典型鞣花酸(EA)衍生物8。不同产地样本提取物的抗菌活性差异显著。
值得注意的是,仅有两份来自地理位置相近(马鲁古群岛的德那第与哈马黑拉岛)的提取物在500 µg/mL浓度下可完全抑制革兰氏阳性菌枯草芽孢杆菌的生长8,34,提示植物产地与其抗菌活性存在关联。该活性与LC-MS谱图中m/z 289 [M−H]⁻信号(图1A色谱峰1)的出现高度相关,且该信号仅存在于上述两份活性提取物中。
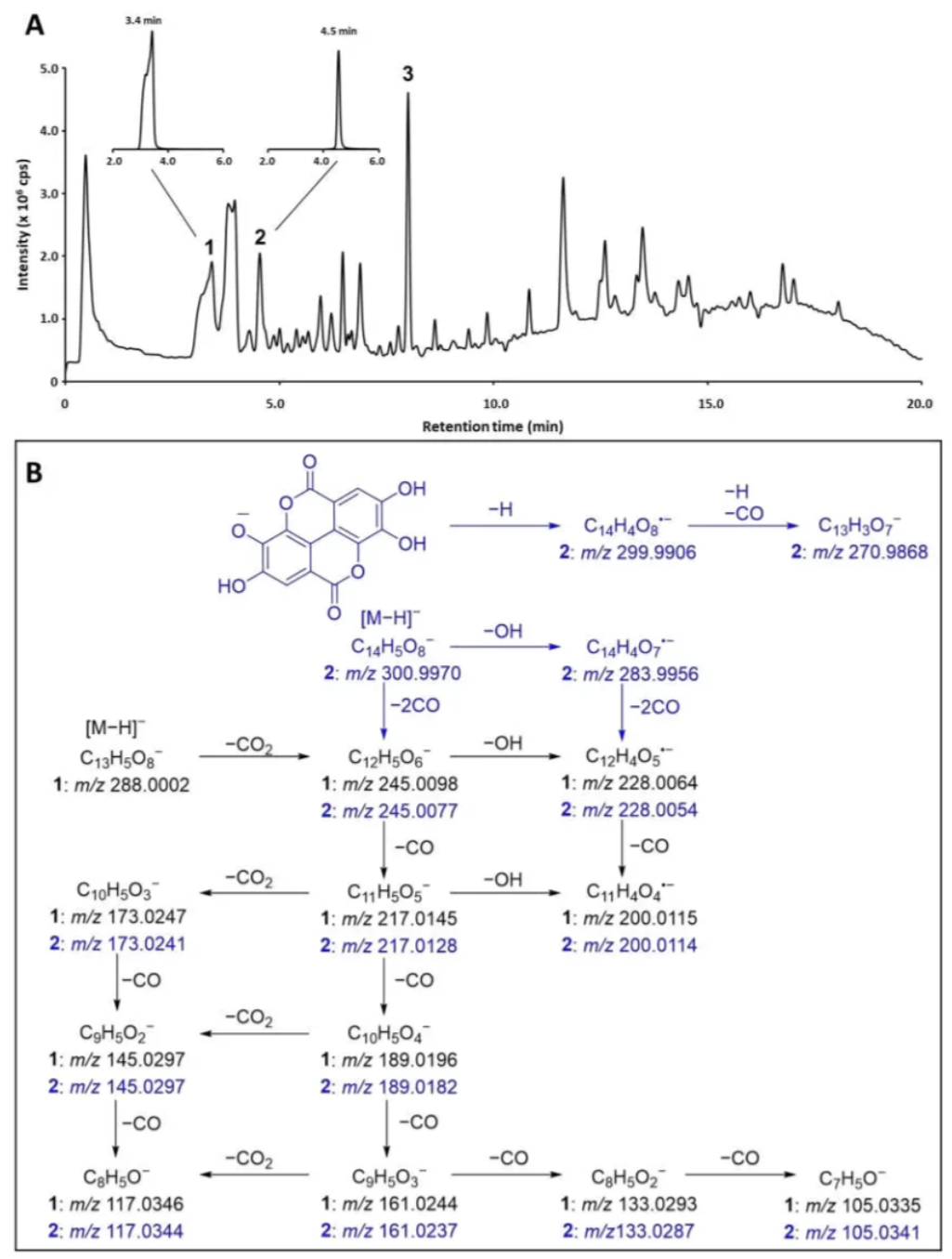
图1. (A) 抗菌活性榄李样本LR7的总离子流图(TIC)及m/z 289.0±0.5(化合物1)和301.0±0.5(化合物2)的提取离子流图。峰3对应3,3′,4′-三-O-甲基鞣花酸(3)。
(B) 推测的化合物1和2的串联质谱(MS/MS)碎裂路径。鞣花酸特有碎片标记为蓝色,共有碎片标记为黑色。
高分辨质谱(HRMS)数据显示,化合物1的分子式为C13H6O8,其[M−H]-离子m/z实测值为289.0002(C13H5O8-理论值288.9990,质量偏差4.2 ppm,图S5)。与鞣花酸(2)相比,化合物1的分子量减少12 amu,表明其少一个碳原子。
该分子式目前仅对应一个已知天然产物——桑黄(Phellinus igniarius)中分离得到的phelligridin J (4)(3-羧基-8,9-二氢吡喃并[4,3-c]异色烯-4-酮,图2)35。然而,化合物1的二级质谱(MS²)碎裂行为与2高度相似(图1B),预示二者结构密切关联。
如Schmidt近期报道36,化合物1与2均遵循酚类化合物的特征碎裂路径,伴随多次CO/CO₂丢失及奇数电子氧中心自由基中间体生成,这一机制合理解释了观测到的碎裂模式。
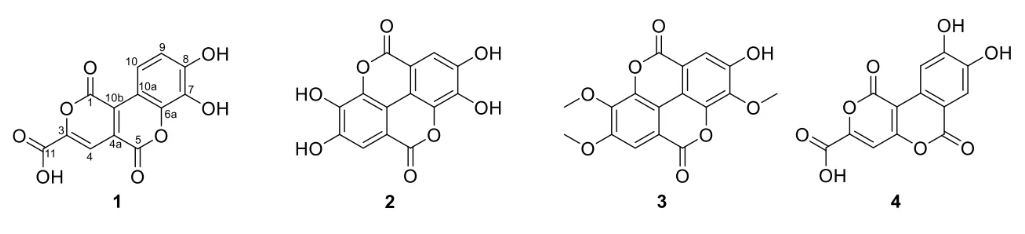
图2. 榄李内酯 (1)、鞣花酸 (EA, 2)、3,3′,4′-三-O-甲基鞣花酸 (TMEA, 3) 和桑黄素J (4) 的结构式。
鞣花酸(2)是植物中广泛存在的次生代谢产物,在使君子科植物中尤为常见,并成为榄李属(Lumnitzera)的化学标志性成分。化合物1与2之间12 amu的质量差提示,1可能具有以下结构特征:五元环取代了2中的六元环,或发生了结构重排并伴随一个(季)碳原子的形式消除。为通过核磁数据明确解析其结构,必须对化合物1进行分离纯化。
分离纯化过程:
首次在非酸性条件下分离得到2.5 mg 化合物1(该化合物在甲醇中溶解度较低)
从剩余的15.06 g干燥根样本中,再次分离获得14.6 mg 化合物1
通过调节液液萃取条件(乙酸乙酯萃取粗提物时对水相进行酸化),成功使该黄色化合物转移至有机相
最终经Sephadex LH20柱层析、反相RP2材料分离及半制备型反相高效液相色谱(RP-HPLC)多步纯化,获得高纯度样品
尽管获得了初步核磁数据(表S1),但首次分离的样品量不足以进行二维核磁结构解析。最终获得的高纯度样品为后续结构鉴定提供了充足材料。
化合物1为黄色无定形固体。在反复溶解与干燥过程中,该物质逐渐变为红色且在甲醇中溶解度降低,表现为可逆的向红移现象(薄层色谱验证见图S1)。
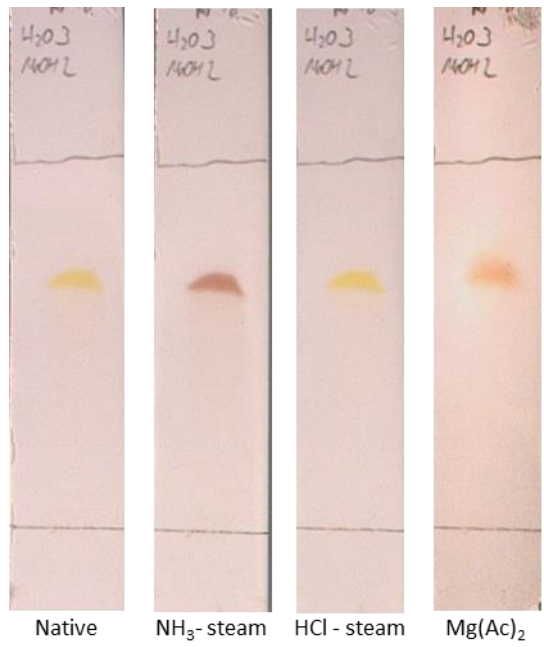
图 S1 lumnitzeralactone(1)的 Bornträger 反应薄层色谱(TLC)图;固定相:RP18,展开剂体系:水 - 甲醇(体积比 3:2)
在氨蒸气作用下,化合物1的黄色斑点立即变为红色,而氯化氢蒸气可使其恢复亮黄色。使用醋酸镁甲醇溶液喷洒薄层板后,因酚氧阴离子生成(机理见Scheme S1)37,红色得以稳定保留,该现象属于典型的Bornträger反应。在中性条件下首次提取时观察到的溶解度下降,可归因于酚氧阴离子形成的稳定盐显著增强了分子极性。
这种卤色效应(分子电荷变化导致盐诱导的显色变化)源于酚氧负离子中氧原子自由电子参与的广泛电子离域,强有力提示化合物1存在酚羟基,这与鞣花酸衍生物的结构特征相符。其紫外-可见吸收光谱在232 nm(4.10)、290 nm(3.95)和407 nm(3.96)处出现最大吸收峰(图S9-1),与文献37-39报道的苯环、共轭羰基及酚羟基特征吸收一致。
在CD3OD中测定的¹H NMR谱(图S2-1,表S1-1)显示三个质子信号:δH 6.87(d, J = 9 Hz)、7.59(s)和8.46(d, J = 9 Hz),其中δH 6.87与8.46位质子存在邻位耦合(COSY与TOCSY谱验证,图S2-2、S2-3)。该耦合模式与仅显示两个芳香族单峰的化合物2不同。
在DMSO-d6中测定的¹H NMR谱(表1,图S2-7)额外显示两个酚羟基质子信号(δH 9.56和10.62,宽单峰)。¹³C NMR谱(DMSO-d6,表1,图S2-8)出现13个碳信号,与分子式相符,包括三个羰基/内酯碳信号(δC 160.0、158.3、158.2)及十个其他碳信号(含七个季碳,其中δC 132.7和150.8为连氧季碳)。
通过HSQC谱归属三个质子化sp2碳(δC 113.2、117.9、107.3)。值得注意的是,在非酸性条件下分离的样品于CD3OD中测定¹³C NMR时仅出现11个碳信号(图S2-4,表S1-2),缺失的C-3与C-11信号通过HMBC相关峰(图S2-6)得以确认,其高场化学位移提示该条件下化合物以盐形式存在。
表1. 化合物1、合成产物1b与5的¹³C NMR (100 MHz) 与¹H NMR (400 MHz) 数据对比表
 a. 与Tokutomi等40研究报道的核磁共振数据一致。
a. 与Tokutomi等40研究报道的核磁共振数据一致。
基于所获数据,化合物1的结构很可能包含以下特征:三个质子化sp2碳(其中两个为邻位耦合的芳香质子)、一个羧基及两个酚羟基。由此推断其应为一个稠合三环体系(含两个内酯环),即结构为桑黄素J(4)的区域异构体35。由于化合物1质子信号稀少,仅靠COSY与HMBC相关难以完成全结构解析。
为避免样品损耗且未获得决定性信息,未对分子进行衍生化(如羟基甲基化或羧基甲酯化)。因此优先选择非破坏性方法。尽管已尝试针对含类似结构单元的分子报道的结晶方法40,42,43,仍未获得适用于X射线分析的晶体。
后续解析转而依赖高场核磁下的非常规二维谱技术,包括¹³C-¹³C INADEQUATE、1,1-ADEQUATE及1,n-ADEQUATE实验。
¹³C-¹³C INADEQUATE通过1JCC耦合展示碳原子间相邻连接关系,但天然丰度13C样品的检测灵敏度极低(13C-13C自旋耦合比仅0.012%),需高浓度或13C富集样品44。因条件所限,持续3天的测试未获得有效相关信号。
随后进行的1,1-ADEQUATE实验通过伪2JCH相关定位质子化碳的相邻碳原子45,成功指认关键结构片段:
H-9与C-8(δC 150.8)、C-10相关
H-10与C-9、C-10a(δC 108.1)相关(图S2-12)
H-4与C-4a(δC 125.1)、C-3(δC 145.8)的相关性(图3)进一步确认稠环连接方式

图3. 化合物lumnitzeralactone (1)的关键二维核磁共振相关信号:HMBC(红色,因相关信号过多分两式展示)、1,1-ADEQUATE(黑色)与1,n-ADEQUATE(蓝色)
1,n-ADEQUATE实验可在天然丰度条件下提供长程碳-碳连接信息46,主要通过伪4JCH(1JCH + 3JCC)相关信号实现,偶尔也可观测到3JCH(1JCH + 2JCC)相关47,48。与常规INADEQUATE实验相比,其灵敏度最高可提升64倍49,适用于微量样品分析。
除最常见的3JCC和少量2JCC相关外,该技术还能检测1JCC相关信号48,50,这与1,1-ADEQUATE谱图特征相似。通过识别1,n-ADEQUATE谱中渗入的1JCC相关信号的反转特性48,50,可明确区分1JCC(蓝色等高线,图S2-11)与nJCC相关(红色等高线,图S2-11),实现单次实验同时获取两类耦合信息。但需注意,1,n-ADEQUATE的灵敏度低于1,1-ADEQUATE。
结合H-9与H-10至C-6a(δC 142.8)和C-7(δC 132.7)的HMBC(3JCH)与1,n-ADEQUATE(4JCH)相关信号,成功指认上述碳位(图3、S2-11)。C-10b的指认较为特殊:该碳与三个质子(H-4、H-9、H-10)均显示HMBC相关。
H-10和H-4与C-10b的强HMBC相关(3JCH)表明空间邻近性,而H-9虽HMBC信号较弱,其1,n-ADEQUATE相关(4JCH)佐证了长程耦合。
三个羰基碳的指认更为复杂:H-4与δC 160.0(C-11)的1,n-ADEQUATE相关(3JCH)得到强HMBC信号支持。DMSO-d6中δC 158.2和158.3处两个未分辨的羰基碳信号,其与H-4的1,n-ADEQUATE相关可能对应3JH4-C5或4JH4-C1耦合,但难以明确区分。尽管这两个信号可能属于C-1或C-5,但在CD3OD中分辨率显著改善(表S1-2、S1-3)。最终通过H-4的强HMBC相关(3JCH)指认C-5位。
为定位羟基基团,本研究参照Vemulua等人成功解析菲并苝醌类色素结构的策略51,在-20°C的CD3OH中进行了低温HMBC实验(图S2-13)。在此特殊核磁溶剂与条件下,甲醇的羟基未被氘代,使得化合物羟基质子无法发生氘交换而保持尖锐信号。
δH 10.62(宽单峰)的羟基质子与C-7、C-8和C-9存在相关信号,表明其位于C-8位;另一羟基质子(δH 9.56,宽单峰)未检测到相关峰,可能源于二维核磁谱信噪比不足、样品浓度过低或硬件限制(如观测频率不足或探头性能局限)52。通过H-9和H-10与C-7的HMBC相关信号,可间接推定第二个羟基位于C-7位。所有HMBC谱数据汇总于表S1-3与图S2。
综合全部数据,化合物1的结构最终确定为7,8-二羟基-1,5-二氧代-1,5-二氢吡喃并[4,3-c]色烯-3-羧酸(图3)。根据其来源属名Lumnitzera,该化合物被命名为lumnitzeralactone。
为验证化合物1的结构,本研究采用ACD/Labs软件中的结构解析模块(ACD/Structure Elucidator)进行计算机辅助分析。基于所有可用的核磁数据与分子式(未预设结构片段)构建计算数据集。尽管可生成"Found Fragments"(FF)碎片库(尤其适用于质子缺失型分子),本次计算仍采用通用模式以确保结果客观性。
经过超过18小时的计算,ACD-SE仅生成44个结构提案(数量显著低于常规情况)。通常90%以上的测试集可在30分钟内完成计算,但存在耗时超48小时且输出超500个提案的案例53。值得注意的是,当提供高质量的谱图数据集(如二维谱、1,1-ADEQUATE)时,即使挑战性分子也仅需数分钟即可完成计算53,54。

图S8-1. ACD-SE软件报告(部分)

图S8-2. ACD-SE生成的结构列表概览
在计算结果中,化合物1的推定结构以八种不同碳原子标注变体出现(主要差异在于羰基碳C-1/C-5/C-11及单氧键芳香碳C-6a/C-7的¹³C指认)。结构提案的排序基于dN(¹³C+¹H)参数(预测与实验化学位移平均偏差)。排名首位的提案(dN=3.888)具有正确的碳原子归属方案,且正确提案同时出现在第2-4、7、8、11和12位(完整排名见图S8),充分验证了lumnitzeralactone (1)的结构注释。
通过DFT计算进一步验证结构,选取lumnitzeralactone及其四种异构体(II-V)进行量子化学建模(图4、表S2-1)。每种结构仅获得一个主导构象(表S2-2)。
通过对比实验与计算化学位移,DP4+分析显示:lumnitzeralactone (1)的¹H-DP4+概率达99.89%、¹³C-DP4+为100%、(¹H+¹³C)-DP4+为100%,而异构体II-V的概率接近0%,确证化合物1的结构正确性。

图4. 化合物lumnitzeralactone (1)及其异构体结构的DP4+概率分析(基于¹H和¹³C NMR实验数据与理论计算核磁屏蔽张量的相关性分析)。计算方法采用PCM/mPW1PW91/6-311+G(d,p)//B3LYP/6-31+G(d,p)理论水平计算核磁屏蔽张量,通过实验值与计算值的相关性分析获得DP4+概率。目标化合物1的¹H DP4+概率为99.89%(蓝色柱状图),¹³C DP4+概率为100%,综合概率(¹H+¹³C)达100%;而异构体II-V的所有DP4+概率均为0%。分析结果表明,DP4+概率>99%证实理论计算与实验数据高度吻合,确证分离得到的天然产物结构为lumnitzeralactone (1),排除其他异构体(II-V)的可能性。该方法通过量子化学计算与统计学分析相结合,为复杂天然产物的结构鉴定提供了可靠依据。
为确证lumnitzeralactone (1)的结构,本研究通过化学合成提供了决定性证据——该步骤对许多争议性天然产物的结构确证至关重要55,56。如Scheme 1所示,以鞣花酸 (2)为起始原料,通过两步反应成功合成目标产物1b。
 Scheme 1. 以鞣花酸 (2)为原料通过稳定中间体(5)两步合成lumnitzeralactone (1b)的化学合成路线
Scheme 1. 以鞣花酸 (2)为原料通过稳定中间体(5)两步合成lumnitzeralactone (1b)的化学合成路线
第一步为2的光氧化反应,生成结构与天然产物1相似的中间体5。参照Tokutomi等人43的方案,在优化条件下(氧气氛、冰浴控温)实现了中间体5的高效制备。中间体5的核磁数据(图S3、表1)与高分辨质谱数据(表2、图S7)均与文献报道一致43。
第二步尝试采用铜催化/银催化芳香酸选择性脱羧策略57,58,但未观察到目标产物;转而采用热脱羧法,在180℃甲苯中将5转化为目标单脱羧产物1b(伴生副产物)。
表2. 天然lumnitzeralactone (1)及合成化合物(1b和5)的反相超高效液相色谱-四极杆飞行时间串联质谱表征分析

合成所得lumnitzeralactone (1b)的核磁数据(表1、图S4)与高分辨质谱数据(表2、图S6)与天然lumnitzeralactone (1)的数据完全一致,确证了合成路线的有效性与结构准确性。
在研究的31份榄李样本中,仅有两份检出化合物18,34,表明该天然产物的生物合成可能不(完全)依赖于宿主植物(种群水平遗传变异较低59),而是与特定环境条件下的共生微生物相互作用相关。
我们推测真菌通过酶促反应参与从化合物2到1的转化过程。Aguilar-Zárate等60的真菌发酵实验曾检测到与1质荷比相同的未知鞣花酸降解产物。一种可能的生物合成路径始于自由基触发的(氧化性)脱羧反应(由真菌来源的氧化酶催化),随后经历氧化-环化等步骤(方案S2-1)。
真菌可产生多种胞外氧化酶作用于多酚类物质61-66,而真菌源脱羧酶已知参与木质素67-69及鞣花单宁/没食子单宁的降解70。
 Scheme 2. 推测的lumnitzeralactone (1)生物合成途径:通过活性氧(ROS)介导的氧化环化或双加氧酶催化形成过氧内酯中间体
Scheme 2. 推测的lumnitzeralactone (1)生物合成途径:通过活性氧(ROS)介导的氧化环化或双加氧酶催化形成过氧内酯中间体
然而,化合物1主要存在于根皮组织中,目前尚无证据表明其形成仅发生于表皮层或由内生真菌参与,也未明确鞣花酸 (2)、其衍生物或lumnitzeralactone (1)在物种间的转运机制。
由于化合物1仅在两种具有抗菌活性的粗提物中被检出8,34,我们推测其可能参与抗菌作用。然而活性测试表明,化合物1本身并未显示细菌生长抑制活性(表3)。
表3. 榄李(L. racemosa)粗提物、活性组分(均为500 µg/mL)及纯化合物(100 µM)对革兰氏阳性菌枯草芽孢杆菌的抑菌活性

有趣的是,纯化过程中以1为主要成分的馏分却表现出显著抗菌效果(500 µg/mL浓度下抑制率达95%,表3)。对该活性馏分的代谢物分析发现,除1外还存在化合物3(图S10)。
与文献报道一致71,化合物3在100 µM浓度下对测试菌株表现出近100%的抑制率(表3)。但31份榄李粗提物的广谱分析表明8,3在多数样本中普遍存在且其分布与抗菌活性无相关性,因此并非红树林提取物抗菌作用的主要贡献者。
如前述,红树林常与真菌等微生物共生。对包括榄李在内的红树林内生真菌的系统研究表明32,71种代表性内生真菌提取物对革兰氏阳性菌(枯草芽孢杆菌、金黄色葡萄球菌)和革兰氏阴性菌(铜绿假单胞菌、大肠杆菌)均具有显著抗菌潜力。
结合本研究结果,我们推断能够代谢鞣花酸的真菌可能对特定榄李样本的抗菌活性具有贡献。
略。(见原文)
本研究首次从真红树林植物榄李(Lumnitzera racemosa)中分离并鉴定了一个新型化合物lumnitzeralactone (1)。通过综合的结构解析手段明确了其结构,包括在不同溶剂及低温条件下测定的¹H NMR、¹³C NMR、二维核磁谱(COSY、TOCSY、HSQC、HMBC、1,n-ADEQUATE、1,1-ADEQUATE),以及高分辨质谱(HR-MS)、计算机辅助结构解析(CASE)、密度泛函理论(DFT)计算和化学合成。
值得注意的是,从具有抗菌活性的粗提物中分离得到的lumnitzeralactone (1)并未对枯草芽孢杆菌表现出显著抗菌活性,与预期不符。
研究提出了化合物1可能的生物合成途径,并指出共生微生物及其分泌酶可能参与该过程。基于微生物的修饰或诱导作用也可解释同一物种在不同采集地点表现出差异抗菌潜力的现象。
尽管化合物1本身未显示显著抗菌活性,但其仅存在于具有抗菌活性的粗提物中。粗提物的活性可能源于尚未鉴定的高活性微量成分。
综上所述,印度尼西亚红树林仍是具有开发潜力的生物活性物质来源。

往期推荐
基于CASE-DFT对浅黄枝衣中质子缺失型Chlorodepsidones的结构解析及Flavicansone的结构修订
04-13 技尔 GL Sciences
活动预告 | 德国斯派克将参加中国国际数据中心液冷关键技术年会04-13 市场部
纳克微束邀您参会|2026年华东地区电子显微学学术交流会04-13 纳克微束
【直播预告】肿瘤免疫课题攻坚难!组织孵烂了,关键免疫 marker 还不显色……04-12
【仅需235元】告别台盼蓝,开启“无毒”细胞计数新时代!04-10 赛默飞生命科学
春启新程,智汇英才|纳克微束(北京)有限公司招聘启事04-10 纳克微束
今天聊聊:ADC 和自身免疫性疾病04-10 小 M
产品试用 | 先试一下!MCE 类器官培养基,是谁还没→薅羊毛04-10 小 M
激酶家族:从分类到关键靶点,一文读懂!04-10 小 M
以象科技-高光谱采集系列 | 布料HL27053高光谱采集04-10 以象科技
Endpoints News独家:Ailux加速人才布局,阿斯利康资深高管出任首席科学官,2027年临床在望04-10 EndpointsNews
晶泰科技旗下Ailux任命Maria G. Belvisi博士为首席科学官,持续升级全球研发布局04-10 晶泰科技
Empower学院计划(三)|Empower MVM助力分析方法周期管理04-09 沃特世
Empower软件使用小技巧(三十七):批处理前如何预览峰纯度计算结果04-09 沃特世
微塑料分析难?沃特世APGC给出全新答案04-09 沃特世
Sievers分析仪如何应用于微电子行业?04-09 Sievers分析仪
《Analytical Chemistry》原位K-Ca地质年代学应用:使用六氟化硫在iCAP TQ ICP-MS/MS中有效去除氩基离子干扰04-09
IGC 2026逛展攻略 | 益世科生物A02展位“隐藏玩法”大公开!04-09
Esco ACC/AMC系列新品上市,让精准计数从“源头”开始04-09
线上/线下课程丨原子吸收仪器使用及维护培训欢迎您参加!04-09
