TDM难点药物 | 如何优化β-内酰胺类抗生素给药方案?
2024-02-20 15:19:26 湖南德米特仪器有限公司


1
β-内酰胺类抗生素详解,哪些患者群体需要TDM?
与通常获得血清浓度的其他药物类似,并非所有β-内酰胺疗程都需要TDM。对于感染了最小抑菌浓度(MIC)接近或高于易感性断点的病原体,有器官衰竭或其他明显改变β-内酰胺PK的情况,或没有其他现成的、合理的替代治疗的重症感染患者,β-内酰胺类抗菌药物实施TDM可改善患者预后。
1、危重症患者;
2、肾损伤患者;
3、使用器官支持技术,如体外膜氧合(ECMO)、分子吸附剂循环系统(MARS)和肾替代治疗(RRT),可进一步分为间歇血液透析(IHD)和连续肾替代治疗(CRRT)的患者;
4、囊性纤维化患者;
5、其他需要考虑的人群可能包括儿科、肥胖患者、移植受者、中枢神经系统(中枢神经系统)感染(可以直接采样,而不是使用血清水平作为替代标记)、已知具有多重耐药性的患者几乎没有其他治疗方案的生物体需要施用比 FDA 批准的更高剂量的 β-内酰胺才能达到临床治疗暴露。
使用 β-内酰胺治疗药物监测的精选案例研究
2
β-内酰胺类抗生素药物起点 | 确定PK/PD目标
在浓度超过2-4×MIC时,β-内酰胺抗生素可以最好地归类为时间依赖性杀菌剂,因此,浓度的进一步增加不再对大多数病原体提供更快或显著更大的杀灭作用。相反,游离浓度作为剂量间隔的函数保持在最低浓度以上的时间(%fT>MIC)似乎最好地预测了体外、体内动物和人类暴露反应研究期间的抗菌效果。类似细菌密度降低所需的%FT>MIC可以通过β-内酰胺类进一步区分,头孢菌素、青霉素/单贝坦和碳青霉烯类通常以大约50%-70%、50%-60%和40%的FT>MIC实现1-2 log10的细菌菌落形成单位(CFU)的降低。
50% 至 70% 之间的 FT>MIC 暴露是现有青霉素、头孢菌素和碳青霉烯类药物的合理目标。但新型 β-内酰胺抗生素,例如 β-内酰胺/β-内酰胺酶抑制剂组合(头孢他啶-阿维巴坦、头孢特洛扎-他唑巴坦、美罗培南-瓦波巴坦等)和头孢地罗可能需要不同的 PD 阈值,特别是当还考虑抑制剂浓度时,需要进一步的人体研究来确认这些新药物的体外和体内小鼠靶标。
3
高参考意义,临床研究整理总结
随着越来越多的数据支持这些β-内酰胺PD靶点,重要的是确定在实践中达到这些靶点的频率。许多研究的一个共同点是,感染机体的MIC是不可得的。因此,大多数研究采用了流行病学截断值(ECOFF)或假定/确定的病原体的易感性断点。有可能患者有由病原体引起的感染,且MICs远低于这些阈值。尽管许多这些研究没有报告临床结果,但它们强调了相当大比例的患者未能达到预定的β-内酰胺疗效目标。
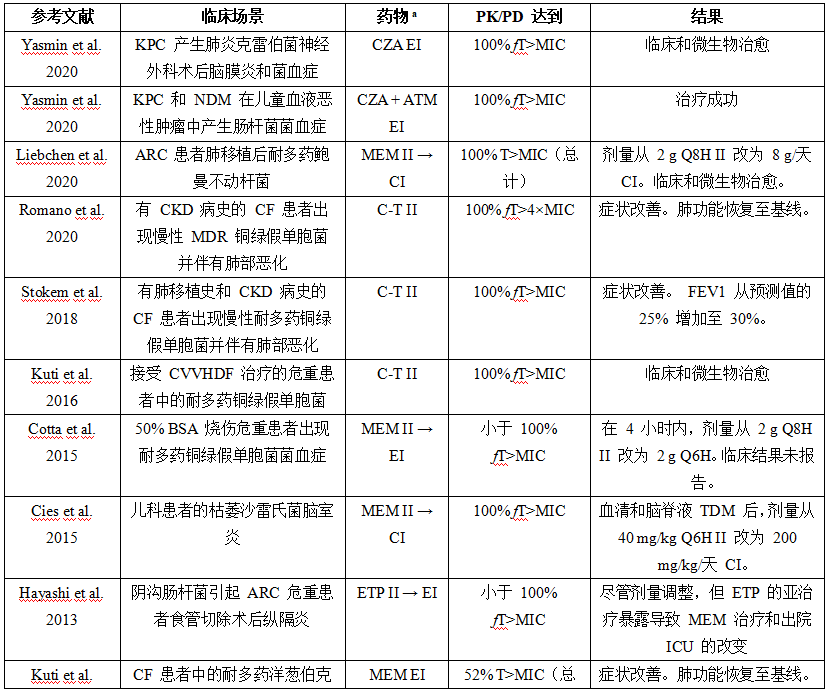
2010-2020年发表的评估β-内酰胺治疗药物监测的临床研究总结

缩写:CI,连续输注;CRRT,连续肾脏替代治疗;EI,延长输液;FN,发热性中性粒细胞减少症;fT>MIC,游离浓度保持高于 MIC 的时间;ICU,重症监护病房;II、间歇输液;IMP,亚胺培南-西司他丁;KPC-KP,肺炎克雷伯菌,产碳青霉烯酶肺炎克雷伯菌;MEM,美罗培南;MIC,最低抑菌浓度;PK/PD、药代动力学/药效学;RCT,随机对照试验;SC,血清浓度;SICU,外科重症监护病房;TDM,治疗药物监测;TZP,哌拉西林-他唑巴坦。并非所有病例均仅使用 β-内酰胺治疗,但本表仅包含使用 TDM 的 β-内酰胺。列出的输注策略适用于初始方案。许多药物都通过 TDM 进行了改变,以达到目标浓度。
有多种输液策略可以优化β-内酰胺剂量以实现PK/PD目标,但都存在诸多限制。虽然传统的5-60min间歇输液仍然很普遍,但这可能会导致标准给药方案的 fT>MIC 和接近药敏断点的 MIC 较低。延长输液时间超过3或4小时会将峰值转移到给药间隔内,这在某些MIC将增加fT>MIC;连续输注(在给药间隔内不间断地施用每日剂量)是优化 fT>MIC 的行之有效的方法。值得注意的是,这两种方法通常也要求将剂量提高到可能被认为是标准的水平以上,而且两种方法都不能保证目标的实现,甚至会影响减少TDM的效用。
4
给药方案:专家建议一览
TDM 测定方法
β-内酰胺在室温下的不稳定性提出了一个独特的挑战,因为样品最好保持在冰或冷冻上,直到加工以限制降解。建立收集和记录样品、时间和条件的协议是必要的,以确保分析前样品的完整性。
大多数内部β-内酰胺定量方法采用色谱分离结合紫外(UV)或质谱(MS)检测,德米特色谱质谱产品以其高自动化、高灵敏度、高分辨率等技术优势,更适用于抗菌药物的血药浓度测定。理想的分析方法要求定量下限低于常见病原体的MIC值,定量上限≥100mg/L,以便避免需要稀释的重复分析。分析运行时间应最小化,快速样品制备,并需要彻底验证以评估许多变量,包括:精密度、准确度、线性、稳定性和干扰。
“fT>MIC”参数的一个关键要素是游离的未结合的生物活性抗生素成分。大多数β-内酰胺与各种血清蛋白(主要是白蛋白)结合,通常在临床可达到的浓度下以线性、剂量成比例的方式结合。已公布的 β-内酰胺蛋白结合百分比差异很大,从美罗培南的 2% 到头孢曲松的 96%。因此,一旦获得β-内酰胺浓度并报告,在与给定的目标MIC值整合之前,应该对蛋白质结合进行校正,以估计自由暴露。当自由分数不直接测量时,进行PK建模后,文献中报道的目标总体的平均自由分数是合理的。解释β-内酰胺浓度的另一个重要警告是,血浆测量不一定反映感染部位的抗生素浓度。理想情况下,抗生素浓度应分别在肺部上皮内层液(ELF)或肺部感染和中枢神经系统感染的脑脊液中测量。虽然有一些方法可以达到这些测量,但它们对患者有一定的风险,因此仔细考虑它们的价值是至关重要的。值得注意的是,血浆浓度往往是感染部位可达到的暴露的一个很好的替代指标。
MIC检测
了解β-内酰胺在体内的游离浓度对 TDM 至关重要,但如果不能与药物对致病生物的 MIC 进行比较,其效用就会受到限制。了解特定的β-内酰胺 MIC 对于解释可达到的暴露和如何进一步优化给药方案至关重要,尤其是考虑到实践中看到的广泛的β-内酰胺 MIC。这在革兰氏阴性病原体中尤其明显,其中β-内酰胺 MIC 值可能非常小,并且非常容易受到高达100倍的高水平耐药性的影响。
由于 MIC 测量本身已确定的可变性,应将单个报告值视为一个范围,真正的 MIC 值很可能高于或低于1稀释度。对于处于或接近易感点的MIC值,当应用 TDM选择最佳药物方案时,可以使用比报道的稀释度高1倍的值来考虑这种可变性。然而,对于在耐药性范围内的 MIC 值,这种保守的练习可能会阻止使用可靠的安全数据支持的给药方案。
一种全面阐明MIC的解决方案是琼脂基梯度条法市面上可用的ETEST®(bioMérieux, Inc)和MIC试纸条(Liofilchem, Inc)都使用了浸渍过抗生素浓度梯度的塑料薄片。这些条带应放置在一个琼脂平板上,该平板以标准化的方式接种了感兴趣的生物体。在孵育过夜后,通过确定生长抑制区域的下半部分与浸渍条的交点来读取平板的MIC值梯度条带法与抗生素敏感性测试的标准方法(包括微量肉汤稀释)进行了比较,在众多临床分离株中显示出极好的一致性。与临床实验室的合作对于了解哪些系统可以最好地报告MIC值是至关重要的。例如,从ICU分离的所有CF分离株和非发酵革兰氏阴性菌可能需要使用梯度条法,以便为TDM提供MIC。应该大力考虑一种系统的方法来确定哪些生物需要进行除自动抗菌素敏感性测试(AST)系统之外的额外检测,并且当地流行病学应该指导这些决定。
分析和可用软件
一旦确定了MIC和β-内酰胺浓度,剩下的部分是样品的收集和现有方案的解释。虽然最好在治疗第一天收集样本,以免延误对方案的解释,但对于临床不稳定的患者,至少应推迟到肾功能稳定后才收集样本。我们推荐的抽样策略包括两个或更多(最好是三个)样本,并使用总体PK软件和贝叶斯模型进行评估。这种方法类似于最近的万古霉素指南中的建议基于贝叶斯模型的TDM应该为单个患者提供最精确的PK剖面,允许精确计算T>MIC,以及需要修改哪些剂量才能达到PD目标。对剂量优化软件所需的理想采样时间点数量进行了分析,一项针对危重患者哌拉西林使用的研究表明,两个样本比一个好得多,几乎与三个或三个以上的样本一样好。另一个需要考虑的问题是,在整个给药间隔时间内采集样品。在接受美罗培南治疗的发热性中性粒细胞减少症和菌血症患者中,注射开始后的最佳采样时间为30分钟(即注射结束时)、1小时、2小时、4小时或6小时定义β-内酰胺暴露的最关键的PK变量将是清除;因此,建议至少两个采样时间点,一个为中点(或至少在延长输液方案结束后30分钟),后者为谷。这将允许对药物的最终消除阶段进行适当的表征。临床药师应认识到检测下限,如果不够敏感,应根据需要调整采样时间点,以增加获得真实值的可能性。建议在注射完成后不久收集第三个样本以表征峰值。如果需要额外取样,在最后消除阶段再加一个取样是最合适的。虽然上述采样方案是理想的,但如果临床情况需要,可以考虑其他时间点(例如,与化学药品同时采集,以减少线路中断)。重要的是,应该记录准确的采集时间,而不是四舍五入到最近的30或60min间隔。
有各种软件/程序可供使用,每一种都有自己的长处和短处。应用程序是基于Web还是需要下载并安装在设备上存在差异。定价范围很广,从免费到每月或每年订阅。某些程序可以直接集成到电子病历中。同样需要注意的是,许多用于贝叶斯建模的软件应用程序都有有限的经验证的β-内酰胺库,这使得考虑与可用的β-内酰胺相比,每个机构最感兴趣的是监测哪种β-内酰胺变得很重要。另外一个考虑点是患者群体,因为很少有方案适合用于儿科。考虑和审查这些差异是至关重要的,以确保所选择的应用程序最适合给定的环境和机构。为特定β-内酰胺提供贝叶斯模型的现有程序包括DoseMe®(DoseMe LLC)、ID-ODS®(Optimum Dosing Strategies)、MwPharm++(Medimatics)和InsightRX®(InsightRX Inc.)
对于缺乏贝叶斯软件的β-内酰胺类抗生素,一个替代策略是基于一室一阶方程评估终端消除。在曲线的末端消去部分可以采集两个TDM样品,从C=C0e-kT确定T>MIC。消除速率常数K由两个测量浓度之间的线的斜率表示,C0可以外推。当C=MIC时,超过MIC的时间将发生,可以计算为剂量间隔的百分比,以确定%T>MIC。这种方法假设快速静脉团注给药,这很少用于β-内酰胺的给药,但对于30分钟或更短的输液可能是一个合理的估计。对于较长时间的输液(例如,3-4小时),应该注意,根据生物体的最低浓度,在输液期间可能有一段时间抗生素浓度不高于最低浓度;此外,延长输液后的最大浓度将低于基于快速静脉推注的估计值。最后,许多PD阈值达到研究使用的过于简化的方法涉及单个样本来确定是否满足fT>MIC参数或阈值。在给药间隔中的一个样本可以用来评估现有方案是否达到>50%fT>MIC,而低谷水平可以确定Cmin和是否达到>100%fT>MIC。尽管这种方法可以提供方案达到PD目标的合理指示,但它不允许根据患者的PK进行个体化修改。剂量调整估计可以假设线性药代动力学(即加倍剂量应使浓度增加两倍),但否则改变剂量间隔或输注时间将不容易预测新的暴露。
德米特
集成血药浓度监测色谱质谱技术体系



04-22
CCMT2026开展即高能 | Equator-X™ 双模式测量仪引爆全场04-21
告别预测偏差!Percepta自建专属训练库,pKa预测更准更快04-21 ACDLabs 李丹
世界地球日,查看地球的【愿望清单】04-21
【前沿激荡,智汇北京】IGC 2026圆满落幕,益世科生物共绘细胞基因治疗新蓝图04-21
会议预告|华大吉比爱邀您共赴第六届北京临床质谱论坛04-21 华大吉比爱
叮咚!您有一份来自地球的“绿色盲盒”待拆封04-21 安捷伦科技
聚焦小核酸与多肽前沿分析:第一届创新药物研发与质量评价技术交流会在沪圆满举办04-21 安捷伦科技
糖基化全流程质控:消耗品方案一站式解决04-21 安捷伦科技
药物分析排忧解难系列 | 自动柱前衍生化方案,完美应对样品复杂前处理04-21 安捷伦科技
“衣”路前行,“安”全守护 | 安捷伦 PFAS 解决方案守护运动健康04-21 安捷伦科技
零压力,低成本 | 安捷伦官方认证翻新仪器开启“以租代售”新模式04-21 安捷伦科技
ESCMID 2026 爆点 | MiSeq i100系列携6项病原精准测序应用数据亮相04-21
高效+精准,VA-5000 让实验室气体分析从此不同!04-21 HORIBA
突破制药检测瓶颈,欧美克NS-180Z系列纳米粒度及电位分析仪重磅登场04-21 欧美克仪器
NS-180Z Pro丨纳米粒度电位分析仪04-21 欧美克仪器
【每天学点粒度知识】动态光散射测量粒径应用案例04-21
还有人不知道吗?代谢组才是多组学联用的灵魂04-20
【星品周 | 好礼翻倍】外泌体富集及miRNA提取攻略04-20
烷基汞检测技术及应用网络研讨会04-20 普立泰科