连发五篇:看Biacore如何助力新冠病毒入侵机制研究及治疗药物发现
2020-04-08 16:31:15, Mengmeng Guan Cytiva(思拓凡)
随着连续多天的新增病例清零,以及一座又一座城市的「解封」,来势汹汹的新冠疫情,在广大医务人员的日夜奋战和全国人民的共同努力下,已经得到了有效阻断,国内抗击疫情也已取得阶段性胜利。然而海外的疫情却日益恶化,截至 4 月 1 日,海外累计确诊的病例已经超过 75 万,超过 3 万人死亡。
病毒肆虐的背后,是到目前为止仍然对新冠病毒的入侵机制缺乏详细的了解,也无十分有效的治疗药物。因此研究新冠病毒的详细入侵机制,并在此基础上开发出高效、低毒的药物仍是目前世界范围内对抗新冠病毒的当务之急。
抗病毒药物的研发有多种方案,目前比较常用的主要有以下两种:
一是通过对病毒与相应受体结合的结构解析,发现两者互作的界面,并针对这些互作位点,筛选特异的中和抗体或抑制剂,阻碍病毒表面的蛋白或多糖与细胞表面受体的结合,从而阻断病毒的入侵途径,将病毒隔离在细胞之外。
另一种方式是针对病毒增殖过程,通过筛选特异的抑制剂,阻断病毒核酸的复制、蛋白的合成或病毒的组装,从而阻断病毒在细胞内的增殖,达到治疗的效果。
作为基础科研和药物研发的利器,Biacore 已经广泛应用到各种病毒入侵机制及相应抗病毒药物的研发过程中,如 SARS、MERS-CoV 与受体的识别及中和抗体的研发,乙肝、丙肝、流感以及埃博拉病毒的入侵机制及治疗药物的研发等等。在新冠病毒的传播机制及抗新冠病毒药物研发的过程中,广大的科研工作者也都不约而同地选择了 Biacore 用于新冠治疗药物研发。
经过广大科研人员的不懈努力,一个个喜讯陆续传来。
最近国内多个科研单位,在 Biacore 的助力下,对 SARS-CoV-2 Spike 蛋白 RBD 及受体 ACE2 的结构进行了精确的解析,揭示了新冠病毒入侵的结构基础和关键位点,并发现了多个治疗新冠的候选药物,涵盖中和抗体及靶点特异的小分子抑制剂,连续发表了五篇文章。
本文中小编就跟大家详细解读其中的四篇文章,看看 Biacore 是如何助力新冠病毒入侵机制解析及治疗性药物发现的。
1
对于治疗性抗体开发和疫苗设计来说,解析病毒侵染细胞的结构基础,明确病毒和受体互作的关键位点尤为重要,这就好比要设计一把「钥匙」之前,必须先把「锁」的结构摸清楚。
2020 年 3 月 30 日,Nature 在线发表了清华大学王新泉教授团队的研究成果,他们解析了新冠病毒 Spike 蛋白受体结合结构域与人受体蛋白 ACE2 复合物 2.45 埃的高分辨率晶体结构,并准确定位了新冠病毒 RBD 和受体 ACE2 的相互作用位点,揭示了受体 ACE2 特异性介导新冠病毒细胞侵染的结构基础。在这篇文章中研究人员利用 Biacore 分别检测了新冠病毒和 SARS 病毒的 Spike 蛋白 RBD 与 ACE2 受体的相互作用,结果表明新冠病毒与受体的亲和力要高于 SARS 病毒。而且从动力学数据可以看出,这种亲和力的差异主要是由解离速率引起的(图 1)。
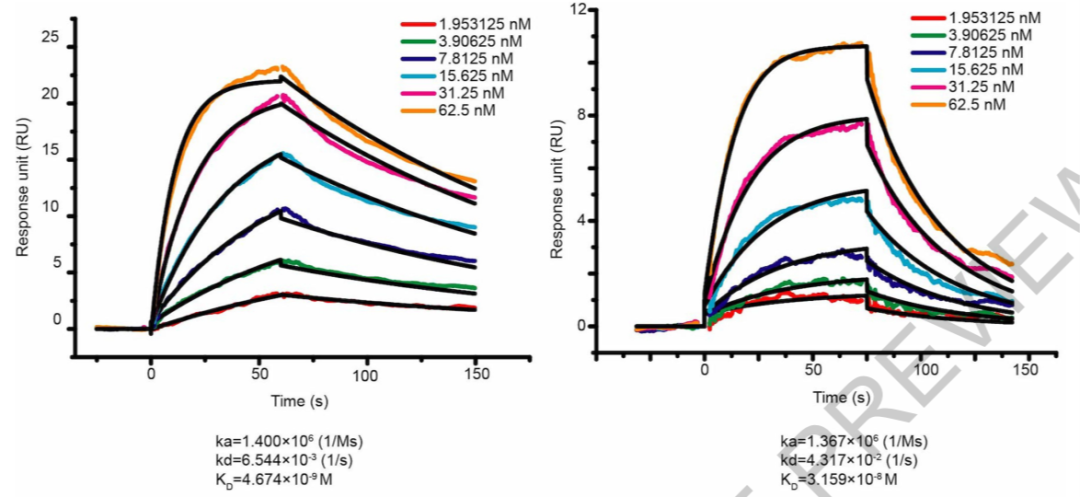
图 1. Biacore 检测 ACE2 与 SARS-CoV-2(左)和 SARS-CoV(右)的亲和力和动力学
有了上述研究成果,在搞清楚「锁」的结构后,「钥匙」就能设计起来了。
2
近日清华大学和深圳市第三人民医院的研究团队合作,从 8 名新冠病毒感染者的单个 B 淋巴细胞中克隆分离了 206 个针对 Spike-RBD 的单克隆抗体,并利用 Biacore 对这些抗体的结合特异性、中和能力以及结合表位进行了深入研究。
他们首先用 Biacore 验证了筛选到的这些抗体和靶点结合的特异性。结果显示这些分离得到的抗体与新冠病毒 RBD 的 亲和力(Kd)都比较强,在 10-8M 到 10-9M 范围内,并且这些抗体只特异性结合 SARS-CoV-2 的 RBD,与 SARS-CoV 和 MERS-CoV 的 RBD 没有交叉反应(图 2),与血浆和细胞实验结果完全吻合。这也解释了为什么之前分离的 SARS 病毒的抗体对新出现的新冠病毒没有中和作用。

图 2. Biacore 检测分离得到的抗体与 SARS-CoV-2 RBD 的亲和力和动力学
然而,抗体结合病毒表面蛋白的特异性和亲和力高低并不足以说明其中和能力,只有具有中和活性的抗体才具有治疗的潜力。随后科研人员又在 Biacore 上巧妙地设计了竞争实验,对这些抗体的中和活性进行研究。科研人员将病毒 RBD 共价偶联在 CM5 芯片上,通过抗体与 ACE2 竞争结合病毒 RBD 的效率来表征抗体的中和效能,只有竞争效率高的抗体能有效阻碍病毒蛋白和细胞受体结合,阻止病毒的入侵。
Biacore 竞争实验结果表明,有两个抗体 P2C-1F11 和 P2B-2F6 能够以近 100% 的效率与 ACE2 竞争和 SARS-CoV-2 RBD 结合,具有潜在的中和活性(图 3)。这与假病毒中和实验结果完全一致(表 1)。在竞争实验中,Biacore 特有的管路进样的设计和连续进样的模式(dual injection),能够实现两种样品连续无缝进样,方便研究人员设计各类竞争实验,获得可靠全面的数据。
图 3. 抗体和 ACE2 竞争结合 SARS-CoV-2 RBD 的 Biacore 检测结果
表 1. 抗体和 RBD 亲和力、与 ACE2 竞争效率以及假病毒中和实验结果
抗体结合不同的抗原表位显示了不同的功能特征和作用机理,因此表位分析是抗体药物研究中的重要环节。那么,这些具有潜在中和活性的抗体是否都结合在相同的抗原表位呢?
随后研究人员选择了 6 个竞争效率高于 70%,具有潜在中和活性的抗体,并利用 Biacore 对其抗原结合表位进行了深入探索。结果表明,这些抗体之间都有不同程度的竞争,例如 P2C-1A3 和 P2B-2F6 几乎与所有检测的抗体都存在明显的竞争,而 P2C-1F11 与 P2C-1C10 之间几乎没有竞争(表 2,图 4)。说明这些抗体所识别的抗原表位既有重叠又有不同,证实这些抗体中和病毒的机制可能有所不同。
表 2. 针对 SARS-CoV-2 RBD 表位分析的 Biacore 结果
图 4. Biacore 对不同抗体结合的抗原表位分析结果
目前 Biacore 升级的表位分析(Epitope binning)模块能提供 Sandwich assay,Premix assay 和 Tandem Assy 等三种实验设计,两小时内即可完成 8x8 组抗体的表位分析,并给出可视化的热图,让表位分析更加简单高效。
回顾整篇新冠病毒的中和抗体研究,Biacore 提供了大量的核心数据,不仅能够确认抗体结合病毒的特异性,提供亲和力和动力学的定量数据,还能对抗体的中和活性、结合表位等进行深入研究,为潜在的治疗性抗体的研发提供了详实的数据。
3
除了中和抗体外,小分子药物开发也是科研工作者的研究热点。中山大学研究团队针对病毒复制所必须的 Mpro 蛋白酶靶点进行了药物筛选。Mpro 是一种 3C 样蛋白酶,可以对病毒在宿主内翻译的蛋白质进行切割,产生病毒复制所必需的非结构蛋白。研究人员利用 Biacore 直接验证了筛选出的候选药物双嘧达莫(Dipyridamole, DIP)与 Mpro 的结合(KD=34uM,图 5)。
图 5.Biacore 验证 DIP 与靶点 Mpro 的亲和力
4
除此之外,武汉大学与华东理工大学研究团队合作,筛选到了针对 DHODH 靶点的抗新冠肺炎候选药物。DHODH,又叫二氢乳清酸脱氢酶,是一种含铁的黄素依赖性酶,它催化嘧啶核苷酸从头合成途径中的第 4 步反应,是抗癌、抗炎、免疫调节、抗疟疾等的重要靶点。
靶向 DHODH 的小分子抑制剂一方面通过阻断嘧啶碱基的从头合成过程,直接切断病毒 RNA 合成的原料供应,另一方面可以调节自身免疫的效果,抑制病毒感染后期诱发的过度免疫反应,达到抗病毒抗炎的双重作用。在前期的研究中,研究人员筛选得到了两种强效的 DHODH 抑制剂,S312 和 S416。它们对禽流感病毒、寨卡病毒和埃博拉病毒都有明显的抗病毒作用。在新冠病毒测试中,两种抑制剂同样显示了强效抑制能力。
图 6. Biacore 检测抑制剂 S312 和 S416 与 DHODH 的亲和力和动力学
而随后的 Biacore 检测结果显示, S312 和 S416 与靶点 DHODH 的亲和力分别为 0.3nM 和 1.69 nM(图 6),呈现出非常好的成药性。特别是 S416,在 SARS-CoV-2 感染的细胞中 EC50 为 17nM ,在细胞水平上抗病毒作用比瑞德西韦强 45 倍,基本上可称得上是目前已报道的体外抑制活性最强的抗 SARS-CoV-2 候选化合物。
并且研究发现这与其和靶点快结合和相对慢解离的动力学模式相关(kon =1.76×106 M-1s-1;koff=2.97×10-3 s-1)。由此可见,除了亲和力的数据,动力学参数对于深入解读药物作用机理有着极其重要的作用。
作为分子互作技术的「金标准」,Biacore 除了能够同时提供亲和力和动力学数据之外,还有非常高的灵敏度,并且对于检测样品的分子量没有下限。作为小分子抑制剂,S312 和 S416 的分子量都很小,结合的信号都非常低,这对检测方法的灵敏度提出了很高的要求,特别是 S312 与靶点 DHODH 互作的最大响应信号不到 5RU,这么低的信号几乎用其他的方法都无法检测。充分体现了 Biacore 极高的灵敏度在小分子药物筛选、表征及优化中不可替代的重要作用。
上述四个例子表明,从病毒入侵和传播机制的阐释,到抗病毒小分子抑制剂和抗体的开发,都离不开 Biacore 提供的精准数据,充分体现了 Biacore 的卓越性能。而在短短半个月的时间里,连续发表五篇高水平论文,离不开广大科研人员的辛苦努力,同样也离不开 Biacore 团队的鼎力协助。从芯片支持到人员协助,从实验设计到数据分析,我们会持续的投入,助力科研人员早日研制出针对新冠病毒治疗的有效药物。
严寒终将过去,
春天如期而至,
Biacore 与大家一起攻坚克难!
参考文献:
1.Potent human neutralizing antibodies elicited by SARS-CoV-2 infection,bioRxiv,March,2020
2.Structure of the SARS-CoV-2 spike receptor binding domain bound to the ACE2 receptor,Nature,March,2020
3.FEP-based screening prompts drug repositioning against COVID-19,bioRxiv,March,2020
4.Novel and potent inhibitors targeting DHODH, a rate-limiting enzyme in de novo pyrimidine biosynthesis, are broad-spectrum antiviral against RNA viruses including newly emerged coronavirus SARS-CoV-2,bioRxiv,March,2020
5.SARS-CoV-2 invades host cells via a novel route: CD147-spike protein,bioRxiv, March,2020
图片来源:图虫创意
06-25
共识速递 | 遗传病SMA最新专家共识发布!06-25
6月19日—21日|CPHI第二十二届世界制药原料中国展—圆满落幕06-25 技尔上海
氨基酸分析仪检测氨基酸纯品中的杂质06-24 大昌华嘉
氨气程序升温脱附测试 (NH₃-TPD) — 脱附能和吸附热的研究06-24 大昌华嘉
润滑油基础油中氮和硫的测试应用---XPLORER NS分析仪06-24 大昌华嘉
大昌华嘉开展Novasina 水分活度仪质量服务月06-24 大昌华嘉
线下培训 | 布鲁克(Bruker)X射线荧光光谱仪用户培训会06-24 大昌华嘉
精彩回顾 | 福立仪器携手纳微科技,共探制药行业新技术06-24
喜讯|奥谱微振获第六届“中国创翼”创业创新大赛厦门市选拔赛“专项赛一等奖”06-24
中科科仪党委召开党纪学习教育专题党课并参观警示教育基地06-24
6月27日 14:30开播 | 电子电器玩具合规性分析的难点及XRF荧光分析应对方案06-24 市场部
短波滤光片产品介绍06-24 韵翔光电
2024长春国际光电博览会圆满落幕!06-24 优尼康
展会预告|苏州、深圳双展本周开幕06-24 优尼康
校企携手育英才,合作共赢谋新篇——宁波工程学院与华仪宁创举行共建联合培养基地签约仪式06-24
血液专题 | NC新研究:血浆蛋白标志物提前7年预测帕金森病06-24
喜讯|中检维康生物连续五年中标广电计量试剂耗材招标06-24
52期名师讲堂预约 | 6月25日,邀您探讨气溶胶光镊相变过程06-24 聚焦光电前沿领域
【展会邀请】微纯生物科技邀您参加2024济南药品质量控制与检验技术大会06-24