面对细胞治疗成本高、产量小,国际制药巨头解决该挑战的策略
2023-02-09 17:38:37 赛默飞世尔科技生命科学产品

免疫细胞治疗利用人体自身或供者来源的免疫细胞,经过体外培养扩增或活化,再回输到患者体内,激发或增强机体的免疫功能,从而清除肿瘤细胞、病原体或病毒感染等异常细胞。
自1986年,免疫细胞治疗泰斗、美国国家癌症研究所(NCI)的Steven Rosenberg首次提出基因工程改造T细胞技术以来,免疫细胞治疗产品经历了30余年的发展历程,CAR-T、TCR-T、TIL、CAR-NK等多种类型的细胞疗法呈现一派百花齐放的态势,并已应用到了广泛的肿瘤以及免疫领域。
不过,细胞治疗产品的特征与传统药品有显著区别,例如:起始原材料来源多样(如自体来源、同种异体来源等);制备工艺复杂(如细胞筛选和纯化、抗原孵育、体外活化、基因修饰或编辑等);自体来源的产品高度个体化,生产规模有限、质量研究和质量控制难度较大等。
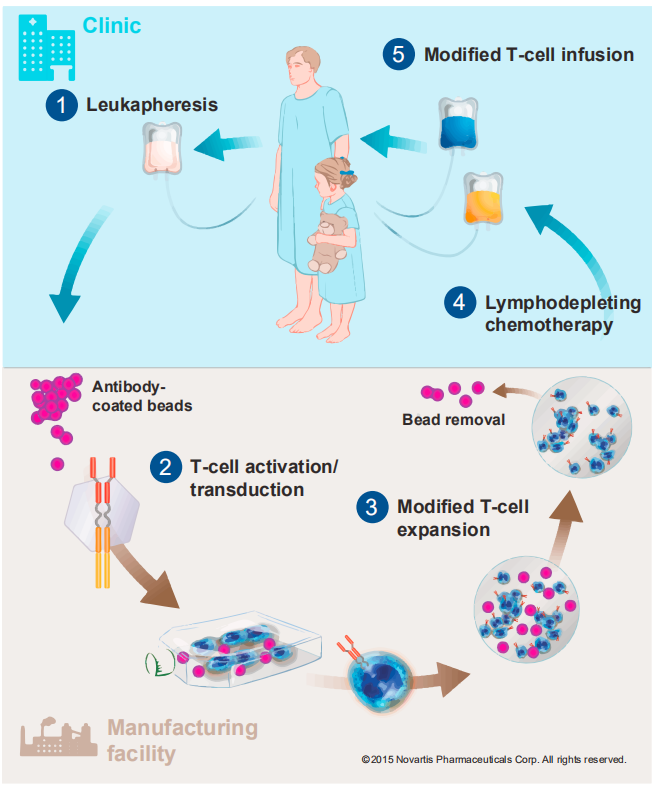
▲ 诺华Kymriah的制备过程(图片来源:Molecular Therapy)
鉴于这些特征,免疫细胞治疗产品面临着规模化生产难、成本高等挑战。以CAR-T为例,最早上市的CAR-T细胞产品至今已经三年有余,在其产业化和商业化探索过程中,业界也已经逐渐清晰的认识到,符合临床和商业规范的CAR-T细胞大规模生产制造,仍然存在诸多难点,使得其目前的患者普及率并不高。
CAR-T目前高昂的治疗费用也是大家关注的焦点之一。对于个体化治疗手段,治疗费用不仅包括生产成本,因样本个体差异而带来的质量控制成本也构成了治疗费用的压力。

▲ CAR-T产品Kymriah与Yescarta的定价(数据来源:星耀研究院)
虽然目前“通用”CAR-T的发展也很迅猛,但是,自体CAR-T依然是主流,疗效往往也是自体CAR-T更好。因此,从提升生产工艺和质量控制方面,来克服免疫细胞治疗产品的挑战,是目前的主要趋势。
解决成本高、产量小的问题,大致可以通过两方面实现,一是提高工艺效率和稳定性,二是降低生产过程中的失败率。
对于前者来说,使用模块化生产体系能够提升生产效率,除此之外,使用创新性的产品和解决方案能够提升质粒和病毒载体的得率。对于后者来说,企业可以更多地采用封闭式生产体系,以及新型、快速的检测方法来提升产品过程质量控制以降低生产失败率。
模块化、封闭式生产体系
提高生产力和安全性
在过去,免疫细胞生产常常以传统人工为主,然而传统的人工操作不仅效率低,还难以保证稳定性;并且开放式生产带来的占地面积大、污染风险、产品一致性差异、耗时长且细胞损耗大等问题,也都极大地限制了产品的制备成功率和最终使用。
随着技术的发展,现在,模块化、封闭式的制造体系已成为行业的发展趋势,其具有提高生产力和安全性的优势。最先拥有商业化CAR-T产品的两家公司,诺华和吉利德/Kite,都经历了从手动到自动化、封闭式的工艺转变,布局先进的细胞疗法制造设施网络提高竞争力的同时,减少了产品制造的周转时间利于患者获得及时治疗。
在国家食品药品监督管理局制定的《细胞治疗产品研究与评价技术指导原则(试行)》文件中,也建议尽量采用封闭或半封闭的制备工艺,以减少污染和交叉污染的风险。封闭式制造系统的使用,还能减少对ISO标准洁净室的需求,降低洁净室的空间成本。结合数字化连接,这些系统能够实现可重复、可跟踪和符合GMP的生产流程。
而模块化设计则提高了仪器的效率和实用性,可以为每个过程步骤选择或设计最适合的程序来优化整个制造过程。例如,细胞扩增等耗时的过程可以与缓冲液更换和细胞浓缩之类的快速过程分开,从而将设施和固定设备的投资减少多达70%。
最后,这些系统还能够有助于避免工艺开发延迟,因为它们从研究到工艺开发和商业制造都使用相同的系统,这将有助于避免与系统变更相关的工艺延迟。
作为个体化治疗的典型代表,CAR-T工艺的稳定性体现于过程控制稳定和严格的质量控制体系。除了尽可能使用封闭式自动化的工艺体系来加强工艺的稳定性外,还可以使用高质量、高批次稳定性的原材料用于生产;严格把控质粒,病毒载体生产工艺和质量标准;对转染、细胞扩增的工艺进行验证;对回输前的细胞进行系统性质控等。
➤ 免疫细胞疗法原材料的选择
原材料是指其生产过程中所用的所有生物原材料和化学原材料。以CAR-T细胞产品为例,这类产品的原材料包括培养基、PBMC分离试剂、T细胞分选试剂、激活剂、细胞因子(如IL-2、IL-7及IL-15)、血清或血清替代物等。
根据相关指导原则,安全性、必要性和合理性,是选择细胞治疗原材料和辅料时需要主要考虑的方面。安全性包括评估原材料或辅料的毒性、可能导致细胞突变或存在致敏可能性的非预期影响等;必要性方面,对于一些高风险的原材料或辅料,可开展工艺去除效果验证或寻找其它替代物或替代来源;除此以外,合理性方面还需要考虑:原材料的目的、功能、作用机制,以及在拟定患者人群中的使用等。
总的来说,细胞治疗市场仍面临着多重的风险,原材料的选择主要考虑高质量、稳定供货、安全、法律支持、无缝转换及商业化用途。
➤ 细胞治疗产品的鉴别
细胞治疗产品的鉴别,即细胞的溯源,是这类产品质量控制与放行检验非常重要的一部分。就自体细胞产品而言,鉴别旨在保证患者使用的是来自自身的细胞。例如,诺华的CD19 CAR-T产品Kymriah,同时通过qPCR检测质粒拷贝数(VCN)和流式细胞术检测CAR表达来鉴别表达CAR的自身T细胞。

▲ 诺华Kymriah关键的质控属性(图片来源:Molecular Therapy)
➤ 生产过程的控制
细胞本身具备体内生存、自主增殖或/和分化的能力,且制备过程可能涉及到病毒转染、外源物质的引进、长时间培养等因素。因此,免疫细胞治疗产品的生产过程控制,包括生产工艺参数和过程控制指标,也具有一定的特殊性。
例如,细胞在体外进行基因修饰/改造时,需要关注基因物质的转导效率、基因进入细胞后的整合情况、细胞的表型和基因型、目的基因的遗传稳定性、转导用基因物质的残留量、病毒复制能力等;细胞在体外进行诱导分化时,需要关注细胞的分化情况、细胞生长特性(如恶性转化等)、细胞的表型和/或基因型、诱导物质的残留情况等。
工艺优化与质控准备
助力免疫细胞疗法产业化、商业化
细胞治疗项目正在从研发到临床试验再到商业批准的过程中迅速发展。然而将研发成果推向市场是一项艰巨的工作,面临着法规监管、工艺放大、稳定性和一致性、风险控制等诸多方面的挑战。
为了满足临床和最终商业化规模生产细胞的需求,一方面,高质量的GMP级细胞治疗原材料和充足的文档支持至关重要,可以最大程度地降低风险,减轻质量控制系统的负担并满足监管要求;另一方面,尽早建立一个稳健,可重复和可持续的工艺,可以帮助加速开发并避免与生产变更相关的延误。
赛默飞世尔科技长期与细胞和基因治疗开发商合作,通过提供创新技术和产品,以及专业知识、服务和定制解决方案,帮助企业的细胞疗法从发现转化到临床研究与商业化生产。
赛默飞提供超过100项领先临床应用案例背书的高度专业化CTS(Cell Therapy Systems)产品线,按cGMP标准生产,拥有严格测试和支持文档,蕴含比研究级产品更有效的监管途径。除此之外,CTS系列产品支持细胞疗法的规模化生产,优化成本;灵活、封闭式的生产体系适用于广泛的细胞处理,并能够提高生产力与安全性。相信依托于扎实数据支撑的一座座里程碑,将连线擘画细胞疗法规模化、商业化的成功之路。
封闭式细胞生产
Gibco™️ CTS™️ Rotea™️ 逆流离心系统
Gibco CTS Rotea逆流离心系统是一款适用于细胞治疗生产的灵活、可扩展、封闭式的细胞处理系统。这种多功能系统可在细胞治疗开发和生产系统中提供非凡的灵活性。它将成熟的逆流离心方法应用于广泛的细胞处理应用,如CAR-T治疗、干细胞治疗和PBMC分离。
Gibco CTS Rotea系统包括一台小巧的多功能仪器、一次性使用无菌试剂盒,以及直观、可视化、可定制程序的软件。它们共同构成了一个完整的系统,可提供出色的细胞回收率、灵活的输入和输出体积以及高效率处理能力。它是工作流程中许多过程的理想选择,包括细胞分离、浓缩、洗涤、缓冲液置换和冻存等。
● 低输出体积——通过专利技术可产出低至5 mL的浓缩物
● 处理灵活——用户可编程的软件可创建和优化广泛的细胞分离、洗涤和浓缩方案
● 优异的细胞回收率和活性——温和的流化床支持低剪切处理,可回收> 95%的细胞,同时还能保持细胞活性
● 实现科研到商业化生产的转化——封闭式一次性使用试剂盒可确保无菌化处理,OPC-UA接口可连接至符合21 CFR Part 11的系统

Gibco CTS Rotea逆流离心系统

长 按 扫 码
了解更多相关资料
Gibco CTS试剂现以灵活的BioProcess Container(BPC)形式提供,非常适合连接到封闭系统中。
● 无缝过渡——CTS细胞培养基和试剂现提供与封闭系统兼容的现货包装,从而帮助缩短产品的交付时间
● 用途广泛——通过内螺纹鲁尔连接器、MPC连接器或无菌焊接技术,这些试剂可以轻松整合到封闭生产系统中。产品所带有的PVC和/或C-Flex管套件与市场主导型无菌焊接设备兼容,可无菌地整合到细胞和基因疗法的生产工艺中
● 质量测试和支持文书——这些试剂和一次性技术均符合行业标准,并提供相应的法规文书和支持(药品主文件和/或法规支持文件,分析证书和原产地证书)。
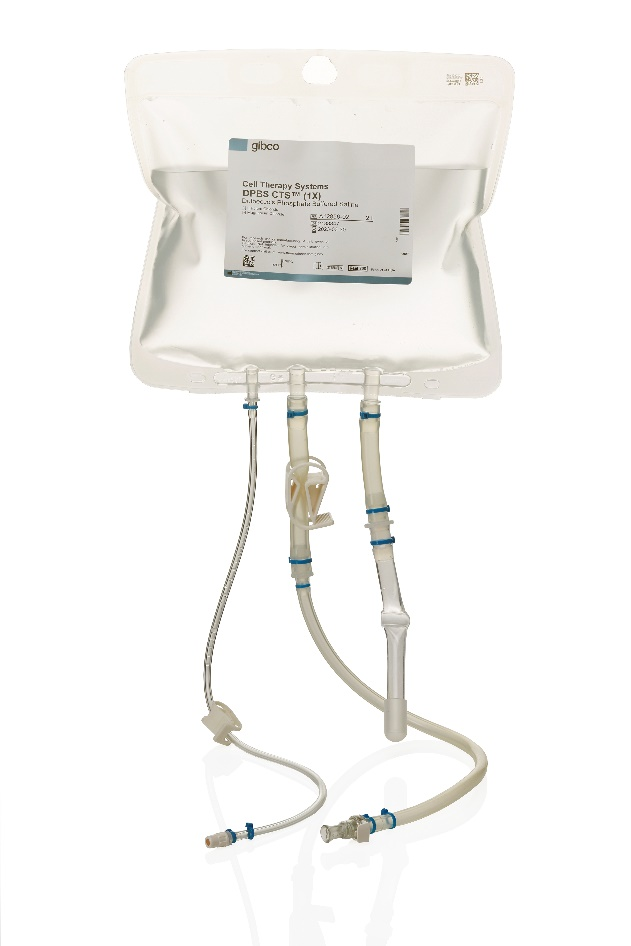
与封闭系统兼容的袋装培养基与试剂
细胞生产原材料的选择与鉴定
Gibco 细胞治疗系统(CTS)系列培养基与试剂
细胞治疗系统——临床级细胞治疗生产的可靠选择。CTS试剂提供专为细胞和基因治疗设计的GMP级产品,帮助开发商将研发成果顺利过渡到临床应用。
● cGMP生产——按照医疗器械的 cGMP 制造,FDA 注册,符合21 CFR 820
● 生产基地通过美国食品药品监督管理局FDA 和 ISO 13485 认证的质量管理体系注册
● 产品经过严格的QA测试,包括培养基和试剂的无菌性、内毒素和支原体测试
● 文档支持——可追溯性文档,包括分析证书、原产地证书和药品主文件(DMF)和/或法规支持文件(RSF)
● 经验证的应用——应用于FDA批准和EMA批准的CAR-T治疗以及首个FDA批准的治疗性癌症疫苗
● 应用于200多项临床试验
质量监控
高通量 Invitrogen 细胞活性/毒性分析试剂
Invitrogen™ Molecular Probes™ 荧光标记试剂专注荧光领域40多年,可提供多样化的检测方法,用于CAR-T细胞活性与活力、细胞毒性等功能分析,以荧光或比色法为基础,具有高灵敏度和便捷性,且已在多种仪器平台上验证,如显微镜、流式细胞仪、酶标仪以及高内涵筛选仪器等。
高通量 Invitrogen 细胞活性毒性分析试剂
Thermo Scientific™ 微孔板酶标仪
Thermo Scientific™酶标仪包含Varioskan LUX,Multiskan SkyHigh/Multiskan FC,Fluoroskan/Fluoroskan FL/Luminoskan,应用灵活、性能优异、简单易用,广泛适用于各类基于微孔板的实验。无论是光吸收,荧光(含FRET),化学发光(含BRET),时间分辨荧光(含TR-FRET)还是Alphascreen等,皆可满足使用需求。
● SkanIt软件兼容所有酶标仪,仪器控制和高级分析功能二合一
● SkanIt软件具有科研版和药研版(符合 FDA 21 CFR 第 11 部分所需功能)
● 使用远程控制接口,易于整合 LIMS 和自动化系统

Thermo Scientific™ 微孔板酶标仪
医麦课堂携手赛默飞,在2021年第2季度上线了“解码细胞免疫治疗,鼎力现在与未来”系列线上专题讲座,届时欢迎各位在线交流学习!第二期课程将在4月22日上线,由赛默飞世尔科技生命科学细胞生物学产品市场经理 刘爽,带来《从研发、工艺和质量监控谈细胞治疗生产的成功之路》的精彩分享。


点击下方“阅读全文”,获取免疫细胞治疗技术支持,更有机会赢取好礼!
12-13 Daria Thorp
分析仪器与应用行业产教融合共同体揭牌成立12-13
倒计时1天!传承40载·创新“谱”未来 40周年纪念活动即将开幕12-13 SHINE
GLMY创想仪器丨参加嘉禾铸造年会12-13 国产精密仪器厂家
ADC药物的CMC监管12-13 基泰生物
技术交流 ∣ 磁微粒化学发光技术12-12 BEAVER
EMMS用力肺功能检测系统——临床前动物肺功能检测的经典之作,呼吸系统研究的强大助手12-12 玉研仪器
免维护,易操作,多功能成像——LabRAM Soleil 拉曼成像仪12-12 HORIBA
【12月14日】华东理工大学邀您探索微观世界——显微红外与拉曼交流研讨会12-12 HORIBA
【环保专题】离子色谱在环境保护——水质中的应用12-12
英诺德INNOTEG Sampling Case气体采样器新品上线12-12 英诺德INNOTEG
赋能冻干技术革新 | 莱奥德创冻干工场—冻干服务实验室正式投入使用12-12 莱奥德创
专访第二期冻干技术分享会,解读行业创新密码12-12 市场部
倒计时2天!传承40载·创新“谱”未来 40周年纪念活动即将开幕12-12 SHINE
中国离子色谱40年《你好,传承者》系列访谈 | 中国地质大学(武汉)特任研究员——黄维雄12-12 SHINE
GLP-1,下一个风口12-12 基泰生物
快来get实验室女神同款涡旋仪!12-12
油脂氧化分析仪的十八般武艺 | 第一式:活性包装,保障食物品质和新鲜度!12-12
年底啦,你的护眼KPI达成了吗?12-11
蔡司光学郑重声明12-11