【First-in-class药设系列】识别CyclinE-CDK2变构位点的新策略及小分子发现
2024-10-22 11:13:11, 洪悦 & 张健 TargetMol中国
在人类基因组中,有超过50%编码蛋白的基因具有同源亚型,这些亚型具有相似的序列和结构。同源亚型蛋白在细胞中产生重叠功能有助于细胞系统的稳健性。尤其在癌症等病理条件下,许多同源亚型蛋白对细胞的存活至关重要。
近年来,发现许多仅在同源亚型蛋白中存在的半胱氨酸残基,通过与共价小分子探针的相互作用,能够帮助发现潜在的配体结合位点。然而,对于缺乏这种半胱氨酸残基的蛋白,这种方法难以奏效。
最近,来自Scripps研究所的研究人员提出“Paralog-hopping”策略来识别缺乏半胱氨酸的同源亚型蛋白中的新配体结合位点。为了验证这个策略,他们选择Cyclin同源亚型蛋白CCNE2(Cyclin E2)和CCNE1(Cyclin E1)(二者都通过与CDK2的结合,调控细胞顺利的通过G1期,进入S期)作为对象开展位点探索。
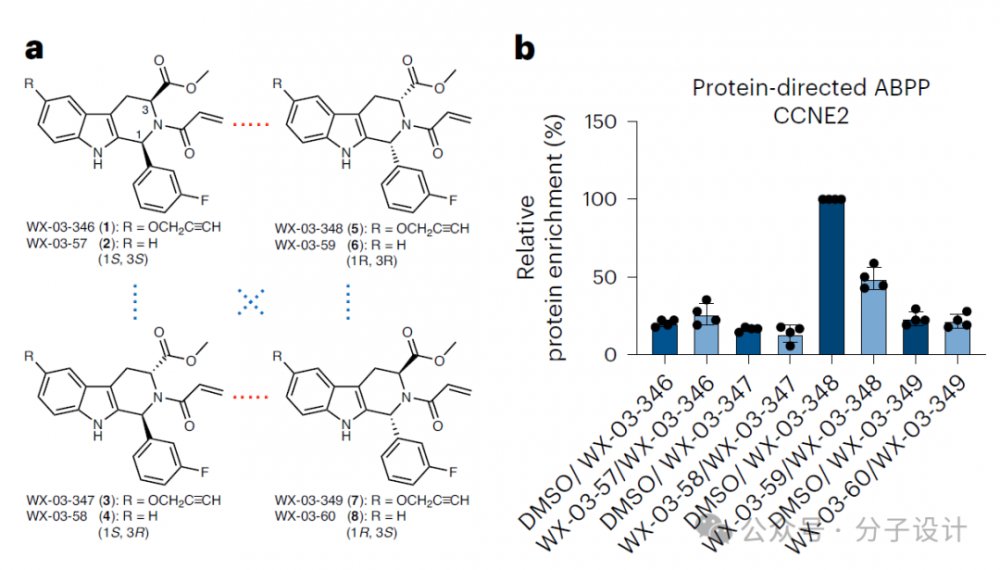
CCNE1和CCNE2都是肿瘤细胞生长所必需的基因,但相比之下,更多的肿瘤细胞对CCNE1的依赖性更强,尤其是在卵巢癌中。
研究人员基于前期发现的色氨酸丙烯酰胺(tryptoline acrylamide)立体探针在肿瘤细胞系中开展了ABPP(activity-based protein profiling)实验,结果表明(R,R)-WX-03-59和WX-03-348会与CCNE2的C109发生立体选择性的特异性反应,该半胱氨酸突变为CCNE2-C109A后,WX-03-348不再与突变体反应,表明CCNE2在C109附近具有可结合位点。
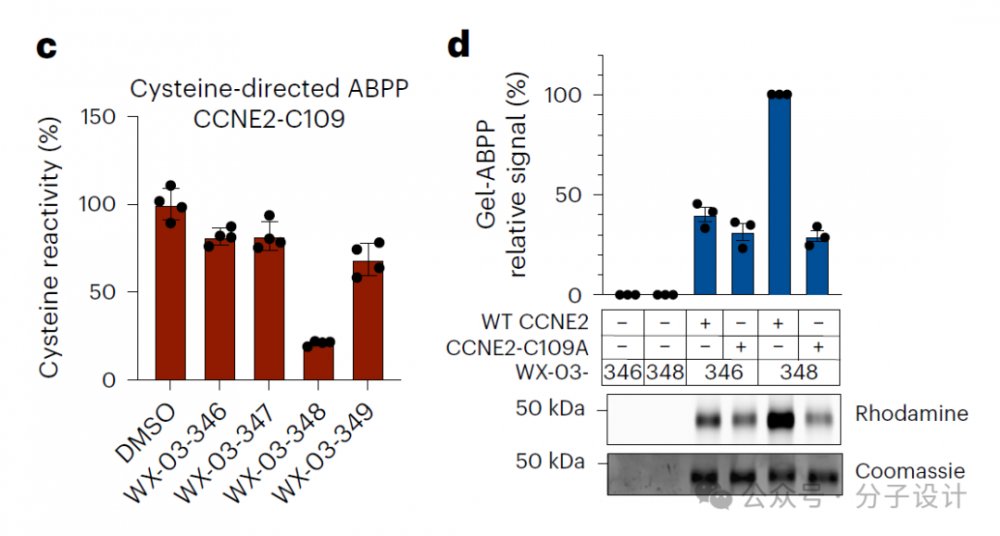
为了促进CCNE1:CDK2抑制剂的开发,研究人员对两者结构进行分析发现,CCNE2的C109位点在CCNE1中对应为N112。为了明确CCNE1是否也可能拥有在CCNE2-C109对应位置的结合位点。通过评估炔烃修饰的色氨酸丙烯酰胺的扩展文库与纯化的CCNE1:CDK2和CCNE1-N112C的反应性。
结果表明,WX-02-520优先与CCNE1-N112C反应,并可被WX-02-308阻断,表明CCNE1靠近N112和CCNE2靠近C109的位置均有小分子结合位点。

接下来,他们建立一种更高通量的测定法来筛选与CCNE1-N112C结合的小分子。首先合成了WX-02308的衍生物,在色氨酸核心的不同位置连接PEG3-甲酯连接基,通过GEL-ABPP实验,发现WX-02-588及其对映体WX-02-589在C3位的PEG3-甲酯修饰具有更好的立体选择性;随后将荧光染料偶联至这两种化合物,生成YZ-01-A和YZ-01-B;利用GEL-ABPP验证了YZ-01-A与纯化的CCNE1-N112C:CDK2复合物的立体选择性反应的程度比纯化的野生型CCNE1:CDK2复合物的程度大得多。
此外,他们还使用了NanoBRET(Nano Bioluminescence Resonance Energy Transfer)方法证实,YZ-01-A选择性地结合了CCNE1-N112C,但不结合野生型CCNE1。这表明NanoBRET和GEL-ABPP可用于精确评估化合物的靶标结合能力及抑制效果。


进一步,他们发现I-125A不影响ATP位点NanoBRET示踪剂K-10与CCNE1 N112C或野生型CCNE1复合物的结合,与ATP位点竞争性抑制剂dinaciclib观察到的完全抑制活性形成对比,表明I-125A和dinaciclib的作用机制不同。

尽管dinaciclib能阻断ATP结合位点的活性,它却不能影响YZ-01-A与CCNE1-N112C的相互作用,说明了YZ-01-A是通过不同于与ATP位点结合的方式与CCNE1-N112C复合物相互作用的。通过ABPP实验,发现探针WX-02-520在细胞中富集了约20种蛋白,其中6种蛋白(包括CCNE1-N112C)的立体选择性结合可被WX-02-308阻断。然而I-125A仅阻止了WX-02-520对CCNE1-N112C的富集,表明其高度选择性。

通过解析野生型CCNE1和CDK2与I-125A和I-198复合物的共晶结构,发现这些化合物的结合口袋位于CDK2的C叶和A环附近,远离ATP结合位点,靠近CCNE1的α1、α7和α8螺旋。这表明它们并非通过直接与ATP口袋结合起作用,而是通过一个更隐蔽的、位于变构位点的口袋发挥作用。I-125A,I-198与CDK2的关键相互作用包括R122侧链胍基与I-125A和I-198的环丙基酰胺羰基之间的氢键,T182主链酰胺与噻唑或吡唑氮原子之间的氢键,此外还有疏水性和溶剂介导的相互作用。这些相互作用进一步增强了化合物与蛋白质的结合稳定性。I-198 结合口袋在Apo CCNE1:CDK2 结构中大部分不存在,通过分析这个口袋是通过CCNE1的α7和α8螺旋之间的环的运动形成的,并且还涉及CCNE1的α8螺旋(残基L244-P266)和CDK2的A环(helixA)的结构调整。进而干扰了CDK2的磷酸化位点和底物肽结合,最终抑制CDK2活性。这一研究为理解变构小分子如何调节CDK2的活性提供了重要的机制见解。

通过ADP-Glo实验,他们测定这些化合物对激酶活性的抑制作用:使用RB1肽作为底物,实验结果表明I-125A作为CCNE1抑制剂比I-198更有效,两者的IC50值分别为0.13μM和0.75μM。对野生型CCNE1-CDK2复合物抑制的IC50分别为:17nM,0.35μM。使用另一种底物组蛋白H1测试时,发现I-125A和I-198的相对效力仍然相似。然而ATP位点CDK2抑制剂dinaciclib在这两个底物测定中都完全阻断了野生型CCNE1和CCNE1-N112C复合物的活性,表现出更强的抑制作用。

WX-02-308和WX-02-14是色氨酸丙烯酰胺类化合物,虽然它们能够在ABPP实验中完全结合N112C,但在底物测定中未表现出抑制CCNE1-N112C复合物的效果.研究还发现,I-125A和I-198对CCNE2复合物的激酶活性没有抑制作用,这进一步表明这些化合物具有特定的靶向性。研究人员试图进一步探索I-125A和I-198的细胞内活性。通过NanoBRET和纤维素GEL-ABPP实验测试,I-125A对CCNE1-N112C的TE50为1.0μM,I-198为10μM。

进一步,他们开发了一种新的高通量筛选(High throughput screening,HTS)法,用于识别与复合物中的变构位点结合的其他化合物。为了实现这一目标,他们对NanoBRET测定进行了改进,使用稳定性更好的底物vivazine,以维持约10小时的稳定发光信号。通过将反应时间延长至185分钟,获得了强烈的立体选择性BRET信号。优化后的测定法在170分钟内表现出良好的实验性能(Z''值为0.85,信噪比约为30)。研究验证了化合物I-125A和I-198与CCNE1-N112C的结合效力,并对324种大环化合物进行了初步筛选,成功重新发现I-125A作为命中配体。这证明了该筛选方法的有效性,并认为可以用于更大规模的HTS,以发现更多结合CCNE1变构位点的化学物质,为药物发现提供工具。
综上,本研究成功证明了 “Paralog-hopping” 策略的可行性。通过利用化学蛋白质组学中发现的亲电试剂-半胱氨酸相互作用,探索到蛋白质配体结合口袋,可以对不含半胱氨酸的同源亚型蛋白的对应活性口袋开发非共价配体。
Zhang Y, Liu Z, Hirschi M, et al. An allosteric cyclin E-CDK2 site mapped by paralog hopping with covalent probes[J]. Nature Chemical Biology, 2024: 1-12.
04-09 毕克气体
邀请函|新品亮相,国仪量子与您相约第35届中国化学会年会04-08 CIQTEK
培训通知|波谱校园行首站启航!华南师范大学站即将开启04-08 CIQTEK
邀请函|新品亮相,国仪量子与您相约中国晶体学会第三届陶瓷青年学术会议暨晶态复合材料研讨会04-08 CIQTEK
展会预告 | 赛恩科仪受邀参与第十届全国磁性材料与器件大会04-08 赛恩科仪
【颗粒攻略】破解高粘粉末检测难题:LS13320XR精准解析锰酸锂粒径分布,助力电池性能跃升04-08 小贝
贝克曼如何帮科学家快速找到答案——对话中国区总经理郝小龙04-08
Biomek i3自动化细胞转染DOE:提升准确性和重现性04-08 小贝
会议预告 | 贝克曼库尔特生命科学诚邀您参加2026分析超速离心技术交流会04-08
亮相ESIE2026|四方光电“复合感知+散热管理+过程控制”产品矩阵构建新能源全生命周期安全监测体系04-08 四方光电
【Biotage产品通讯】使用 Biotage® PhyPrep 自动化质粒纯化系统简化质粒制备流程04-08
5999元|Fluke ii01手机声学成像仪 4月13日全网开售04-08
领先发动机制造商的选择:两台ii1020C声学成像仪,两年就能回本04-08
限时促销|经典专业款TiS55+热像仪,备战零事故安全月!04-08
气密检漏仪及标准漏孔的校准方案介绍04-08
电机对中:您需要知道如何入门04-08
积分商城 | 3月积分兑换名单04-08
邀请函 | 新能源应用技术交流会-重庆/广州/深圳04-08
【直播预告】HJ 1444-2026标准解读与检测经验分享会来啦!04-07 北京博赛德
Cytiva思拓凡智服平台重磅上线:服务一键触达,体验全面升级04-07 为您服务的