细胞外靶向蛋白质降解:药物发现的新兴方式
2024-03-13 11:54:42, Untangled 上海氨探生物科技有限公司

近年来,细胞内靶向蛋白质降解(iTPD, intracellular targeted protein degradation)正成为新药研发的重要路径;区别于经典的“占位驱动”药物,iTPD往往通过循环催化的方式发挥作用,因而更持久、有效且剂量更低。

图1. iTPD类药物的靶标蛋白质降解原理(图片来源:Nat Rev Drug Discov.)
通过构建异双功能小分子,iTPD能够劫持细胞内的泛素化-蛋白酶体系统,同时招募靶蛋白(Protein of interest, POI)和E3连接酶,促使靶蛋白发生泛素化修饰并随后进入蛋白酶体降解(图1)。基于相似的原理,iTPD已衍生出包括Dual-PROTAC、photo-PROTAC等丰富的范式(图2),其中最主要的是蛋白水解靶向嵌合体(Proteolysis-targeting chimeras, PROTACs)与分子胶(molecular glues degraders, MGDs),目前已有几十项涉及PROTACs和MGDs的临床试验,其中一些已达到临床II期和III期阶段。iTPD的飞速发展启发了学界将类似的策略扩展到细胞外蛋白质组,即细胞外靶向蛋白质降解(eTPD, extracellular targeted protein degradation)。
细胞外靶向蛋白质降解
细胞外蛋白质组由分泌蛋白和膜结合蛋白组成,人类基因组中超过1/4的基因可编码分泌蛋白和膜结合蛋白(图2),二者是细胞和组织外部交流的枢纽,在许多生理和病理过程中都发挥着至关重要的作用。重要的分泌蛋白包括细胞因子、凝血因子、激素和生长因子,而膜蛋白包括离子通道、分子转运蛋白、酶、受体和其他锚定蛋白。

图2. 人类基因组中细胞外蛋白质的数量(图片来源:Science.)
针对细胞外蛋白质组的eTPD通常通过使用双特异性生物制剂或小分子,将 POI募集至膜结合再循环受体并运输至溶酶体,这是细胞外蛋白质降解的典型途径(图3)。与iTPD类似,eTPD类药物同样以不需要像传统占位型药物结合到活性或变构位点,理论上可以结合 POI 上的任何位置;其次,靶标的降解会去除整个蛋白质,包括其支架功能,因此药物的治疗活性能够持续更长时间,并且更接近基因敲除实验的表型;最后,eTPD类药物能够以亚化学剂量发挥催化循环作用。
与iTPD相比,eTPD类药物具有去除蛋白质聚集体、损坏多余细胞器、膜和细胞外蛋白质的潜力,补充了泛素-蛋白酶体系统无法靶向的底物范围;此外,iTPD系统主要依赖于Cereblon (CRBN)和Von Hippel–Lindau (VHL)两种E3连接酶降解体系,二者均缺乏组织特异性,如何选取合适的E3连接酶以开发具备组织特异性的iTPD分子仍是目前研发的热点之一;eTPD已经使用了多种降解器系统,为eTPD类药物的开发提供了更多的选择性和更高的组织特异性。

图3. 溶酶体降解途径(图片来源:Signal Transduct Target Ther.)
细胞外靶向蛋白质降解的常见种类
基于“清除抗体”降解可溶性POI
清除抗体(Sweeping antibodies)作为潜在的治疗方法,通过两种截然不同的工程化改造技术:通过改变抗原的pH依赖性或增强抗体Fc部分对Fc受体(FcR)的亲和力。
注射后,清除抗体会在血液循环中与靶标蛋白质结合。由此产生的免疫复合物通过胞吞作用或 Fc受体介导的内吞作用进入内皮细胞。在分拣内体(sorting endosome)中,pH 值从中性变为弱酸性(pH 值为 6),抗原从清除抗体中释放出来。被 FcRn 结合的清除抗体穿梭到细胞表面并在那里释放,而抗原则在溶酶体中降解。对FcRn进行多种不同的突变可以增强抗原-抗体复合物通过FcRn的主动内吞,从而导致抗原的高效降解。增强对Fc受体的亲和力使治疗性扫描抗体能够在内皮细胞和血浆之间进行有效循环,从而进一步清除循环中的抗原,形成“清除”效应。
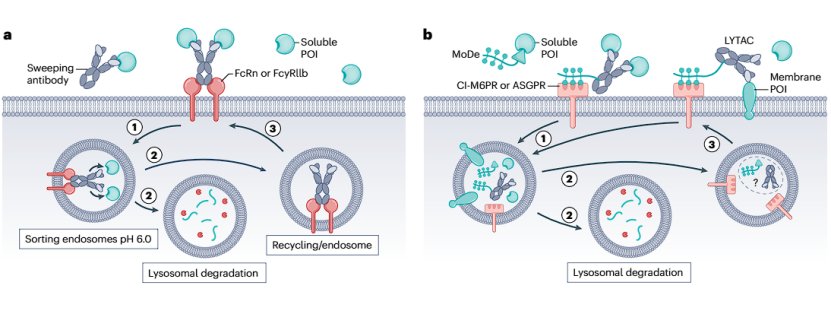
图4. 基于清除抗体(a)和基于聚糖(b)的eTPD (图片来源:Nat Rev Drug Discov.)

基于聚糖的循环受体eTPD
利用聚糖靶向回收受体,如阳离子非依赖性甘露糖6-磷酸受体(CI-M6PR)或脱唾液酸糖蛋白受体(ASGPR),促进膜和可溶性POI的溶酶体降解。一种方法涉及将CI-M6PR 的多个聚糖配体生物偶联到针对POI的特异性抗体上,形成一种被称为溶酶体靶向嵌合体(LYTAC)的构建物。LYTAC–POI复合物结合到CI-M6PR后,被内吞并导致POI在溶酶体中降解。利用类似的路径,通过将生物制剂以及双功能性小分子与ASGPR相结合,开发出了MoDE和ASGPR-targeting chimeras(ATACs)的降解手段。

基于跨膜 E3 连接酶实现膜蛋白的 eTPD
利用双特异性抗体开发跨膜E3连接酶,通过将其中一个抗体臂与E3连接酶的胞外结构域结合,另一个抗体臂与跨膜POI的胞外结构域结合,形成被称为基于抗体的蛋白水解靶向嵌合体(AbTACs)、蛋白水解靶向抗体(PROTABs)或通过E3泛素连接酶招募消除受体(REULR)。通过拉近降解器和 POI 的空间距离,实现 POI 细胞内结构域泛素化,引导其进入溶酶体或蛋白酶体降解。
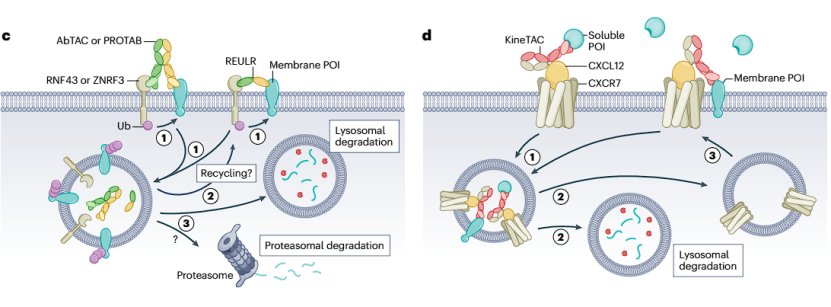
图5. 基于跨膜 E3 连接酶(c)和基于细胞因子和生长因子循环受体(d)的eTPD (图片来源:Nat Rev Drug Discov.)

基于细胞因子和生长因子循环受体实现膜蛋白的 eTPD
众所周知,许多细胞因子和白细胞介素可通过穿梭到溶酶体而被其受体吸收和降解。细胞因子受体靶向嵌合体(KineTACs)提供了另一个利用内源性机制进行 eTPD 的机会。KineTACs通过将双特异性抗体的一个抗体臂与天然细胞因子或生长因子结合,另一个抗体臂与 POI 结合,实现针对膜蛋白和可溶性蛋白质的降解。与 AbTACs 一样,KineTACs 也能降解多种细胞类型上的多种膜蛋白,但与 LYTACs 一样,它们也能降解可溶性蛋白,因为其循环不依赖于泛素化。

基于整合素的溶酶体降解
受利用整合素 αVβ3 靶向递送抗癌药物的配体递送系统的启发,研究人员开发了基于整合素的降解器系统。这些细胞粘附分子是细胞-细胞外基质连接的关键介质,在癌症模型中经常过度表达,能够与含有简单 Arg-Gly-Asp (RGD) 基序的配体结合,并将其转运至溶酶体,因此是极具吸引力的降解系统。类似的,通过使用一端结合整合素,一端结合POI的双特异性抗体,能够有效地将POI引导质溶酶体并实现降解;由于整合素在癌症中常见的过表达,为肿瘤选择性降解膜蛋白或可溶性蛋白提供了令人兴奋且相对尚未开发的潜力。

图6. 基于整合素(e)和基于PROTACs(f)的eTPD (图片来源:Nat Rev Drug Discov.)

基于PROTACs的膜蛋白降解
PROTACs通常被用于细胞内可溶性蛋白质的降解,但一些研究小组也利用含有与 CRBN 或 VHL 的经典 E3 连接酶结合剂的 PROTACs 靶向受体酪氨酸激酶(RTK),RTK通常是跨膜蛋白质,包含一个细胞外结构域、一个跨膜区域和一个细胞内激酶结构域。举例而言,C4 Therapeutics开发的EGFR小分子降解剂(L858R)CFT8919,已获得美国食品药品监督管理局(FDA)的研究新药批准。在跨膜蛋白质上的应用拓宽了PROTACs的适用范围。



eTPD领域尚处于初期阶段,但发展十分迅速,各种创新的降解策略和制剂方法层出不穷;尽管在eTPD的发展之路上仍有诸多问题亟待解决,包括但不限于其适用靶标、治疗领域、安全性、组织选择性、耐药机制等等,eTPD仍然展出了其独特的魅力和令人兴奋的前景,为细胞外蛋白质的特异性降解提供了全新的路径。
解构健康奥秘、探寻生命答案,氨探生物以一流的分子表型组平台和成熟的临床转化应用体系,为优秀的研究团队进行技术和数据赋能,致力于实现分子表型水平的精准诊疗。

04-09 毕克气体
邀请函|新品亮相,国仪量子与您相约第35届中国化学会年会04-08 CIQTEK
培训通知|波谱校园行首站启航!华南师范大学站即将开启04-08 CIQTEK
邀请函|新品亮相,国仪量子与您相约中国晶体学会第三届陶瓷青年学术会议暨晶态复合材料研讨会04-08 CIQTEK
展会预告 | 赛恩科仪受邀参与第十届全国磁性材料与器件大会04-08 赛恩科仪
【颗粒攻略】破解高粘粉末检测难题:LS13320XR精准解析锰酸锂粒径分布,助力电池性能跃升04-08 小贝
贝克曼如何帮科学家快速找到答案——对话中国区总经理郝小龙04-08
Biomek i3自动化细胞转染DOE:提升准确性和重现性04-08 小贝
会议预告 | 贝克曼库尔特生命科学诚邀您参加2026分析超速离心技术交流会04-08
亮相ESIE2026|四方光电“复合感知+散热管理+过程控制”产品矩阵构建新能源全生命周期安全监测体系04-08 四方光电
【Biotage产品通讯】使用 Biotage® PhyPrep 自动化质粒纯化系统简化质粒制备流程04-08
5999元|Fluke ii01手机声学成像仪 4月13日全网开售04-08
领先发动机制造商的选择:两台ii1020C声学成像仪,两年就能回本04-08
限时促销|经典专业款TiS55+热像仪,备战零事故安全月!04-08
气密检漏仪及标准漏孔的校准方案介绍04-08
电机对中:您需要知道如何入门04-08
积分商城 | 3月积分兑换名单04-08
邀请函 | 新能源应用技术交流会-重庆/广州/深圳04-08
【直播预告】HJ 1444-2026标准解读与检测经验分享会来啦!04-07 北京博赛德
Cytiva思拓凡智服平台重磅上线:服务一键触达,体验全面升级04-07 为您服务的