AAV滴度检测,耶拿可以做什么(上篇)——感染滴度检测
2022-07-15 16:39:13, 德国耶拿生命科学 德国耶拿分析仪器股份公司生命科学
基因治疗领域目前最常用病毒载体之一是腺相关病毒(AAV),以AAV作为载体开发基因治疗药物时,必须对多种关键质量属性进行检测,其中放行的最关键指标之一就是AAV病毒滴度测定,准确定量AAV载体病毒滴度对于临床前和临床剂量标准至关重要。
AAV病毒滴度通常分为物理滴度和感染滴度。
物理滴度一般是指基因组滴度或者衣壳滴度。通常采用qPCR或ELISA的方法进行检测。
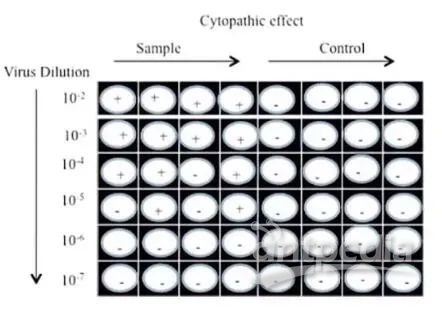
在感染滴度方面,AAV感染性滴度的金标准是采用TCID50细胞体外感染的方法。通常的实验流程是AAV样品通过梯度稀释,并在腺病毒的辅助作用下感染96孔板中携带rep和cap的靶细胞,通过qPCR扩增获取扩增信息从而判定感染的培养孔是否有阳性感染。通过起始滴度和基于病毒感染细胞的统计数值, 采用组织培养半数感染剂量公式—Spearman- Karber公式来评估感染滴度(也有其他计算公式,比如Reed-Muench Method、Improved Karber method等)。
目前AAV采用TCID50方法面临的挑战是精密度差,变异系数大,对于质量控制检验而言,放行标准更难以建立,日常工作的稳定性考察也有很大的困扰。
TCID50实验结果变异系数大是最难克服的挑战,通常文献发表的TCID50感染滴度结果%CV值>70%,很多因素都会影响检测结果。
一方面为了摸索更加稳定的放行标准,需要在诸如辅助病毒的稳定性、易感细胞的类型和接种浓度、培养液体积、培养的时间、后续检测体系筛选等等方面进行较多的条件摸索,工作量较大,对于QC方法开发的部门压力较大。另一方面体系建立以后,人员的培训熟练程度、实验室的背景污染、移液的精准度、流程重复完成的精确度等等都会影响检验结果,对于放行部门也有较大挑战。
耶拿自动移液工作站Felix可以在哪些方面提高TCID50方法的可重复性、稳定性?
AAV样品梯度稀释及分板:人工操作需要对每个AAV样品进行梯度稀释,在样品量较多时,工作量大,耶拿工作站Felix可以在这种重复工作中有效节约人工,并且完全在生物安全柜中完成,避免污染,同时通过仪器操作可以更好保证操作的一致性。梯度稀释后病毒样品需要再分装到4个或者更多复孔,也可以完全由工作站自动进行,提高重复性。
宿主细胞和腺病毒移液:如果涉及到整版或者较大工作量,可以通过工作站进行分板,同时进行多个96孔板移液,提高工作效率的同时,在生物安全柜中进行自动操作,避免实验室污染。
在方法开发过程中,需要摸索测试各种不同细胞系和培养液的量,使用Felix进行研发测试,由程序记录下具体过程,避免人工操作误差,可以及时追溯实验过程。
07-01 英斯特朗
连载 | 药物一致性评价与粒度分析(三)07-01 欧美克仪器
【仪器百科】LS-909丨干湿二合一激光粒度分析仪07-01 欧美克仪器
标准物质解决方案 | PFASs(全氟及多氟化合物)06-29
第九期阿尔塔有约 | 环境专题【新污染物:PFAS】技术研讨会精彩回顾及提问解答06-29
“绿色技术范式”,分析化学未来发展方向——访中国分析测试协会副理事长、辽宁省分析科学研究院原院长刘成雁教授06-29 转载仪器信息网
华西医院-标准型数显脑立体定位仪、双通道体温维持仪、体式显微镜安装完成06-29 迈越生物
科鉴检测助力2家仪器企业获得首批产品可靠性认证证书06-28 科鉴检测
德国耶拿:锂电池生命周期分析解决方案06-28 德国耶拿
AI已来!生命科学本科教学如何紧跟技术浪潮06-28 Opentrons
盛瀚售后,五星级服务的秘诀是什么?06-28 SHINE
专为汽车制造商打造的柔性解决方案——实现制程控制06-28
西北工业大学-脑立体定位仪安装完成06-28 迈越生物
会议邀请 | 第九届海上检验医师论坛06-28
卓立要闻 | 创新发展ing…6月卓立“大事小情”速览06-28 光电行业都会关注
打造信任合作伙伴!2024年度卓立汉光客户满意度调查开启06-28 光电行业都会关注
如何挑选适用于三阶光学非线性的测量系统?Z扫描测量系统来助力!06-28 光电行业都会关注
招聘启事—中国科学院沈阳自动化研究所微纳光学测量表征技术课题组06-28 光电行业都会关注
谱育科技作为主要完成方 荣获2023年度国家科学技术进步一等奖和二等奖06-28 点击关注→
仪器原理丨顶空仪与吹扫捕集仪科普小知识06-28 天美色谱