一觉解“千愁”,NUCLEIC ACIDS RES | MazF毒素蛋白诱导病原菌休眠,产生抗生素耐受
2021-04-26 16:25:54, 景杰学术 杭州景杰生物科技股份有限公司

景杰学术|报道
题目:MazF toxin causes alterations in Staphylococcus aureus transcriptome, translatome and proteome that underlie bacterial dormancy
发表时间:2021年2月
期刊:Nucleic Acids Research (IF=11.501)
作者及单位:日内瓦大学医学院
主要结论:MazF毒素蛋白通过调控细胞变化导致细菌休眠,从而使金黄色葡萄球菌产生耐药性。
关键词:金黄色葡萄球菌、休眠机制、耐药机制
金黄色葡萄球菌(Staphylococcus aureus,S. aureus)为一种常见的食源性致病微生物,世界上约有三分之一的人口感染,可以导致各种疾病。抗生素治疗是现代医学用于对抗细菌感染的主要方法之一,但随着耐药病原菌的出现,抗生素的作用受到破坏。有研究报道细菌可以不通过基因突变的方式,自身进入非生长的静止或休眠状态,降低细胞代谢,抵抗抗生素的作用。细菌毒素-抗毒素系统(TASs)在细菌中普遍存在,被认为是形成细胞休眠的主要因素,但该过程中的作用和机制尚不清楚。
MazEF是S. aureus金黄色葡萄球菌中的Ⅱ型TAS,由两种蛋白质组成:稳定的毒素蛋白MazF和不稳定的抗毒素蛋白MazE。MazF在大肠杆菌中被广泛研究,被证明能阻止蛋白质合成,并参与可逆的生长抑制、药物耐受和持久性的产生,对S. aureus 金黄色葡萄球菌MazF知之甚少。最近研究发现MazF促进了S. aureus金黄色葡萄球菌生物膜的抗生素耐受性,导致急性感染向慢性感染过渡。有人认为MazF不仅使细菌对抗生素更具耐受性,而且使细菌对宿主更具耐受性。因此,MazEF系统可能是S. aureus金黄色葡萄球菌耐药性和抗生素耐受性的重要因素之一。
近日,来自日内瓦大学医学院的研究团队在Nucleic Acids Research上发表了最新研究,运用蛋白质组学等多组学联合分析,揭示了MazF毒素蛋白通过调控细胞变化导致细菌休眠,从而使金黄色葡萄球菌产生耐药性机制。
Graphical Abstract
1
MazF诱导对S. aureus转录组和翻译组的影响
MazF是一种内切核糖核酸酶,优先切割UACAU位点的mRNAs。为探究MazF毒素蛋白对细胞生理的影响机制,研究人员首先通过RNA-Seq和Ribo-Seq分析了MazF诱导对金黄色葡萄球菌转录组和翻译组的影响。结果显示,在MazF诱导后,导致RNA和Ribo-Seq的转录物减少约50%,绝大多数基因的表达显著下调。约有17%的转录物增加,这表明一些转录途径上调。MazF表达导致核糖体休眠,这些核糖体分离出来并以二聚体的形式存在。切割后的转录本属于许多不同的基因家族,没有任何显著的富集。研究人员推测,MazF能切割广泛的mRNAs(而不是某一类),影响整个转录组和翻译组,引起细胞代谢的整体变化。并且这种调控不会导致完全的抑制,而是导致翻译程序的改变,从而为细胞的长期生存做好准备。
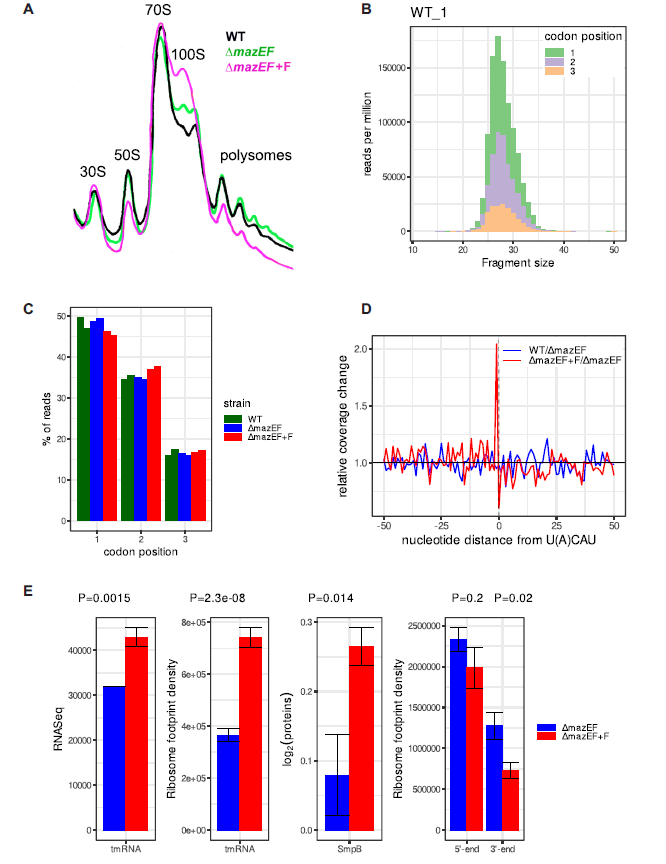
图. MazF诱导对S. aureus翻译组的影响
2
转录组、翻译组与蛋白质组间的相关性
Ribo-Seq中核糖体保护的mRNA片段(RPFs,ribosome-protected mRNA fragments)数量的变化与翻译的变化相对应,并且比RNA-Seq更直接地与蛋白质水平的变化相关。然而,翻译的改变并不一定意味着翻译蛋白质丰度的改变,翻译同时受到其他因素的影响,这些因素可能会影响蛋白质的产生,例如,共翻译因子或伴侣的存在有助于新生链的折叠。因此,必须分析RNA-Seq、Ribo-Seq与定量蛋白质组学数据之间的关系。
研究人员进一步通过基于TMT标记的串联质谱方法,分析了在MazF诱导下S. aureus的蛋白质组学,并且整合了RNA-Seq,Ribo-Seq和蛋白质组学数据,分析三者之间的相关性。结果表明,敲除mazEF引起的差异不明显,而添加mazF诱导使大量基因表达下调,表明MazF可能发挥核糖核酸内切酶活性,剪切RNA,抑制其转录和翻译。这些被MazF切割的转录物(以黑点标记)主要与基因表达的各个阶段(转录、翻译和蛋白质生产)下调的基因相关。
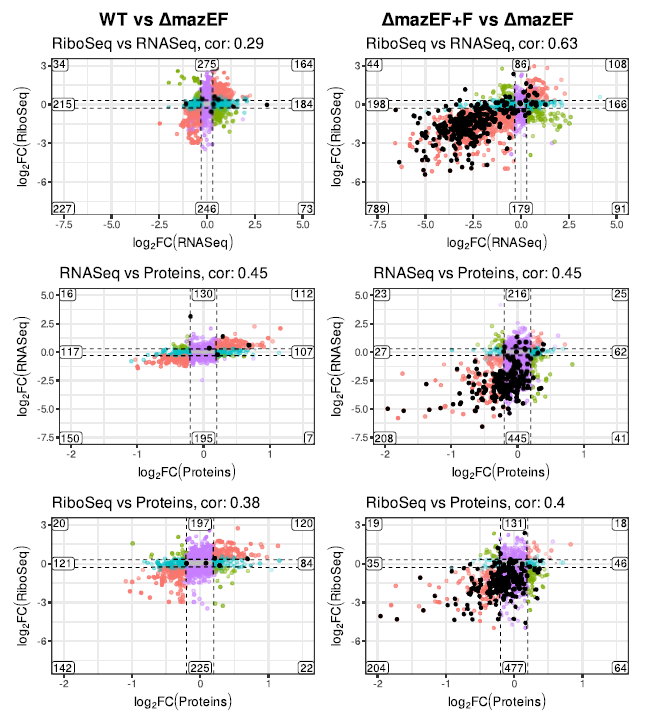
图. 蛋白质组学与RNA-seq、Ribo-Seq的相关性
值得一提的是,转录物丰度(RNA-Seq)和蛋白质合成率(Ribo-Seq)的定量数据使我们能够推断相对翻译效率(TE)。该研究的数据表明,TE的变化与蛋白质的相关性非常低,甚至是反相关性,即在转录减少的情况下蛋白质增加。因此,用这种方法计算的TE不能完全解释蛋白质丰度。事实上,TE取决于许多因素,如密码子使用、tRNAs的可用性、序列依赖性决定因素(如Shine-Dalgarno序列)和mRNA二级结构。这也提示我们蛋白质组学对蛋白质丰度变化进行系统分析的必要性。
3
MazF影响特定信号通路
研究揭示了MazF可能激活的三种途径,即翻译拯救和共翻译质量控制、核糖体休眠和再循环以及细胞分裂和细胞壁增厚。这些途径的激活可能导致可逆的细菌休眠,这使细胞能够在不利的生长条件下生存。
A、翻译拯救和共翻译质量控制:MazF诱导过程中,MazF激活了共翻译质量控制机制,包括SsrA系统和ATP依赖的分子伴侣,从而恢复蛋白质合成,以维持休眠时的细胞存活,并可能促进随后从休眠状态的退出。
B、核糖体冬眠和循环:研究观测到,MazF抑制负责翻译、tRNA氨基酰化、核糖体分解的要素和冬眠促进因子Hpf。如核糖体循环因子(Rrf,也称为Frr)和延伸因子G(EF-G,也称为FusA)等。MazF抑制翻译主要作用于翻译水平和核糖体休眠因子,而不是核糖体蛋白。这种机制允许细胞快速减少翻译,但也可以在需要时快速重启,例如从休眠状态退出。
C、细胞分裂和细胞壁增厚:MazF影响许多参与细胞壁生物合成的基因的翻译和蛋白质水平,如ADI途径基因arcRCDBA的翻译显著增加,ADI途径的上调与氨的升高和Glm途径的激活有关,最终导致细胞壁增厚。MazF表达改变的另一个途径是嘌呤和嘧啶的生物合成以及与之相连的途径,增加的嘌呤生物合成可能需要维持一定水平的ATP生产,以满足细胞壁合成的需要。
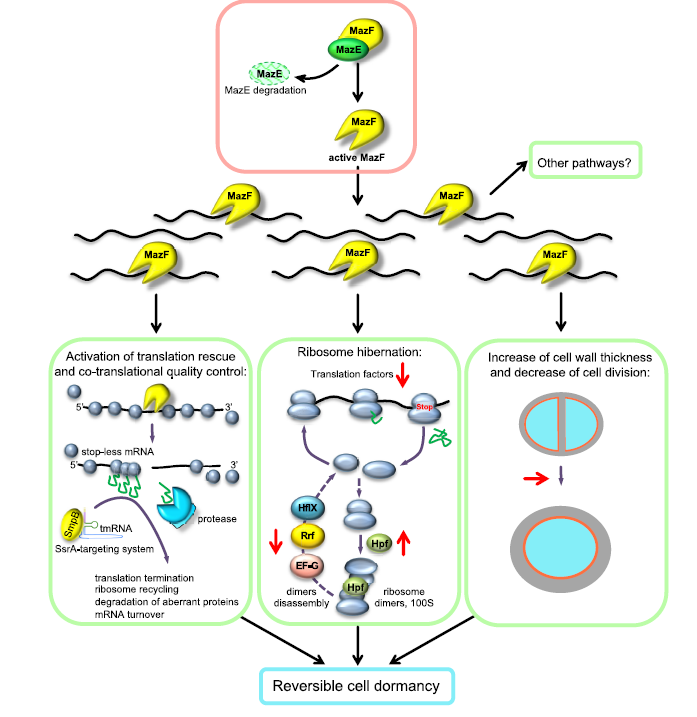
图. MazF对细胞生理的影响模型
了解休眠的原因对于抗生素耐药性的管理至关重要。目前,尚不清楚有多少不同的机制最终导致金黄色葡萄球菌休眠。本研究通过蛋白质组学为核心的多维组学方法,分析了S. aureus中MazF引起的转录组、翻译组和蛋白质组的变化,助于更全面地了解MazF毒素之间的联系及其与休眠的关系。
研究结果揭示了环境应激(如抗生素)条件下,MazF通过调节细胞变化导致休眠(而不是死亡)的机制。MazF通过切割mRNA直接降低翻译效率,通过减少翻译因子和促进核糖体休眠间接降低翻译效率。并鉴定到在MazF诱导的早期阶段(处理10min)受影响的重要途径:MazF可以增加细胞壁厚度且减少细胞分裂;MazF可以激活SsrA系统,拯救由于MazF切割mRNA而出现的核糖体停滞。这些途径有可能成为新型抗菌药物的靶点,以防止细菌休眠。
更多阅读
mSystems | 医科院皮肤病研究所首次揭示白念珠菌中巴豆酰化修饰的生物学角色
2021-02-09
新晋诺奖得主团队新成果,蛋白组学描绘肠道病毒切割宿主细胞蛋白组全景变化
2020-10-14

Nat Comm | 蛋白质组学和磷酸化修饰组学揭示肠道病毒感染宿主的动态调控
2020-09-09

东北大学丁辰团队揭示乙酰化修饰在人类真菌病原体毒力中的关键作用
2019-05-22

新进展!中国学者运用蛋白质组学发现人类新型抗艾滋病毒蛋白
2019-03-13
参考文献
1. Bezrukov F, et al. 2021. MazF toxin causes alterations in Staphylococcus aureus transcriptome, translatome and proteome that underlie bacterial dormancy. Nucleic Acids Res.
本文由景杰学术团队报道,欢迎转发到朋友圈。如有转载、投稿等其他合作需求,请文章下方留言,或添加微信ptm-market咨询。
#关注领取新人福利,下载最近三年影响因子(后台发送关键词“新人”)
06-27
大盘取厚势 落子开新局:战略聚焦开启品牌发展新篇章——访Veralto大中华区总裁秦晓培06-27 星羽
实验操作 | 质粒构建、转化、提取、鉴定、转染、测定(完整版)06-27 小 M
有投必奖 | 大家都用 MCE 产品做了啥? (感染领域)06-27 小 M
科研助攻 | 一文讲清:如何破解 PPI 靶点成药难题06-27 小 M
干货分享 | 谈谈天然产物的改构策略06-27 小 M
玉研口鼻暴露系统 | 精准、可控、高通量的动物肺部疾病造模工具,助力创新药物研发06-26 玉研仪器
医药行业指南:电位滴定仪选型攻略来啦~06-26
屹路同行 悦启新程06-26 屹尧科技
徕卡精准空间生物学解决方案 第四弹06-26 童昕、南希
【直播预告】第一届大湾区生物电镜制样讲习班06-26 徕卡显微系统
徕卡常规显微镜历经严苛的ISO9022标准测试06-26 徕卡显微系统
Viventis LS2 Live 光片显微镜发布会06-26 徕卡显微系统
前沿应用 | 经皮无创血糖检测中葡萄糖拉曼峰直接观测06-26 鉴知技术
SNEC光伏展圆满落幕 | OTT HydroMet闪耀时刻精彩回顾06-26 OTT HydroMet
激光指向稳定在光刻系统应用中的关键作用,及其优化方案!06-26 圈内人都会关注
推陈出新!通微公司携新品亮相本届CPHI06-26 Unimicro
远离氟污染!开启无氟接触前处理技术新篇章06-26
浑然一体的ChemiSEM技术:集成式扫描电镜成像与 X 射线能谱解决方案06-26
荧光计 VS 分光光度计,倒底怎么选?06-25