面包酵母快速质检 | FlowRACS 新应用
2026-02-11 10:36:03, 小赛 青岛星赛生物科技有限公司
FlowRACS
面包酵母快速质检
抗冻性能分析
自动化、高通量的单细胞技术

市场上面包酵母产品琳琅满目,质量却参差不齐。
海藻糖的SCRS采集:制备梯度浓度的海藻糖标准溶液,取适量溶液置于载玻片上,在与采集酵母细胞SCRS相同的条件下进行单细胞拉曼光谱表征。
以 1130 cm-1处的峰面积为 y 轴,海藻糖浓度为 x 轴,建立海藻糖的拉曼标准曲线,因为峰面积比峰高更能准确地定量物质。使用R软件获取酵母细胞的平均 SCRS。将平均 SCRS 与拉曼标准曲线相关联,实现对酵母细胞内海藻糖含量的定量分析。
通过分析酵母细胞的SCRS,获得MAL值,进而评估酵母单细胞的代谢活力。具有高MAL的细胞具有高效的代谢过程,表明在利用D2O方面效率更高,因此具有更高的C-D峰。

研究人员从市场上购买广泛使用的酵母产品,获得了8种面包酵母菌株(菌株A-H),其中菌株A-D从商业化低糖酵母产品中分离获得,菌株E-H从商业化高糖酵母产品中分离获得。
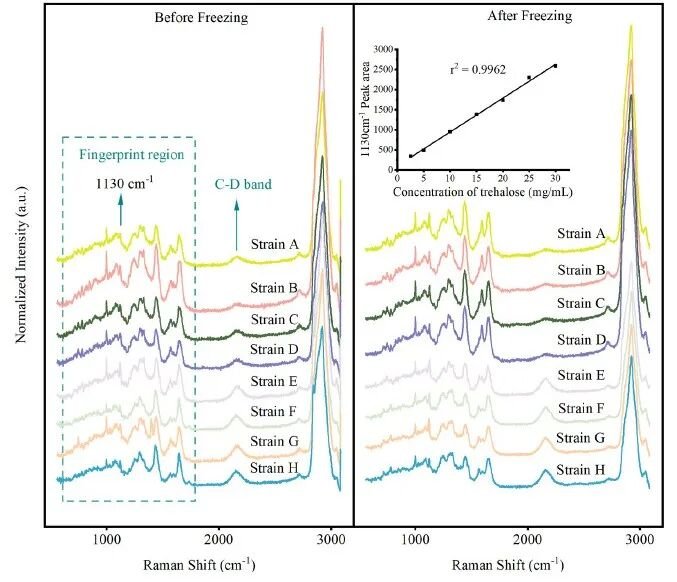
图1 八种酵母细胞冷冻前和冷冻后的单细胞拉曼光谱(SCRS)
将冷冻前后的酵母菌株分别置于含D2O的培养基中孵育,每组菌株采集120-150条SCRS,海藻糖在1130 cm-1处显示出一个强峰,冷冻后的SCRS中海藻糖标准曲线显示海藻糖特征峰面积与海藻糖浓度存在线性相关(图1)。由于细胞对D2O的利用,在2000-2300 cm-1出现C-D峰,可用于量化酵母细胞的代谢活性。
将冷冻前后的菌株分别置于含D2O的培养基中,不同发酵时间点取样检测,结果发现,随着发酵时间的增加,低糖酵母菌株的细胞活性呈上升趋势(图2A-D),而高糖酵母菌株则呈下降(图2E-H)。拉曼光谱法检测细胞活性的结果与传统方法(平板菌落计数法)高度相关,所有菌株显示出高皮尔逊相关系数(r > 0.9)。

图2 传统方法(TM)和拉曼方法(RM)测量冷冻前和冷冻后(F)酵母细胞的代谢活性
值得注意的是,与传统的标准平板菌落计数法相比,拉曼方法的细胞活性结果比传统方法高出10-20%。这归因于拉曼方法是在单细胞水平上检测细胞活性,可识别低代谢活性的酵母细胞,而这些细胞无法通过传统方法检测到。因此,拉曼方法在测量酵母细胞活性方面具有高灵敏度和准确性的优势,能够准确分析和评估酵母的发酵性能。
分别使用拉曼方法和传统方法(蒽酮-硫酸法)测量八种酵母菌株在冷冻前后细胞内海藻糖含量和冷冻保存存活率。结果显示,每种酵母菌株胞内海藻糖的含量在冷冻后普遍增加,表明细胞通过内源性海藻糖合成来抵抗外部压力。

图3 传统方法(TM)和拉曼方法(RM)测量冷冻前和冷冻后(F)酵母细胞的胞内海藻糖含量、冷冻存活率
具体而言,高糖酵母菌株的冷冻耐受性要高于低糖酵母菌株,菌株A的胞内海藻糖含量最高为40.1 mg/g(图3A),菌株E的胞内海藻糖含量最高为139.5 mg/g(图3E),且高糖酵母菌株的冷冻保存存活率通常高于低糖酵母菌株,该结果与细胞活性一致。拉曼方法与传统方法在评估胞内海藻糖含量方面显示出高度相关性,证明拉曼方法的可行性和可信度。
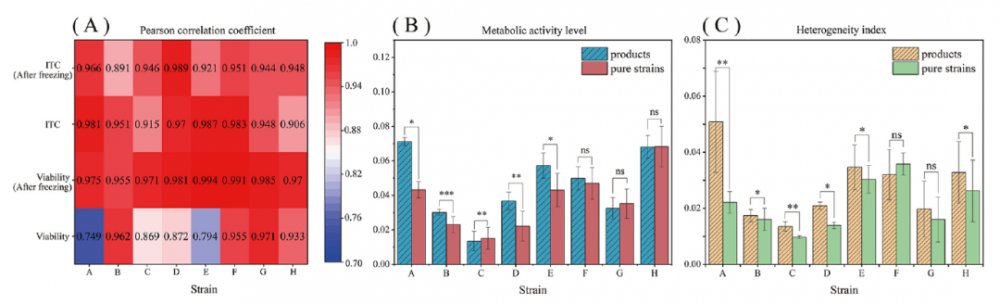
如图4D所示,在冷冻前,低糖酵母中菌株A显示出最高的MAL,表明具有最高的细胞活力,而菌株B最低;高糖酵母中菌株G的MAL最低,与传统方法的结果一致。值得注意的是,传统方法显示菌株H与其他菌株发酵能力差异较小,而拉曼法则显示其具有更高的MAL,表明菌株H的发酵能力未被传统方法识别。

本研究利用SCRS技术,建立了一种具有单细胞精度的面包酵母快速、精准评估方法。该技术通过重水孵育面包酵母细胞,根据SCRS的重水峰强度,实现了对单个酵母细胞代谢活性和细胞活力的量化分析,与传统方法相比具有更高的敏感性和准确性;根据SCRS中指纹区特征峰的分析,实现了对酵母细胞中海藻糖含量的定量检测,这一指标是衡量酵母细胞抗冻性能的关键,为耐寒酵母菌株的高效分辨及筛选提供了强有力的支撑。利用这一特点,研究人员可以进一步筛选出具有目标代谢水平和海藻糖含量的单细胞,并对其进行基因组测序或进一步培养,从而更有效地筛选培养出更有利于酵母产业发展的菌株。






02-10 安淼
手慢无!飞诺美球仔专属红包封面,2026「球」好运!02-10 市场部
春立万象新,丹纳赫中国区集团总裁彭阳给您拜个早年!02-10
马跃春晖,骐骥贺岁 | 与安捷伦开启万象新春祝福02-10
PFAS 知识狂飙赛,速来闯关赢大奖!02-10 安捷伦科技
安捷伦官方认证翻新仪器以租代售,助实验一马当先!02-10 安捷伦科技
重磅发布!SCIEX创新整合Echo® MS+与ZenoTOF 8600,实现高通量筛选灵敏度飙升02-10 SCIEX
徐医团队首篇Cell|看MST技术如何锁定肿瘤免疫逃逸关键互作机制02-10 丁浩
2026春节期间发货安排02-10 NanoTemper
春节放假前必看!真空离心浓缩仪“假期保养指南”02-09 吉艾姆离心浓缩
马踏春风至,佳节共团圆|2026春节放假通知02-09 吉艾姆离心浓缩
华仪宁创2026春节备货通知02-09
免费领取|这份 “马” 上暴富的红包封面,手慢无!02-06 Opentrons
24个精选真实故事,25年的最好工作搭档!02-06
精准赋能实验室智能化,阿斯曼尔全自动液体工作站解锁高效实验新范式02-06 ASHMAR
官宣!飞诺美首席“科研搭子”球仔,正式入驻小红书!02-06 市场部
QATM 奥德镁 | 全自动磨抛方案拉满球墨铸铁金相检测效率——Qpol 300 BOT 全自动研磨抛光系统02-06 弗尔德仪器
实验室选柱不踩坑!珀金埃尔默推出国产气相色谱柱,性能与性价比双在线02-05 珀金埃尔默
Pyris™ STA 9在药物分子研发中的应用--事半功倍,精准可靠02-05 珀金埃尔默
根据ASTM D6370使用珀金埃尔默Pyris™ TGA 9热重分析仪分析轮胎橡胶02-05 珀金埃尔默




