吉凯助力! 中山大学肿瘤防治中心陈明教授团队揭示PI3K/AKT通路激活可能是小细胞肺癌放化疗耐药的潜在机制
2022-10-12 12:26:44, ShanR 上海吉凯基因医学科技股份有限公司
小细胞肺癌(SCLC)占肺癌的13%至15%,估计全世界有25万癌症死亡。虽然小细胞肺癌最初对化疗和放疗高度敏感,但治疗耐药性的发展基本上是普遍的。由于在治疗后缺乏有效的后续治疗方法,导致治疗失败。因此,迫切需要阐明小细胞肺癌耐药的机制。
中山大学肿瘤防治中心陈明教授团队通过比较治疗敏感和耐药SCLC肿瘤样本的基因型和表型,研究了SCLC的治疗耐药机制,研究表明PI3K/AKT通路激活可能是小细胞肺癌治疗耐药的潜在机制之一。这一发现值得进一步研究,并为逆转化疗/放疗耐药性提供了一种可能的方法。相关研究结果以“Activation of PI3K/AKT Pathway Is a Potential Mechanism of Treatment Resistance in Small Cell Lung Cancer“为题发表在了Clinical cancer research期刊上(IF:13.801)。吉凯基因提供了本文FFPE样本的label free蛋白质组学服务。


研究方法

对11例接受CCRT治疗配对的LS-SCLC初发和复发时的肿瘤样本进行WES分析,观察到放化疗后的基因组变化富集在PI3K/AKT通路及存在克隆进化。公开数据库及独立ES-SCLC队列的FFPE蛋白质组学进一步证实化疗耐药与PI3K/AKT通路的激活有关,并进一步通过体外实验证实化疗耐药细胞株对PI3K抑制剂敏感,有望成为逆转化疗/放疗耐药性的潜在治疗靶点。

研究结果

1. 初治与复发SCLC肿瘤的基因突变情况
研究者收集了11例接受CCRT治疗的局限期小细胞肺癌(LS-SCLC)治疗初期及复发的肿瘤组织样本,共鉴定出4824个非沉默体细胞突变,包括SNV和indel,每个样本的变体中位数为216个。结果表明,TP53和RB1的改变是原发性和复发性SCLC的突变特征。在该SCLC队列中也发现了其他SCLC中的频繁突变癌基因(24个)及先前报道在介导SCLC细胞系或其他恶性肿瘤的化疗或放疗抵抗中起着关键作用的多个突变基因。

2. 放化疗后的基因组变化富集在PI3K/AKT通路
研究团队比较了治疗初期与复发SCLC肿瘤的基因组特征,以确定与CCRT后复发相关的基因组特征。在所有患者的2827个突变中,基线和复发样本共同拥有1997个突变(71%),与非小细胞肺癌相似,但明显高于乳腺癌和结直肠癌。复发肿瘤中发现了平均94%的治疗初期的肿瘤突变。

最常见的复发特异性突变基因为RB1、PCLO、DNAH5、PRUNE2、SYNE1和TACC2。这些获得性改变涉及多种途径,尤其是PI3K/AKT途径。11名患者中有8名患者的PI3K/AKT信号通路中富含20个获得性突变的基因,其中16个基因位于该通路上游。

3. 放疗下SCLC的克隆进化
接下来,研究团队通过PyClone推断治疗初期和复发SCLC肿瘤的亚克隆结构,以描述放化疗下的克隆进化。有趣的是,大多数共享突变(95%)显示复发肿瘤的癌细胞分数(CCF)增加,包括714个突变CCF增加超过20%。此外,复发样本中克隆的数量也显著高于治疗初始样本,表明CCRT后出现新克隆。总的来说,治疗初期肿瘤中的主要克隆在复发肿瘤中表现为主要克隆或次要克隆。
根据治疗初期和复发肿瘤中克隆结构的变化,确定了两种进化模式。第一种模式显示,治疗初期和复发肿瘤(患者N04、N05、N06、N07、N09和N10)中的主要克隆持续存在。第二种模式的特点是初治肿瘤的主要克隆减弱,然后继续演变为两种进化模式。具体而言,患者N01、N03和N11在治疗初期肿瘤中一些次要克隆发展为复发肿瘤中的主要克隆。另一方面,患者N02和N08表现出新克隆的出现和快速扩展,成为复发性肿瘤的主要克隆。有趣的是,与模式1相比,模式2与更长的PFS相关。

4. 独立的SCLC患者队列和公共数据集验证难治性SCLC中PI3K/AKT通路的激活
由于对与小细胞肺癌治疗后复发相关的PI3K/AKT通路激活特别感兴趣,研究团队试图在另外的患者样本以及公开的小细胞肺癌数据集中验证这些发现。
(1)首先,对另外9名接受CCRT治疗的LS-SCLC患者的初始诊断和复发时的1021个癌症相关基因(cfDNA)进行靶向测序。复发样本56个基因携带获得性突变或增加的CCF,也都富集在PI3K/AKT信号通路。(图A)
(2)第二组独立的28个化疗耐药和23个化疗敏感的ES-SCLC的FFPE样本。Label free蛋白质组学(由吉凯基因提供)被用于鉴定化疗耐药和化疗敏感性SCLC之间差异表达的蛋白质,KEGG途径富集分析表明,具有差异上调蛋白的基因(倍数变化>1.2)在WNT信号途径、RNA降解、嘌呤代谢和HIF-1信号途径中富集。由于PI3K/AKT通路在维持HIF-1a在各种恶性肿瘤中的转录、翻译和生物活性方面发挥着关键作用,重新标记了62个PI3K/AKT信号通路基因,并从WES队列中确定了拷贝数增加。有趣的是,HIF-1途径涉及7个基因(AKT1、AKT3、BCL2、IL6R、PIK3CA、PIK3CB和RPS6),其中6个位于HIF-1上游。(图B&C)

(3)一项12对治疗初期与复发肿瘤的WES公开数据,分析发现882个基因携带复发肿瘤的获得性突变,这些突变也富含PI3K/AKT信号通路。基于公共数据库的具有不同治疗反应的SCLC细胞系的转录组数据,GSEA差异表达通路分析显示,PI3K/AKT通路和HIF-1通路在顺铂耐药但对PI3K抑制剂敏感的细胞中显著上调。
5. 体外验证PI3K/AKT通路激活功能与小细胞肺癌治疗耐药相关
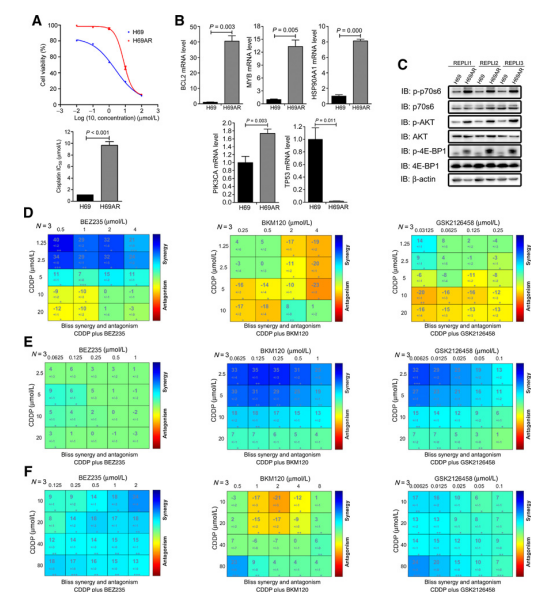
研究者进一步尝试用一对化疗敏感(H69)和化疗耐药(H69AR)SCLC细胞系验证PI3K/AKT通路在小细胞肺癌治疗耐药性发展中的作用。首先评估了14个携带获得性CNV基因的表达。与CNV分析一致,具有拷贝数增加的MYB、PI3KCA、HSP90AA1和BCL2上调,而具有拷贝数丢失的TP53在耐药H69AR细胞中下调。此外,western blot评估PI3K/AKT途径中的总蛋白以及关键基因的磷酸化形式,结果表明耐药H69AR细胞中AKT及其下游靶点4EBP-1和p70S6的磷酸化增加。最后,对顺铂联合或不联合PI3K抑制剂处理的H69AR、DMS53和H446细胞进行了细胞活力测定。结果表明,顺铂与几种PI3K抑制剂(包括BEZ235、BKM120和GSK2126458)之间存在协同效应。

研究结论

WES分析表明LS-SCLC复发时,PI3K/AKT信号通路中的基因因获得性体细胞突变或高频获得性CNV而富集。ES-SCLC队列中差异蛋白的通路分析显示HIF-1信号通路富集,并且62个含有获得性体细胞拷贝数扩增的PI3K/AKT途径基因中有7个在HIF-1途径中富集。独立的SCLC患者队列和公共数据集证实化疗耐药SCLC细胞系中PI3K/AKT和HIF-1通路上调。此外,体外实验表明,化疗耐药细胞株对PI3K抑制剂敏感。因此,以上研究表明PI3K/AKT通路激活可能是小细胞肺癌治疗耐药的潜在机制之一。这一发现值得进一步研究,并为逆转化疗/放疗耐药性提供了一种可能的方法。

吉凯助力

吉凯基因提供了本文FFPE样本的label free蛋白质组学服务。

吉凯基因凭借多年在靶标筛选及验证服务领域的技术积累,建立的标准化 、工程化 、系统化的GRP平台,为中国研究型医生提供科研服务,加快科研成果转化。其中,多组学平台包含蛋白质组学平台和高通量测序平台:
·蛋白质组学平台拥有多台timsTOF Pro、Exploris 480高精度质谱仪,专业领先的Spectronaut Plusar、Mascot等分析软件,提供专业的4D、DIA、TMT、PRM、磷酸化修饰组、olink蛋白质组等检测服务,强大的机器学习算法、IPA分析、蛋白基因组分析服务,系统的生物标志物、分子分型、药物靶点、基因功能研究等解决方案,真正让广大研究型医生的科研工作更省心、更省力、更高效;
·高通量测序平台分为常规测序服务和单细胞测序服务:单细胞测序拥有10x和BD两个平台,提供单细胞RNA-seq、单细胞核测序、单细胞混样RNA-seq、单细胞TCR/BCR、单细胞(RNA+ATAC)、空间转录组测序等服务;常规测序服务提供meRIP-seq(m6A/m1A/m7G/m5C 等RNA甲基化修饰测序)、acRIP-seq(ac4C RNA乙酰化修饰测序)、ATAC-seq、Ribo-seq(翻译组测序) 、mRNA/miRNA/LncRNA/circRNA-seq、全转录组测序(两文库/三文库)、外泌体miRNA/LncRNA-seq、WGS/WES、WGBS、RRBS、BSAS等服务。




1.实验技术干货
2.蛋白质组学研究
3.腺病毒简介及应用
6.单细胞测序
8.悬浮细胞专用病毒
10.测序技术研究与应用
12.腺相关病毒选择/应用
13.表观遗传研究
14.文章解析
15.国自然课题设计思路解析
16.生物信息分析及工具
17.外泌体研究
18.肿瘤免疫研究
19.高分文章
20.吉凯病毒神经方向应用案例

12-06 赛默飞
重磅!2023年“女科学家成长计划”圆满收官12-05
多巴胺女孩|叶慧教授:生如夏花「不设限的女学者」12-05
参与互动|科研人脱掉白大褂,是怎样的穿搭?12-05
炼油厂水质监测:实时数据如何影响水质、合规性和水的重复利用12-05 Sievers分析仪
宠粉时刻 | 2023年11月微信活动获奖名单12-05 Sievers分析仪
珀金埃尔默白皮书:选择聚合物生产和回收检测技术的最佳实践12-05 珀金埃尔默
【珀金大讲堂】高效问题解决之道12-05 珀金埃尔默
有“锂”行天下 | 钠离子电池能否成为替代能源的未来?12-05 珀金埃尔默
开课啦!珀金埃尔默2024年客户培训已开放报名12-05 珀金埃尔默
珀金埃尔默收购Covaris,共建全球创新主导的生命科学与诊断平台12-05 珀金埃尔默
使用NexION 5000 ICP-MS对超纯水中的杂质进行快速超痕量分析12-05 珀金埃尔默
应用分享 | MaxPeak Premier色谱柱分析靶向癌症生长抑制剂治疗药物12-05 沃特世
新品发布 | Imaris10.1人工智能显微图像分析软件12-05 牛津仪器
明确禁止检测人员同时在两家及以上检测机构从事检测活动12-05 交通运输部
超值特卖 | 赛默飞 离子色谱 准新机专场12-05 检测家
最美检测家 丨 敢于尝试,才能遇见新机遇——广东中健检测彭亚欣12-05 yea
校企合作,融合发展—岛津持续关注支持中国教育事业12-05 医疗中心
安捷伦PD-L1检测试剂盒(免疫组织化学法)获得FDA批准用于检测胃或胃食管结合部(GEJ)腺癌12-05
《安益谱MATE11便携气质,整车承包全国直达!》12-05