对SARS-CoV-2患者免疫反应的表征,是了解COVID-19疾病进展或者疫苗功效的关键。SARS-CoV-2抗原例如刺突蛋白(Spike Protein),S1和S2亚基,S1受体结合域(S1 RBD)以及病毒核衣壳蛋白(Nucleocapsid Protein)均可以刺激机体产生体液免疫应答,产生相应抗体。因此,不同抗原的反应性可能揭示了疾病进展的不同阶段。例如,与核衣壳的反应性可能是病毒早期感染的敏感性指标,而与S1 RBD和刺突蛋白的其他部分的反应性可能与病毒的中和有关。
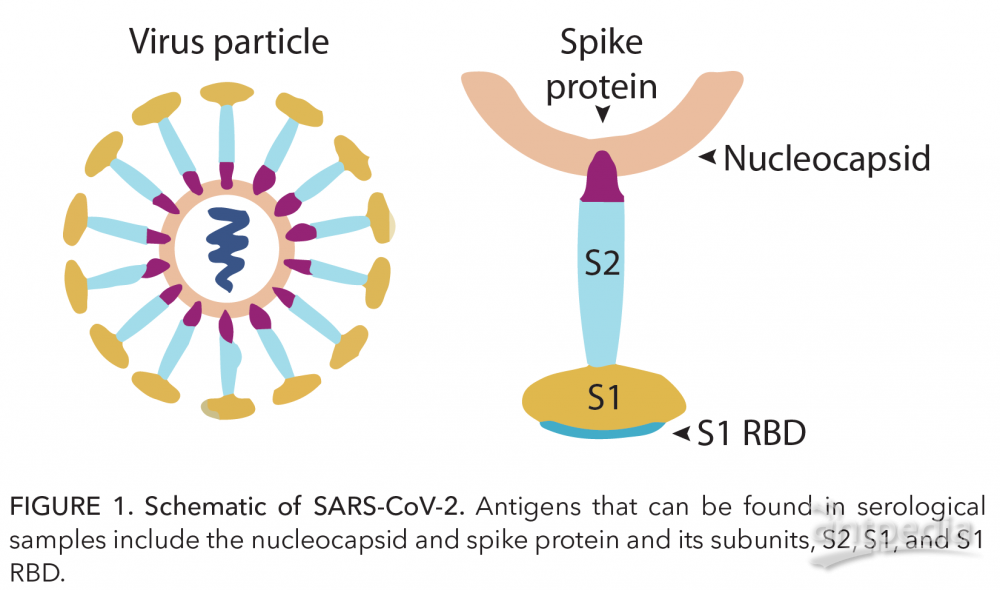
血清学免疫检测的常见方法是酶联免疫吸附测定(ELISA)法。但这种方法会面临:
为了克服这些局限,
全自动Western多抗原血清学检测试剂盒已上市!!
全自动Western多抗原血清学检测试剂盒的特点:
检测原理:
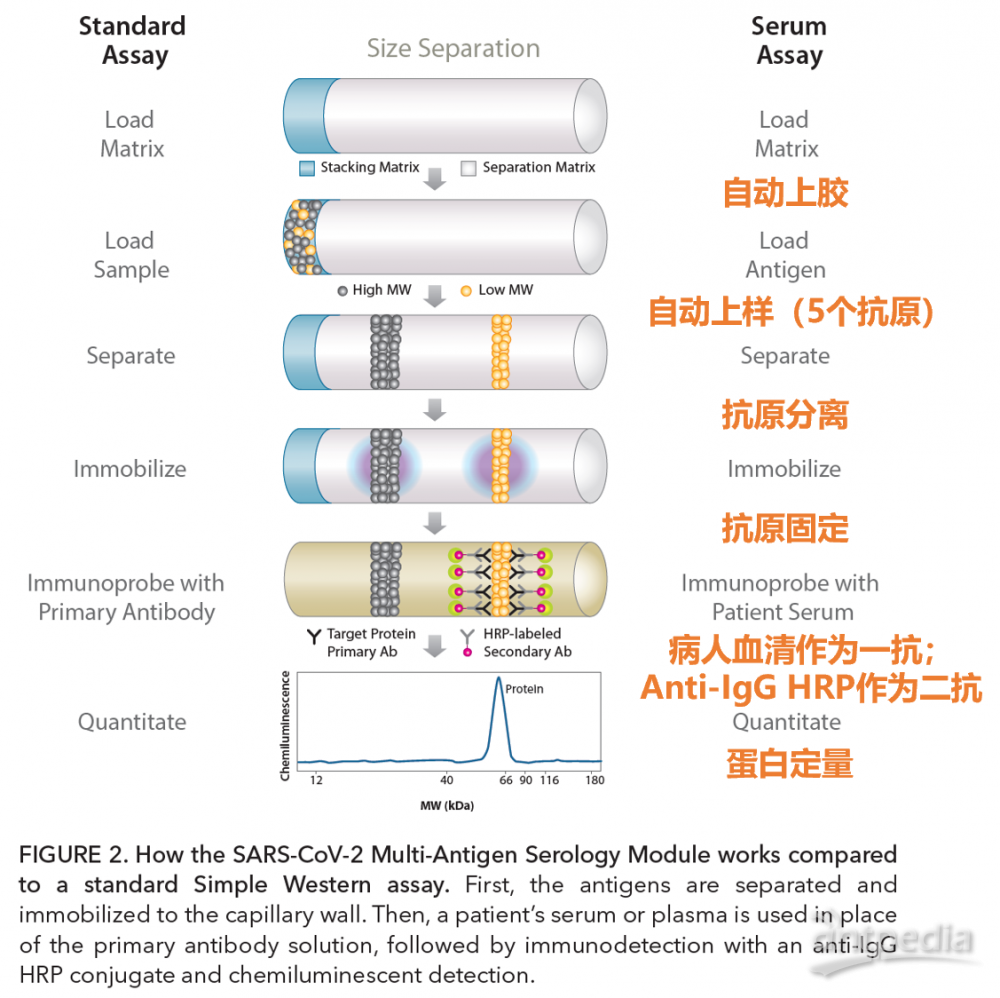
应用举例:
一份样品提供多种抗原信息
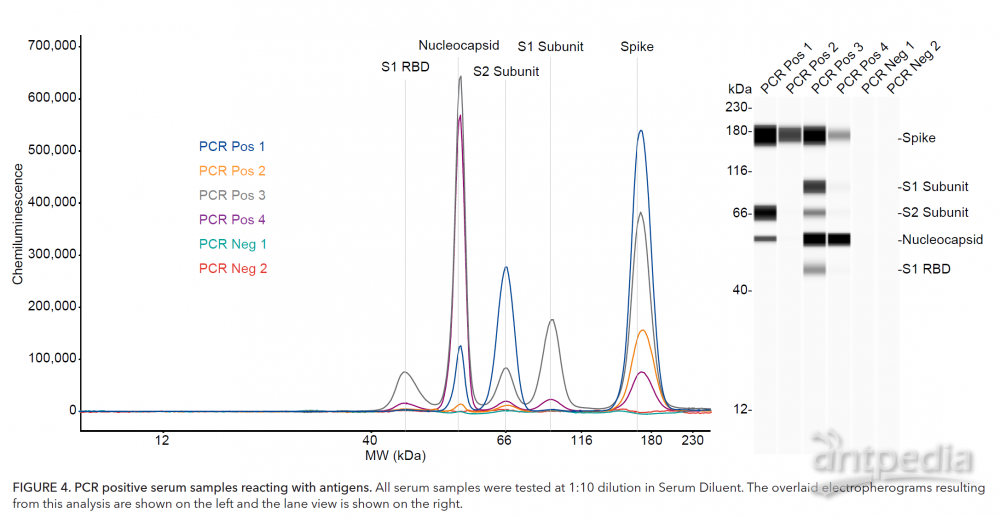
为了测试血清样品对这些抗原的反应性,对聚合酶链反应(PCR)确认为COVID-19阳性的4位患者的血清样品以及2份阴性样品进行全自动Western的血清学检测。结果显示,PCR阳性血清样品与试剂盒中包含的抗原具有高度反应性,PCR阴性血清样品没有反应性发生。其中PCR阳性3号样品中,可以显示出该血清样本对5个抗原(刺突蛋白(Spike Protein)、S1亚基、S2亚基、S1受体结合域(S1 RBD)、病毒核衣壳蛋白(Nucleocapsid Protein))均有反应性。
一份样本提供多种体液免疫学表征
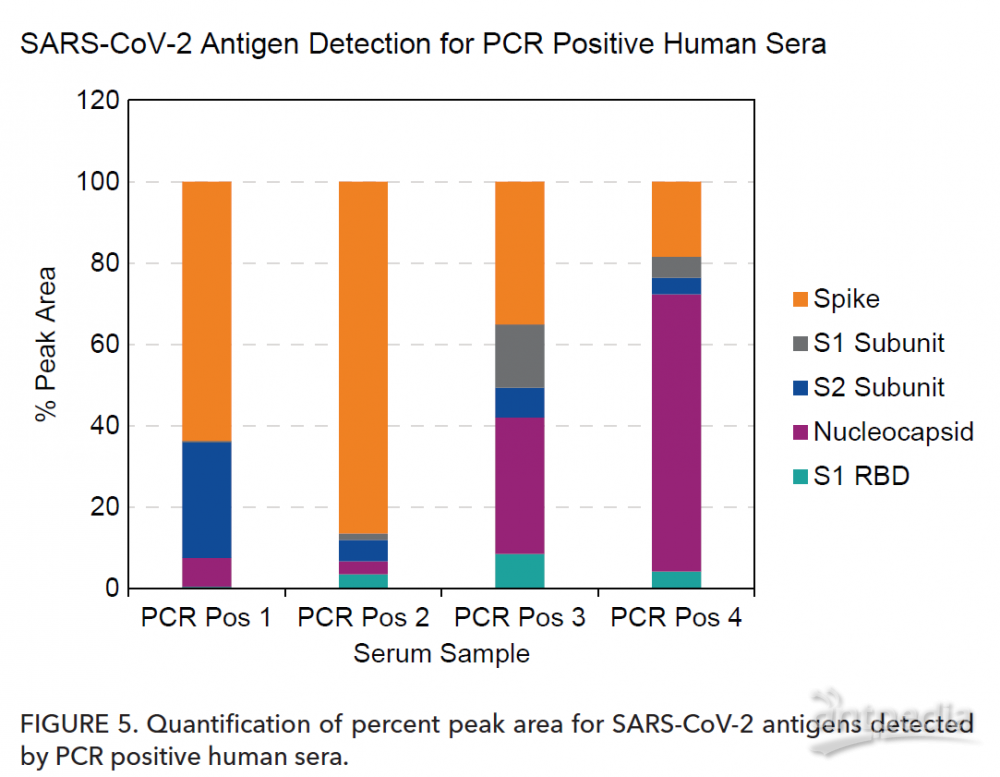
当对相对峰面积进行定量时,结果显示了与患者血清样品中的5种抗原中的每一种的IgG反应性的高度可变性。例如,患者4的血清样本与核衣壳的反应性高(占总峰面积的68%)。而患者1、2、3的血清样本与核衣壳的反应性低得多(分别为7%,3%和34%),但与Spike蛋白反应性增加。这预示着患者4血清样本中显示其对早期感染的指标敏感,而患者1、2和3的血清样本中可能已产生与靶向刺突蛋白上的表位相结合的中和抗体。
良好的稀释线性
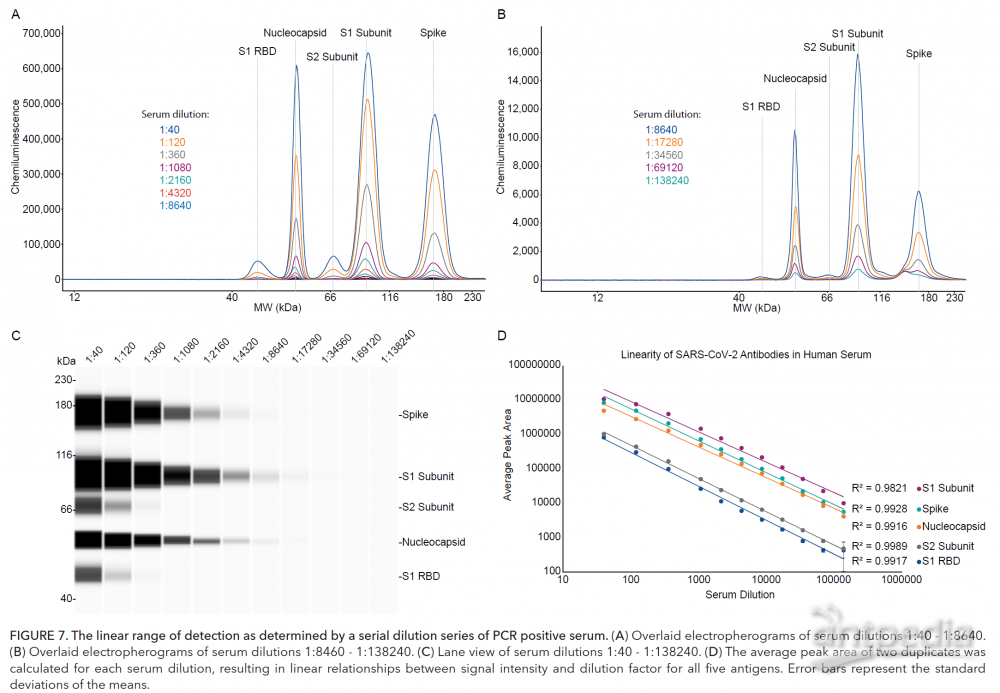
对PCR阳性血清样品从1:40到1:138240进行稀释系列,一式两份,并使用SARS-CoV-2多抗原血清学检测模块进行分析。结果显示,信号随着血清样品浓度的降低而降低(图A-C),并且该测定法显示出良好的线性,在3.5 log滴定系列中,五个抗原中的四个抗原的R2≥0.99,第五个抗原的R²≥98%(图D)。
高重复性
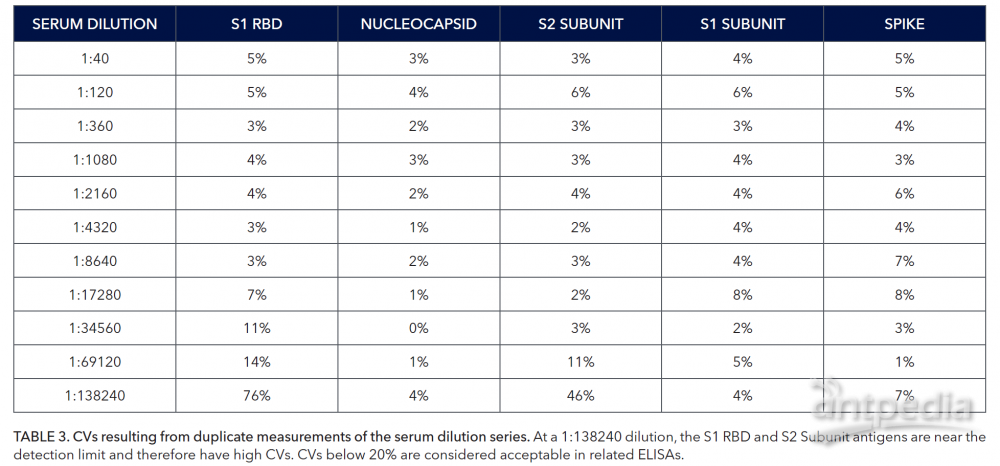
超过检测极限或≥1:69120的血清稀释液的CV小于15%,这表明该方法在重复测量中具有极好的可重复性。
结论:
随着SARS-CoV-2入侵机体的发展,可能会出现几种不同的抗原,这些抗原会导致体液免疫反应异常,而针对这些抗原的抗体的出现可能表明了疾病进展和病毒中和的不同阶段。因此,传统ELISA检测仅用一种抗原包被的蛋白只能捕获非常有限的免疫学反应信息。但借助适用于全自动Western(Jess/Wes)的SARS-CoV-2多抗原血清学检测试剂盒,可以同时分析COVID-19中常见的多达5种不同抗原在人血清或血浆样品中的IgG反应性。这使得能够对体液反应进行更深入的分析,并且揭示了血清反应性之间的差异,而这种差异是传统ELISA试剂盒无法获取的。

参考文献:
1. Sensitivity in detection of antibodies to nucleocapsid and spike proteins of severe acute respiratory syndrome coronavirus 2 in patients with coronavirus disease 2019, P Burbelo, F Riedo, C Morishima, S Rawlings, D Smith, S Das, J Strich, D Chertow, R Davey and J Cohen, The Journal of Infection Diseases, 2020; 222:206-213.
2. Isolation of potent SARS-CoV-2 neutralizing antibodies and protection from disease in a small animal model, T Rogers, F Zhao, D Huang, N Beutler, A Burns, W He, O Limbo, C Smith, G Song, J Woehl, L Yang, R Abbott, S Callaghan, E Garcia, J Hurtado, et al., Science, 2020; 369(6506):956–963.
3. A panel of human neutralizing mAbs targeting SARS-CoV-2 spike at multiple epitopes, T Noy-Porat, E Makdasi, R Alcalay, A Mechaly, Y Levy, A Bercovich-Kinori, A Zauberman, H Tamir, Y Yahalom-Ronen, M Israeli, E Epstein, H Achdout, S Melamed, T Chitlaru, S Weiss, et al., Nature Communications, 2020; 11(1):1–7.
更多信息请咨询ProteinSimple销售或技术人员。














