
健 康
肥胖、糖尿病、心血管疾病以及其他代谢综合征范畴内的相关疾病,是关系到我们健康最紧迫的问题,其中代谢相关的激素由内分泌系统的各个器官,包括脂肪细胞、胰腺和胃肠道分泌。在调节能量、食物摄取量和全身代谢方面发挥着重要作用。
近些年,随着II型糖尿病的发病率上升,代谢类疾病甚至已经影响到儿童和青少年人群。所以加快代谢综合征相关的激素研究,对代谢类疾病的治疗和预防都至关重要。
因为维持系统的平衡状态需要多个信号分子,所以没有一个生物标志物足以定义一个系统。另一方面,基于传统的检测手段,由于样本容量的限制,一次测量多个分析物是难以完成的。
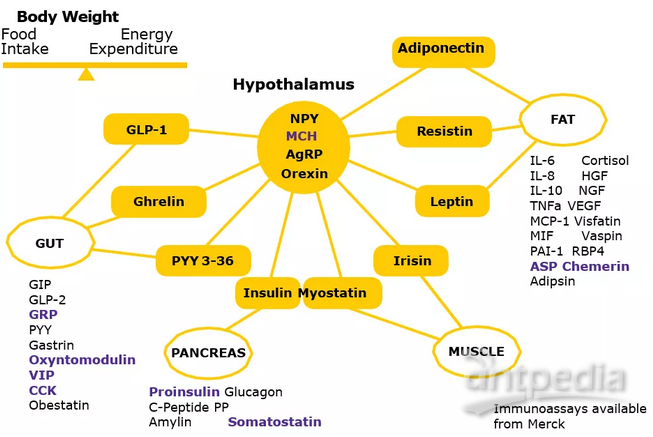
▲图1:各种器官向大脑分泌的多种信号有助于维持食物摄入和能量消耗之间的平衡,调节体重和新陈代谢
为了克服这些挑战,基于Luminex®xMAP®磁珠技术的MILLIPLEX®MAP多因子检测试剂盒,可以实现同时定量代谢相关分析1。MILLIPLEX®代谢激素检测试剂盒的主要优势是包含:总GLP-1的检测和活性GLP-1的高灵敏度检测。
▼在此案例中,我们向您介绍一个多重、稳定、灵敏的代谢激素多因子检测试剂盒,可以同时检测包括如下13种代谢激素:

除了评估整个试剂盒的准确性和精密度外,我们还比较了MILLIPLEX®活性GLP-1高灵敏度试剂盒与默克金标准高灵敏度活性GLP-1的ELISA法试剂盒,得到的检测结果一致(货号:EZGLPHS-35K)。
1.材料和方法
实验检测使用:MILLIPLEX®人类代谢激素检测试剂盒(货号:HMHEMAG-34K),实验按照试剂盒说明书进行操作。
为了确定代谢激素水平与食物摄入量的关系,我们采集了正常受试者(n=20)在禁食一晚或标准早餐后一小时的血液样本。在采集的血样中立即加入蛋白酶抑制剂(DPPIV抑制剂、AEBSF、蛋白酶抑制剂)。根据检测方案,使用MILLIPLEX®人代谢激素试剂盒,对血清和血浆样品进行分别进行检测。
同时,针对同一份样本使用默克公司高灵敏度GLP-1 ELISA试剂盒(货号:EZGLPHS-35K)进行检测,按照试剂盒说明书进行操作。
2.结 果
使用血清基质中连续稀释的每种分析物的标准,制备标准曲线,以测定相对于分析物浓度的测定反应(以平均荧光强度[MFI]测量)(图2B)。
标准曲线为所有因子设定用于检测的线性度超过3~5个数量级(图2A),试剂盒内所有因子未见交叉反应(数据未展示)。根据检测数据显示,MILLIPLEX®回收率达94%~107%,精度好(小于10%的板内变异系数[CV]和15-20%的板间变异系数(图2A)。
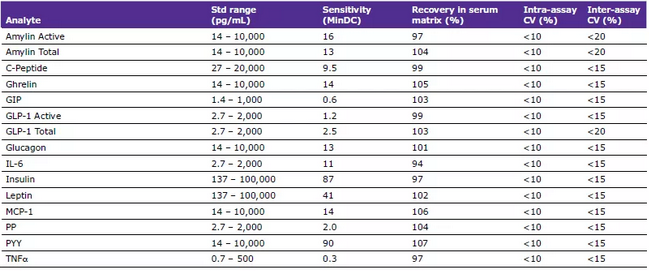
▲ 图2A
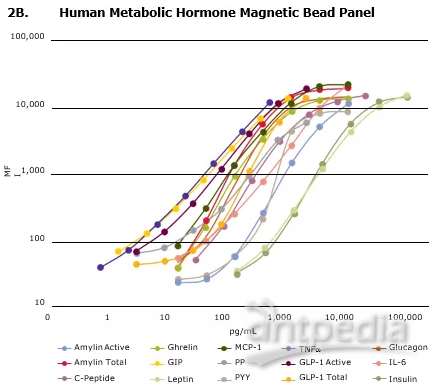
▲图2B:验证数据(2A)和标准曲线(2B)使用血清基质稀释,并使用MILLIPLEX®MAP 人类代谢激素试剂盒(Cat. No. HMHEMAG-34K)
接下来,我们评估了MILLIPLEX®试剂盒检测生物样品的性能。
正如之前的预期,多种代谢激素水平会随着食物的摄入而发生变化(血清中C-Peptide, GIP, active GLP-1与Insulin水平升高,如图3A所示)。将匹配的人血清和血浆样本进行比较,发现大多数分析物的血清和血浆样本浓度非常接近(数据如图3B所示)。
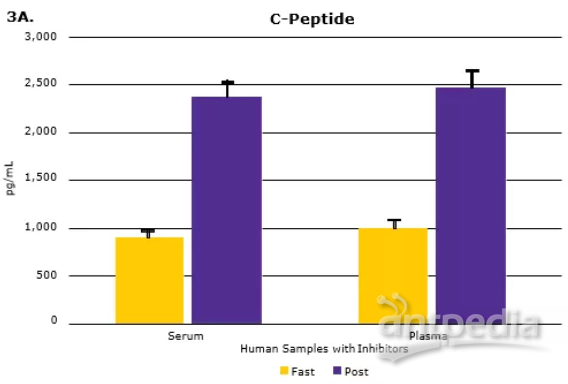
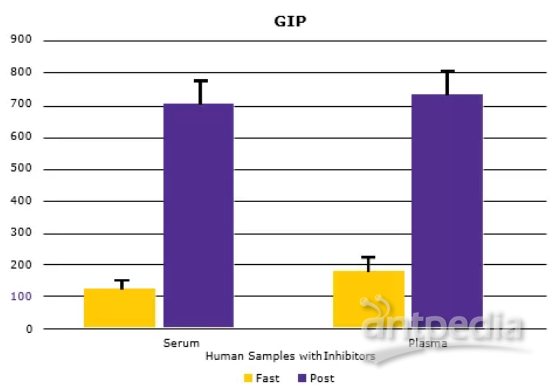
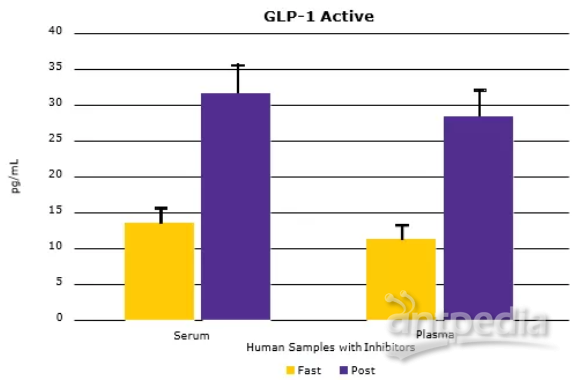
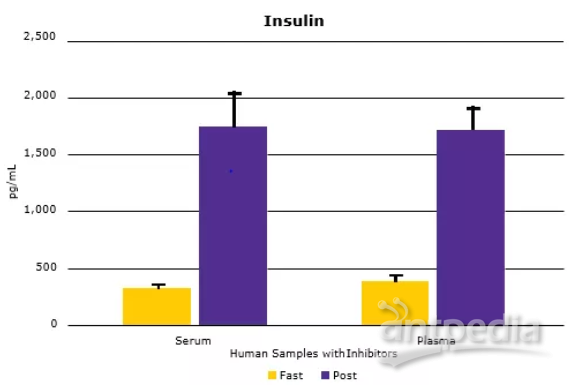
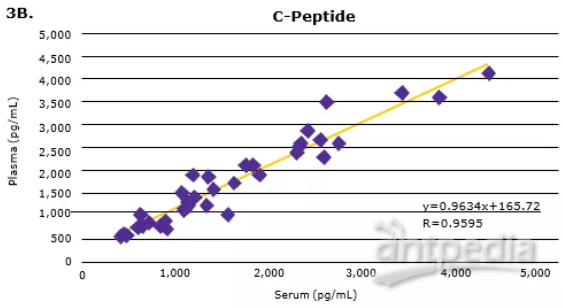
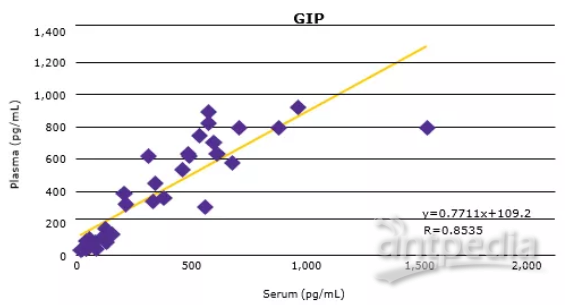
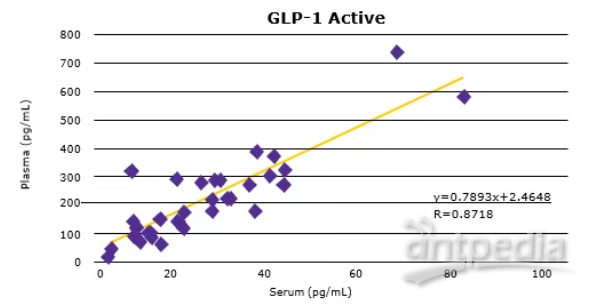
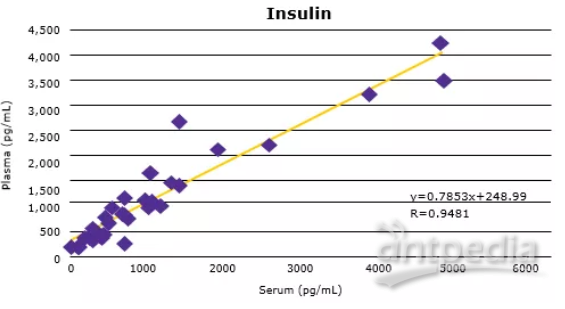
▲图3:使用MILLIPLEX®多因子试剂盒检测人类空腹或餐后受试者血清(样本中已加蛋白酶抑制剂)和血浆中的代谢激素。血清C-Peptide, GIP, active GLP-1和Insulin (3A)均有预期升高。从相关曲线(3B)中的斜率和R值可以看出,血清分析物水平与血浆分析物水平比较具有良好的相关性
我们分别使用MILLIPLEX®人类代谢激素检测试剂盒与目前已证实稳定的默克高敏活性GLP-1 ELISA试剂盒同时进行检测,并比较了活性GLP-1的定量检测结果(图4):
● 使用GLP-1重组蛋白,按照一定比例进行梯度稀释建立标准曲线,最终显示出几乎一致的反应结果数据和分析的线性范围(图4A);
● 使用MILLIPLEX®多因子技术与ELISA技术分别检测生物样品中GLP-1的表达水平,并进行比较后(图4B),显示这两种方法检测结果具有很好的相关性。
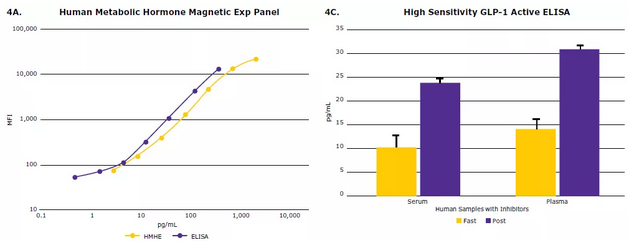
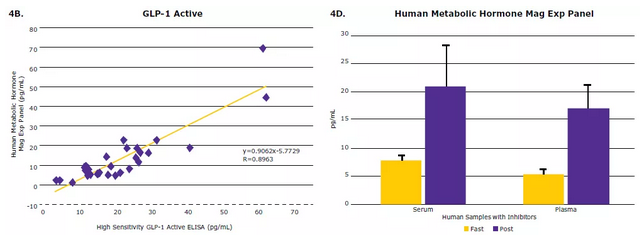
▲图4:MILLIPLEX® GLP-1(活性)检测结果与GLP-1(活性)ELISA检测结果(4A)的相关性,血清样本(4B)和空腹与餐后受试者的比较(4C和4D)
讨 论
通过以上的实验结果,MILLIPLEX®人类代谢激素检测试剂盒与其他商业上可用的多重检测试剂盒进行比较,该试剂盒操作更加友好、结果更加准确,检测性能与其他供应商的试剂盒相似或更好。该代谢相关激素检测试剂盒,在代谢疾病和其他相关病理生理学领域的基础研究和临床研究中,有潜力成为一个非常有用的工具。
代谢研究相关MILLIPLEX®试剂盒▼
Name | Analytes | Cat. No. |
Human Adipokine Panel 1 (Serum/Plasma samples) | Adiponectin, Adipsin/FactorD/NGAL/Lipocalin-2, PAI-1 (total), Resistin | HADK1MAG-61K |
| Human Adipokine Panel 2 (Serum/Plasma samples) | HGF, IL-1β, IL-6, IL-8/CXCL8, Insulin, Leptin, MCP-1/CCL2, NGF, TNFα | HADK2MAG-61K |
Human Adipocyte (Cell culture samples) | Adiponectin, HGH, IL-1β , Il-6, IL-8/CXCL8, Leptin, MCP-1/CCL2, NGF,PAI-1 (total), Resistin, TNFα | HADCYMAG-61K |
| Human Myokine | Apelin,
BDNF, Erythropoietin (EPO), FABP3, FGF21, Fractalkine/CX3CL1,FSTL1,
IL-6, IL-15, Irisin, LIF, Myostatin/GDF8, Oncostatin-M
(OSM),Osteocrin/Musclin, Osteonectin/SPARC | HMYOMAG-56K |
Human Pituitary Panel 1 | ACTH, Agouti-Related Protein (AgRP), CNTF, FSH, GH, LH, TSH | HPTP1MAG-66K |
Multi-Species Steroid/Thyroid Hormone | Cortisol, Estradiol, Progesterone, T3, T4,Testosterone | MSHMAG-21K |
参考文献
1.Gibbons C, Caudwell P, Finlayson G, Webb DL, Hellström PM, Näslund E, Blundell JE. Comparison of postprandial profiles of ghrelin, active GLP-1, and total PYY to meals varying in fat and carbohydrate and their association with hunger and the phases of satiety. J Clin Endocrinol Metab. 2013 May; 98(5): E847-55.
2.Unger RH, Aguilar-Parada E, Müller WA, Eisentraut AM. Studies of pancreatic alpha cell function in normal and diabetic subjects. J Clin Invest. 1970 Apr; 49(4): 837 – 48.
3. Marliss EB, Aoki TT, Unger RH, Soeldner JS, Cahill GF Jr. Glucagon levels and metabolic effects in fasting man. J Clin Invest. 1970 Dec; 49(12): 2256 – 70.
4.Felig P, Wahren J, Hendler R. Influence of physiologic hyperglucagonemia on basal and insulin-inhibited splanchnic glucose output in normal man. J Clin Invest. 1976 Sep; 58(3): 761 – 5.
5.Nishino T, Kodaira T, Shin S, Imagawa K, Shima K, Kumahara Y, Yanaihara C, Yanaihara N. Glucagon radioimmunoassay with use of antiserum to glucagon C-terminal fragment. Clin Chem.1981 Oct; 27(10): 1690-7.
6.Aliberti G, Pulignano I, Proietta M, Miraldi F, Cigognetti L, Tritapepe L, Giovanni CD, Arzilla R, Vecci E, Toscano M. Hormone metabolism in the pulmonary circulation. Physiol Res. 2001; 50(3): 231 – 5.
7.Zoladz JA, Duda K, Konturek SJ, Sliwowski Z, Pawlik T, Majerczak J. Effect of different muscle shortening velocities during prolonged incremental cycling exercise on the plasma growth hormone, insulin, glucose, glucagon, cortisol, leptin and lactate concentrations. J Physiol Pharmacol. 2002 Sep; 53(3): 409 – 22.
8.Nauck MA, Heimesaat MM, Behle K, Holst JJ, Nauck MS, Ritzel R, Hüfner M, Schmiegel WH. Effects of glucagon-like peptide 1 on counterregulatory hormone responses, cognitive functions and insulin secretion during hyperinsulinemic, stepped hypoglycemic clamp experiments in healthy volunteers. J Clin Endocrinol Metab. 2002 Mar; 87(3): 1239 – 46.
9.Broglio F, Gottero C, Prodam F, Destefanis S, Gauna C, Me E, Riganti F, Vivenza D, Rapa A, Martina V, Arvat E, Bona G, van der Lely AJ, Ghigo E. Ghrelin secretion is inhibited by
glucose load and insulin-induced hypoglycaemia but unaffected by glucagon and arginine in humans. Clin Endocrinol (Oxf). 2004 Oct; 61(4): 503 – 9.
10.Hattori N, Saiki Y, Kajikawa M, Ishihara T, Moridera K, Hino M, Ikekubo K, Kurahachi H. Immunoglobulin G can cross-react with glucagon antisera and cause a spuriously high plasma immunoreactive glucagon level. Endocr J. 1995 Aug; 42(4): 455-60.
11.Teixeira RC, Nico MM, Ghideti AC. Necrolytic migratory erythema associated with glucagonoma: a report of 2 cases. Clinics (Sao Paulo). 2008 Apr; 63(2): 267 – 70.
12.Okauchi Y, Nammo T, Iwahashi H, Kizu T, Hayashi I, Okita K, Yamagata K, Uno S, Katsube F, Matsuhisa M, Kato K, Aozasa K, Kim T, Osuga K, Nakamori S, Tamaki Y, Funahashi T, Miyagawa J, Shimomura I. Glucagonoma diagnosed by arterial stimulation and venous sampling (ASVS). Intern Med. 2009; 48(12): 1025 – 30.
13.Jin Wang, Merck In-House Assay Results. July, 2011.

















