
诚信认证:
工商注册信息已核实! 扫一扫即可访问手机版展台
扫一扫即可访问手机版展台
如何理解电子记录和电子签名(21CFR Part11,Electronic Records; Electronic Signatures)
| 领域: | 细胞生物学,原料药/中间体,药物代谢 | ||
| 资料类型: | 课件讲义 | ||
| 资料文件名 | 下载 |
|---|---|
如何理解电子记录和电子签名(21CFR Part11,Electronic Records; Electronic Signatures) |
下载此篇资料 |
CFR 21主要涉及的是食品与药品。Part 11规定了电子记录和电子签名的要求,并说明了FDA认可电子记录和电子签名与纸质记录和纸质签名具有相同法律效力,均是可信和可靠的。以下这是FDA网站公布的21CFR Part11的年度版内容大纲(如图1)。
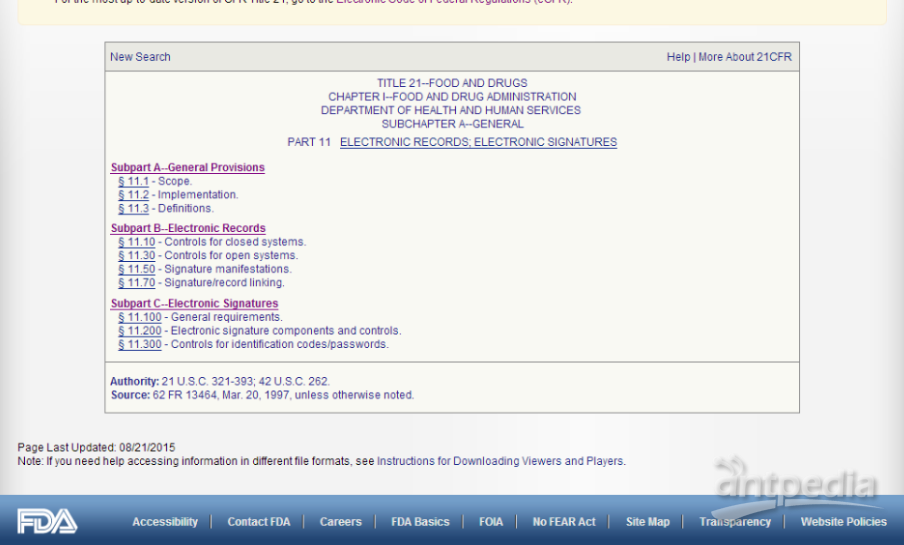
为了方便大家理解,我先向大家介绍几个专有名词。
封闭系统是指一种环境,在此环境中,登录系统会被那些对系统上的电子记录的内容负责的人员所控制。基本上所有医院和实验室的系统都是封闭的。通过相应的安全系统,实验室对谁能够进入系统实行完全的控制,例如软件登录。
与之相对就是开放系统,在此环境中,登录系统不被那些对系统上的电子记录的内容负责的人员所控制。实验室里的开放系统一般是由第三方控制的,数据存储在服务器上的系统,开放系统还包括每个人都可以访问Internet,例如MS完成测试后,对未知蛋白搜库比对。
电子记录相对好理解,是种数字格式的记录,由文本、图表、数据、声音、图示或其他数字信息构成。电子记录的创建、修改、维护、归档、读取(包含检索、展示)或分发都由计算机系统执行。
手写签名是个人手写的名字或合法的标记,以一种永久的方式来证明其签名是真实的,签字行为代表了签名者的当时意图。使用书写或做标记工具(例如钢笔或尖笔)来保存签字的行为。通常而言,签名和标记都是指在纸上产生的签名或标记,但此处同样适用于在其他能够捕捉名字和标记的装置上产生的签名或标记。
电子签名是指任何一种符号或者符号集的计算机数据汇编码,该符号或符号集由使用者绘制、采用或批准,该电子签名与手写签名具有相同的法律效率。如手机上的手势解锁。
数字签名是电子签名的一种方式,数字签名采用密码(固定密码、动态密码)方式进行发起人身份鉴别,该密码由一套规则和一系列参数计算生产,以此来验证签名者的身份和数据的完整性。如网银的电子口令卡,固定密码和U盾。
在21 CFR Part11的总则中,阐述了1)满足此条款的电子记录、电子签名和电子记录上的手签名与纸质记录、书写在纸质记录上的签名具有相同的法律效力,除非纸质记录有特殊的要求,否则符合本条款要求的电子记录均可以替代纸质记录,以及2)本条款中内容适用包括现有体系中所有FDA监管的工作中的电子记录。值得注意的是在总则中规定了1997年8月20日生效日之前的电子记录、电子签名和电子记录上的手签名,对纸质记录有特殊的要求和以电子方法(例如:扫描、传真)提交给FDA的纸质记录均不符合此条款。
在本条款实施过程中,分两种情况:1)针对FDA要求维护但不需要提交的记录 ,能证明全部满足本条款的要求;2)针对FDA要求提交的记录 ,能证明全部满足本条款的要求 ;FDA接受的电子形式的文件必须已在公共摘要NO.92S-0251上明确刊出,其中内容包括电子文件的类型和接收单位。否则,必须提交纸质的文件(电子文件是附件)。
电子记录(Electronic Records)
对于电子记录部分来说,封闭系统的管理,核心原则有两条:1)保证记录的真实性、完整性和保密性;2)确保签名者无法轻易地否认其签名行为,即防止签名者不承认签字是他本人的。具体操作分系统,用户和审计追踪三个方面控制。而开放系统的管理,与封闭系统主要的差别在于机密性,即必要时,需要使用额外的方法(文档加密技术、合适的数字签名技术)来确保电子记录的真实性、完整性和机密性。其余控制方式,与封闭系统几乎没有差别。
对于签署电子记录,其电子签名应包括至少三点信息才算完整:签名人的完整名字,签名的日期和时间,签名代表的含义。电子记录本身也应包含这三方面的信息。为了防止他人伪造,在电子记录上签署的电子签名和手签名必须和对应的电子记录紧密关联在一起。
电子签名(Electronic Signatures)
电子签名应具有三个特性:唯一性,确定性和合法性。唯一性是指个人拥有的电子签名应该是一一配对的,唯一的,(即使此人今后不再使用其电子签名),该电子签名也不能被他人再次使用,或被再次分配给其他人。 确定性是指当组织创建、分配、认证、批准个人的电子签名(或电子签名的要素)之前,组织应先核实个人的身份 。合法性是用户在使用电子签名之前或首次使用之际,应向FDA声明在自己(或公司)的系统内(该系统是1997.08.20起或之后投入使用的)电子签名,与其传统的纸质手签名具有相同的法律效力。在21 CFR Part 11的电子签名部分规定了身份识别码和密码的管控。譬如每个用户有自己的用户名(即身份识别码)和密码,用户名唯一,密码只有使用人员自己知晓,需要定期修改密码和符合相应密码复杂性的要求。
21 CFR Part 11的应用
对于这条法规的解读,大家可能形成一个误区。只需实验室的相应软件符合21 CFR Part 11,其实FDA审查是看体系的符合性,除软件外,还包括体系内硬件、SOPs、人员培训和管理的对21 CFR Part 11 的符合性。
对于CFR Part11的具体应用,我认为系统的安全、确保电子记录的完整性和数据保存迁移三个方面较为重要。
对于系统的物理安全,例如门禁系统,SOP的执行等等。而逻辑安全,包括用户ID在系统中具有唯一性;用户组,用户类型,项目权限和系统权限均需区分管理等内容。此外,我们还需定期评估和验证系统是否符合21 CFR Part 11的要求。
对于确保电子记录的完整性,主要是审核跟踪,可追溯性和时间标记和参考完整性三个方面。1)审核跟踪体现了数据的可追溯性,主要还是5W+1H(who、what、when、why、where and how)原则。2)可追溯性和时间标记,包括实验室所在的时区等相关信息。3)完整数据是由没有被破坏的原始数据,元数据(处理过程参数、审核追踪日志)和 结果组成。因此,电子记录的完整性还包括了参考完整性,确保数据完整性要求相关联的电子记录之间保持不可破坏的关联性。
对于数据保存和数据迁移,需要衡量不同指标。对于记录的归档和恢复,需要衡量FDA的指导原则,数据类型,储存介质和读写记录用的软件;而对于数据的迁移,需要衡量兼容性、有效性、迁移过程和旧数据的依从性等等。






