
扫码预约聆听婷声音



声音节目5期已全部更新
本期“婷视角”专栏,婷姐谈生物药的研发第2期:宿主细胞蛋白残留分析
本期声音内容
Hey,大家好,我是您的质谱应用专家刘婷,来自SCIEX中国市场部,负责高级解决方案的开发与支持。15年的一线应用经验,让我深感到质谱应用信息共享的重要性。无论是质谱前沿技术,还是常用技术的深入应用,都希望在我的这个专栏中能和大家分享。“婷视角,看分析“希望拓宽您的视野,进入美妙的的质谱应用世界。
01
大家好,我们又见面了。上期内容我们聊了聊LC-MS/MS在生物技术药物质量控制中的两个热点应用。一个是 “细胞上清液或培养基监控”,LC-MS/MS能一针高通量定量上百个目标化合物,如:糖,氨基酸,有机酸,核酸和维生素等;另一个是 “一次性使用系统的萃取物及可浸出物研究”,LC-PDA/UV-MS/MS配合数据库使用,能快速鉴定未知化合物。
在质量控制中,除了上期谈到的两方面应用外,生物技术药物的残留物检测也非常重要,如:残留抗生素的测定和宿主细胞蛋白残留分析(Host Cell Protein,HCP)。LC-MS/MS进行残留抗生素的测定[1],相比传统的“培养法”和“酶联免疫法“,具有高通量,高灵敏度和快速的特点, 这是大家所熟知的。特别是在食品抗生素残留的检测应用中,LC-MS/MS已成为检测的黄金标准。另一方面,使用 LC-MS/MS进行HCP研究,也越来越多地被科研工作者所使用。HCP检测正是本期内容的重点。
生物制品中残留的宿主细胞蛋白作为外源蛋白,含量低,可能在不同程度上引发机体的免疫应答,最终导致过敏反应或其他不良反应,因此建立合适的HCP检测方法监控生物制品的质量尤为重要。
酶联免疫法(Enzyme-Linked ImmunoSorbent Assay,ELISA)是应用最广泛的 HCP检测方法,但这个技术本身也具有局限性。如:ELISA法并不能保证检测到每个潜在的HCP杂质,且仅能进行半定量,无法判断是多个HCP残留还是一个HCP的高浓度残留;同时,开发特定工艺专用的ELISA试剂盒耗时长, 成本高;且不适用于全面综合评估利用不同细胞类型或纯化方案制得的生物药产品。为了解决这些问题,LC-MS/MS作为ELISA方法的正交和补充手段进入科研人员的视野,主要对痕量HCP进行鉴定和定量。
使用LC-MS/MS进行HCP检测,根据不同的研究目的,主要有两个测定思路。1个是目标HCP测定,适用于已确定生产工艺的生物药的质量控制,常使用常规分辨率质谱的MRM[2]或者是高分辨MRM(MRMHR)扫描模式, 获得亚µg/mL或µg/mL级别的灵敏度。
第2个是在工艺研发中,为了设计和优化纯化过程,需要对不同的纯化工艺或不同纯化步骤中的HCP进行高通量、稳定评价。且由于产品的纯化工艺往往是通过特定的结合或反应来进行, 这表明残留的HCP往往是未知的。因此在此类研究中,高分辨质谱(High Resolution Mass Spectrometer, HRMS)被广泛使用。
美国基因工程技术公司(简称基因泰克, Genentech)的Donald E[3] 报道了一个支持纯化工艺研究的通用流程。文中指出该流程支持纯化工艺研究的两个难点:首先是通量要求,为了满足工艺的快速优化要求,每天至少20个左右的样品通量;其次是要求有一种采集方式,可同时对多个未知HCP进行高灵敏度定量。所以作者将样品检测分为2类,根据样品不同特点,选择不同采集模式测定。
他首先使用1D MicroLC-DDA(数据依赖采集模式,Data Dependent Acquisition)采集模式,每个样品运行时间1h,可以鉴定到上千个蛋白,添加多个(>=2个)特定HCP蛋白于不同样品中,同时检出的灵敏度可达50µg/mL, 该方法适用于纯化工艺前期较高浓度的HCP样品;依据该方法,可鉴定未知HCP,同时对其定量。
但我们也知道, 在纯化工艺的后期,HCP的浓度大大降低,仅为10µg/mL级别。文中指出:对于灵敏度要求高的样品,使用1D MicroLC-SWATH采集技术,可对多个未知HCP同时定量,且能达到10µg/mL的检测灵敏度,普遍比Full MS的灵敏度提高了2-8倍;该采集模式既满足了同时定量多个未知HCP的通量要求,又满足了灵敏度要求(图1)。
上面提到的两种采集模式相结合,完全满足样品通量要求,可支持10-20个不同条件下的样品测试。报道中提到:早先的2D-NanoLC-MS工作流程,由于2D系统保留时间(Retention Time, RT)很难重现,且Nano的低流速导致每个样品分析时间需要10-20h, 所以很难支持高通量的纯化工艺要求。同时,高分辨质谱的MRM和常规分辨率质谱的MRM 扫描仅为靶向蛋白的定量方法,并不适用于未知HCP的定量。
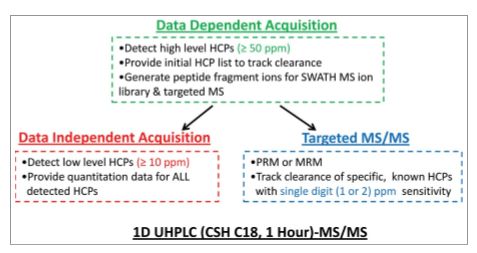
图1:HCP分析策略,目标和非目标HCP在不同方法平台下的灵敏度和通量对比; (摘自文献[3])
02
对于SWATH的定量能力,南丹麦大学的Søren[4]使用1D MicroLC-SWATH采集技术对不同数量级的HCP进行快熟可靠的绝对定量。在样品处理前,将一组参考蛋白加入样品中,通过选择Top3个肽段定量,评价不同浓度的无标(Label-free)定量结果。然后,使用稳定同位素标准肽(SIS)进一步评价无标绝对定量结果,结果显示:CV%偏差平均值为6%。将这一策略用于真实样品的纯度测定,其结果表明样品中HCP含量值和ELISA方法一致,说明此策略的分析速度和简单的操作流程,完全支持纯化工艺的开发要求。
通过上面的两个研究,可以了解到:使用1D-MicroLC-SWATH采集技术可以在30min-1h的时间内完成上百个HCP蛋白的相对或绝对定量,定量灵敏度可达10 µg/mL, 且平均CV%在6-7%左右。该技术的定量性能,也被作者Justin[5]的研究所证实,他也使用1D-MicroLC-SWATH进行定量,其可测定到7-30µg/mL的HCP残留,平均CV%为7%。
如果您希望进一步提高未知HCP的灵敏度,作者Bryan[6]使用CESI-SWATH采集技术可定量到亚µg/mL级别的HCP。使用CESI技术分离,可以减少基质抑制效应,提高定量灵敏度,为我们的研究提供了进一步的参考。
最后,总结一下本期内容:
如果测定目标HCP,可以选择常规分辨率质谱的MRM或高分辨质谱的MRMHR扫描模式,可提供亚µg/mL或µg/mL级别的灵敏度;
如果需要设计和优化纯化工艺, 可以选择高分辨质谱的1D-MircoLC-DDA鉴定未知HCP后,使用1D-MircoLC-SWATH采集技术对其相对或绝对定量, 灵敏度可达10µg/mL,,重现性良好;方法简单,测定通量高,具有普遍性;
如果既要测定未知HCP,又要达到亚µg/mL级别的灵敏度,不妨试试CESI-SWATH采集技术;
本期内容到这里就结束了,本期主要介绍了在生物技术药物中HCP的测定策略,也听到了一个新词汇“CESI” 。下期内容,我们就来了解一下“高效毛细管电泳(CE)和毛细管电泳质谱联用技术(CE-MS/MS)在生物技术药物研究和开发中的应用” 尽请期待!
参考文献:
1. 徐传学等. 生物制品中抗生素的使用及残留检测方法[J]. 国外医药抗生素分册, 2017年7月第38卷第4期;
2. Steven A. Carr‡, et al. Targeted Peptide Measurements in Biology and Medicine: Best Practices for Mass Spectrometry-based Assay Development Using a Fit-for-Purpose Approach[J]. Molecular & Cellular Proteomics, 2014, January 17.
3. Donald E. Walker, et al. A modular and adaptive mass spectrometry-based platform for support of bioprocess development toward optimal host cell protein clearance[J]. mAbs, 2017, Apr 07.
4. Søren Heissel, et al.Evaluation of spectral libraries and sample preparation for DIA-LC-MS analysis of host cell proteins: A case study of a bacterially expressed recombinant biopharmaceutical protein[J]. Protein Expression and Purification, 2018, 147, 69-77.
5. Justin Blethrow, Eric Johansen. High Sensitivity Host Protein Quantitation in an IgG1 Monoclonal Antibody Preparation via Data-Independent Acquisition. SCIEX Technote.
6. Bryan Fonslow, Eric Johansen. Ultra-sensitive host cell protein detection using CESI-MS with SWATH® acquisition. SCIEX Technote.
声明:版权为 SCIEX 所有。欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权, 转载时须注明「来源:SCIEX」。申请授权转载请在该文章下“写留言"。


喜欢就点在看哟



