
上海欧易生物医学科技有限公司
诚信认证:
工商注册信息已核实! 扫一扫即可访问手机版展台
扫一扫即可访问手机版展台
项目文章 | 上海九院发现头颈癌化疗耐药中外泌体 miRNA 作用机制
基本信息
论文题目:Exosomal miR-196a derived from cancer-associated fibroblasts confers cisplatin resistance in head and neck cancer through targeting CDKN1B and ING5
发表期刊:Genome Biology
发表时间:2019.1.14
影响因子:13.214
本文第一作者为上海交通大学医学院附属第九人民医院口腔-颌面头颈肿瘤科博士研究生秦星、检验科郭海艳医师。本文通讯作者为上海交通大学医学院附属第九人民医院张建军副研究员、陈万涛教授和上海交通大学医学院附属仁济医院陆尔奕教授。
本文涉及的高通量技术:基因芯片(Affymetrix miRNA 芯片)由欧易生物提供服务
研究背景
头颈癌(head and neck cancer, HNC)是一种发病率较高的侵袭性肿瘤,恶性增殖和化疗耐药是 HNC 治疗的主要限制因素。目前头颈癌的治疗手段包括手术、放疗、化疗和 EGFR 抗体治疗。顺铂是晚期 HNC 患者化疗使用的核心药品,对基于顺铂的化疗,患者最初会有良好的初始反应,但随着顺铂耐药性的出现,临床治疗效果显著降低。课题组前期研究发现,作为肿瘤间质的重要组成部分,癌症相关成纤维细胞(cancer-associated fibroblasts, CAFs)在促进 HNC 进展中发挥重要的作用。研究报道,外泌体可以通过传递多种细胞活性物质参与细胞间通讯。同时,已有的研究表明 CAFs 来源的外泌体介导的 miRNA 递送在多种癌症的耐药中发挥重要的作用。然而,目前有关 CAFs 来源的外泌体 miRNA 在 HNC 细胞顺铂抗性产生过程中所发挥的功能及相应的机制尚不清楚。
研究内容
本文中作者首先确定了 CAFs 具有天然的顺铂耐受性,且这种顺铂耐受性可通过 CAFs分泌的外泌体传递到 HNC 细胞中,促进细胞增殖与存活。之后作者对其中的机制进行了研究,发现外泌体介导的 miR-196a 传送在其中发挥了重要的作用,而 CAFs 中的 hnRNPA1 蛋白介导了 miR-196a 包装进入外泌体。进一步研究发现,CDKN1B 和 ING5 是 miR-196a 潜在的下游靶基因,且外泌体 miR-196a 通过下调 CDKN1B 和 ING5 的表达促进头颈癌细胞对顺铂的耐药性。同时,体内实验也证明了外泌体 miR-196a 在头颈癌顺铂耐药中发挥着重要的促进作用。此外,结合临床数据分析发现,除了在肿瘤组织,miR-196a 在血浆中的表达水平也同患者的不良预后和化疗耐受密切相关。上述结果表明,miR-196a 可作为头颈癌顺铂耐药潜在的预测因子和治疗靶点。
研究思路
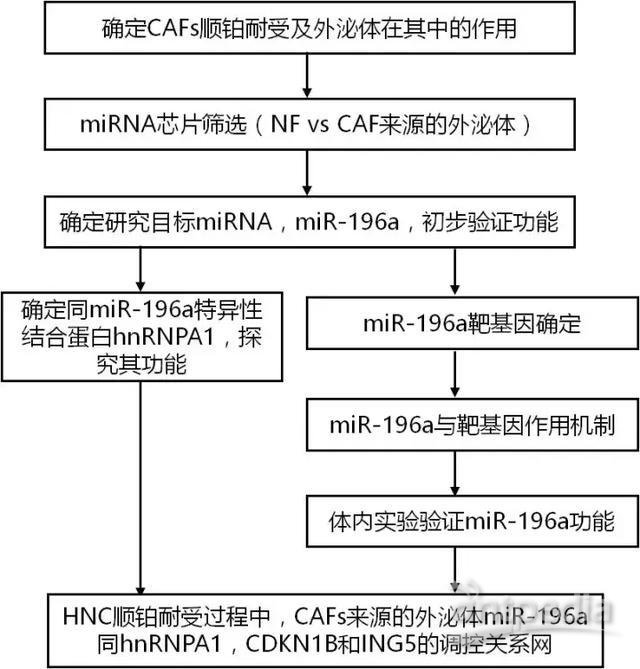
研究结果
1.CAFs 分泌的外泌体可以赋予 HNC 细胞顺铂抗性
作者首先检测了 CAFs、顺铂敏感的 HNC 细胞(CAL 27, SCC-25, HN4)以及有顺铂抗性的 HNC 细胞(HN4-res)的顺铂耐受性(图 1c),发现 CAFs 的存活率是最高的。其后,作者检测了顺铂对细胞增殖能力的影响以及与顺铂耐药相关蛋白的表达情况(图 1d, 1g)。上述结果共同表明 CAFs 天然具有顺铂耐药性。

图 1 | HNC 来源的 CAFs 本身即有顺铂抗性
此后作者分离了 CAFs 的培养基(CAF-CM)用以培养细胞,发现其可显著促进 CAL 27 和 HN4 的增殖(图 2a)和存活(图 2b)。当去除 CAF-CM 中的外泌体时,可检测到 CAF-CM 的作用明显被削弱(图 2c, 2d)。而分离自 CAFs 的外泌体作用于 HNC 细胞后则具有同 CAF-CM 相近的结果(图 2j, 2k)。

图 2 | CAFs 来源的外泌体可以增加 HNC 细胞增殖以及顺铂抗性
2.外泌体中的 miR-196a 可促进 HNC 细胞的增殖及对顺铂的耐受
用基因芯片技术检测 NF-CM 和 CAF-CM 来源的外泌体 miRNA,结合 qPCR 验证实验确定了一个在 CAF-CM 组中表达显著上调的 miR-196a 进行后续研究。去除外泌体后,可检测到 HNC 细胞中的 miR-196a 水平显著降低(图 3b, 3c)。随后又确认了 miR-196 的来源(图 3d)以及递送过程(图 3e),进一步证明 HNC 细胞中的 miR-196a 是通过 CAFs 分泌的外泌体递送的。在 CAFs 中过表达或敲低 miR-196a 则会影响与相应外泌体共培养的 HNC 细胞中 miR-196 的含量(图 3g)。

图 3 | 外泌体将 miR-196a 从 CAFs 转运至 HNC 细胞
随后作者在 CAL 27 中过表达了 miR-196a,发现其可促进细胞的增殖、细胞活力以及克隆的形成,而敲减 miR-196a 则有相反的效果(图 4b-4d)。流式细胞术的结果则表明 miR-196a 表达升高会促进 G1 期向 S 期的转换(图 4e)。除此之外,miR-196a 表达水平升高还会伴随着 HNC 细胞在顺铂作用下凋亡的减少(图 4f)。

图 4 | miR-196a 通过促进 G1/S 转换、抑制凋亡实现对 HNC 细胞的促进增殖和生存的作用
3.hnRNPA1 蛋白介导 miR-196a 选择性包装进入 CAFs 的外泌体中
用 RBPDB 预测并结合敲减实验确认了一个会引起外泌体中的 miR-196a 表达水平显著下降的蛋白 hnRNPA1(图 5c)。之后利用 miR-196a pull down 实验和 RIP 实验证明 hnRNPA1 和 miR-196a 可特异性的结合(图 5e)。当 CAFs 中的 hnRNPA1 被敲降后,miR-196a 的转运被削弱(图 5h)。体内实验证明也证明了 hnRNPA1 对肿瘤生长的促进作用(图 5i)。

图 5 | hnRNPA1 介导 miR-196a 进入 CAFs 来源的外泌体
4.miR-196a 通过下调靶基因 CDKN1B 和 ING5 发挥提升顺铂抗性的作用
利用数据库和 qPCR 实验,作者发现 CDKN1B 和 ING5 是 miR-196a 潜在的靶基因,且表达水平同 miR-196a 呈负相关 (图 6b, 6c)。Luciferase 实验和 IP 实验证明二者均为 miR-196a 的直接靶基因(图 6g, 6k)。蛋白层面也有相似的结果(图 6l)。

图 6 | 外泌体的 miR-196a 在 HNC 细胞中直接的靶基因是 CDKN1B 和 ING5
作者随后尝试证明了 miR-196a 是通过下调 CDKN1B 和 ING5 实现对 HNC 顺铂耐受的促进作用。共转 miR-196a 和 CMV-CDKN1B 或 CMV-ING5 会发现 miR-196a 提升顺铂耐受能力减弱(图 7d)。而在抑制 miR-196a 的前提下,将两个基因一同敲除可以消除 miRNA 的影响(图 7e)。当转染 miR-196a 时,共转染 CMV-CDKN1B 或 CMV-ING5 会抵消 miRNA 的作用,而转染的质粒中包含有相应的 3‘UTR 区域时,无法抵消(图 7f, 7g)。

图 7 | miR-196a 在 HNC 细胞中通过下调 CKDN1B 和 ING5 促进顺铂抗性
5. 体内实验证明 CAFs 来源的外泌体中的 miR-196a 促进 HNC 细胞顺铂抗性
在确定了 miR-196a 的作用机制后,作者进行了体外实验。在小鼠皮下异体移植瘤实验中,有外泌体呈递的小鼠肿瘤体积与质量都明显高于无外泌体作用小鼠(图 8a)。而注射 miR-196a 过表达 CAL 27 细胞的小鼠的顺铂耐受性强于对照组小鼠。而在头颈癌组织中,miR-196a 的高表达水平通常伴随着较重的病情以及较差的生存率(图 8c-8e)。此外,还可观察到 HNC 患者血浆中外泌体来源的 miR-196a 较健康人群更高,且进行手术切除后,miR-196a 水平明显下降(图 8f-8h)。以上种种暗示,miR-196a 可作为一个有价值的预后分子,也可以作为独立的化疗耐受预测因子,图 9 则显示了其可能的作用机制。

图 8 | 体内实验证明 CAFs 来源的外泌体 miR-196a 提升 HNC 细胞顺铂抗性

图 9 | CAFs 来源的外泌体 miR-196a 调节 HNC 细胞增殖和顺铂耐药的模型
总结
本研究发现了 HNC 细胞的顺铂抗性很大程度由 CAFs 分泌的外泌体赋予,并找到了其中一个重要的分子 miR-196a,并探索了这个 miRNA 发挥功能的上下游机制。体内、外实验共同证明了 miR-196a 可作为一个有价值的预后分子以及独立的化疗耐受预测因子。
参考文献
Qin X, Guo H, Wang X, et al. Exosomal miR-196a derived from cancer-associated fibroblasts confers cisplatin resistance in head and neck cancer through targeting CDKN1B and ING5. Genome Biol 2019; 20(1): 12.
文章通讯作者简介:张建军,副研究员,硕士生导师,国家口腔疾病临床医学研究中心PI,美国哈佛医学院(BIDMC)访问学者,上海市科技启明星,上海交通大学医学院双百人计划,SMC-晨星青年学者。主要从事口腔肿瘤表观遗传学方面的研究工作,近年来,作为负责人主持国家自然科学基金项目 3 项,主持上海市科学技术委员会基础重点项目 1 项。
近一年内发表文章如下:
[1]. Qin X, Guo H, Wang X, et al. Exosomal miR-196a derived from cancer-associated fibroblasts confers cisplatin resistance in head and neck cancer through targeting CDKN1B and ING5. Genome Biol 2019; 20(1): 12.
[2]. Yu B, Wu K, Wang X, et al. Periostin secreted by cancer-associated fibroblasts promotes cancer stemness in head and neck cancer by activating protein tyrosine kinase 7. Cell Death Dis 2018; 9(11): 1082.
[3]. Qin X, Yan M, Li R, et al. Identification and characterization of a highly metastatic epithelial cancer cell line from rat tongue cancer. Arch Oral Biol2018; 95: 58-67.
[4]. Xiao M, Zhang J, Chen W, et al. M1-like tumor-associated macrophages activated by exosome-transferred THBS1 promote malignant migration in oral squamous cell carcinoma. J Exp Clin Cancer Res 2018; 37(1): 143.
[5]. Zhang J, Guo J, Qin X, et al. The p85 isoform of the kinase S6K1 functions as a secreted oncoprotein to facilitate cell migration and tumor growth. Sci Signal 2018; 11(523): pii: eaao1052.
[6]. Qin X, Yan M, Wang X et al. Cancer-associated Fibroblast-derived IL-6 Promotes Head and Neck Cancer Progression via the Osteopontin-NF-kappa B Signaling Pathway. Theranostics 2018; 8(4): 921-940.
[7]. Liu J, Ben Q, Lu E, et al. Long noncoding RNA PANDAR blocks CDKN1A gene transcription by competitive interaction with p53 protein in gastric cancer. Cell Death Dis 2018; 9(2): 168.
[8]. Wang Y, Qin X, Zhu X, et al. Oral cancer-derived exosomal NAP1 enhances cytotoxicity of natural killer cells via the IRF-3 pathway. Oral Oncol 2018; 76: 34-41.
- END -


