
分析测试百科网 认证会员,请放心拨打!
蓄能2020药典:生物制品标准接轨国际
蓄能2020药典:生物制品标准接轨国际,5分钟了解世界生物药前沿
关注我们,更多干货和惊喜好礼

导读:
“2020年版《中国药典》草案审议通过,三部生物制品收载153种,其中新增20种、修订126种;新增生物制品通则2个、总论4个。”——第十一届药典委员会执行委员会会议审议通过2020年版《中国药典》草案。
随着草案审议的通过,标志着2020版药典正式进入收官。着眼药典三部生物制品篇,从编制之初,就强调要进一步完善生物制品全过程质量控制的要求,进一步补充完善生物检测技术、方法以及相关技术指南,并与国际接轨。新版药典的出台,必将引导整个行业向更严格、更国际化的方向发展,也让中国生物药产业迎来新的变革与机遇。

从两大板块到三驾马车
中国生物制药创新格局初现
在一系列创新政策的驱动下,我国生物医药格局发生了重大变化,逐步出现第三个新型板块,即国产创新药,由此打破了近几十年来国产仿制和进口创新长期主导的两大板块的格局,组成三大板块:国产仿制药、进口创新药和国产创新药[1]。
生物制药由两大板块向三驾马车的格局变化,标志着全新的中国生物制药创新格局初现。同时,如百济神州等中国生物药企业获批FDA,越来越多中国制药企业加速扩展海外版图,也标着接轨国际标准的中国式创新,越来越被世界所认可。
无疑,中国生物制药正在驶向前所未有的黄金快车道,但其中也蕴含着诸多挑战:例如,如何在创新同时讲求效率,切实帮助企业的药物开发更快获批上市?从早期研发、表征分析、工艺优化到 CMC、QC 分析,生物制品在每一个环节均存在着极其复杂的不确定性,如何正面树立中国生物制药企业的整体“质量”形象?如何创新和质量并重,同时接轨世界标准?这些都成为值得讨论的课题。
拥有中国“灵魂”,世界“眼光”
开启中国生物药企业新范式
不论是立足国内市场,满足2020版《中国药典》三部,多项指导原则(如人用重组DNA产品质量控制技术指导原则等)及药品注册管理办法等;还是扩展世界市场,满足繁多的国际标准:如WHO、FDA、EMA技术指南和相关指导原则、以及ICH 指导原则等标准,都要求中国生物药企业,越来越拥有中国“灵魂”-创新,和世界“眼光”-满足接轨国际标准。
那么如何对标国际领先的生物药企业,满足严格的国际生物制药标准?正所谓知己知彼,百战不殆,赛默飞拥有完善的生物药表征和质量控制方案,我们携手世界知名生物企业首席科学家们,开启了名为: Leaders in BioPharmaceutical Characterization and Control的系列微课堂,为您带来最前沿的生物药表征与质控的最佳实践,一探生物药“创新”与“质量”的世界前沿:
微课堂系列开启,了解生物药表征和质量控制中的全球前沿应用
第一期:
Alternative strategies for peptide mapping of challenging monoclonal antibodies in clinical development

Dan Bach Kristensen
Symphogen首席科学家
Dan Bach Kristensen拥有生物学博士学位和化学学士学位。Dan专门从事蛋白质化学和质谱分析,最初活跃于日本的蛋白质组学研究领域,后来又拓展至丹麦的蛋白质组研究领域。在过去的15年中,Dan一直在生物制药行业中从事分析与开发工作,涉及从早期发现到注册的各个环节。临床适应症包括出血性疾病,中性粒细胞减少,自身免疫性疾病和肿瘤等。Dan目前是Symphogen的首席科学家,该公司专门研究用于癌症治疗抗体的开发。

Tom Buchanan
赛默飞高级应用科学家
Tom Buchanan于2018年加入赛默飞,担任Allergan Biologics欧洲生物制药应用开发科学家,他是分析方法开发领域的生物药物表征科学家。在Allergan,他负责开发用于生物制剂的LC-UV / LC-MS肽图分析方法,特别是单克隆抗体。Tom在cGMP下游生物生产和质量控制以及过程中的批次测试,稳定性研究和分析方法验证方面拥有专业知识。
在生物制药领域,生物技术药物的表征和质量控制这两词及所涉及的检测方法早已植根于每个研发和分析者的内心,然而由于生物药物极其复杂的结构,仍需要不断的研发新技术、开发新方法以解决生物药物表征及质量控制中不断出现的新问题,确保药物的安全性和有效性。
5min速览版
为了方便您快速掌握微课堂咨询与要点信息,我们特地总结了5min速览版。当然,如果您想深入了解课程精髓,不错过原汁原味的国际专家分享,推荐您一定要观看完整版微课堂。
本期微课堂为您带来:
具有挑战性单克隆抗体肽图分析的难点及解决方案
要点1
蛋白类药物在肽图分析过程中监测翻译后修饰的种类和含量对生产和工艺的优化至关重要,最终影响着药物的安全性和有效性,然而也存在诸多挑战,如酶解时间长,且在酶解过程中会引入新的翻译后修饰或提高翻译后修饰含量,这将导致无从判断翻译后修饰的具体来源:是否来源于工艺参数或来自于酶解,不断优化实验条件进而影响药物的研发周期。此次报告中使用了SMART Digest Low pH Trypsin and Pepsin创新的自动化样品酶解方法,将酶解过程中对修饰的影响降低至最少甚至消除,有助于解决绝大多数生物制药企业对于翻译后修饰研究的困扰,从而根本上提升蛋白类药物研发的效率和质量控制的准确度。
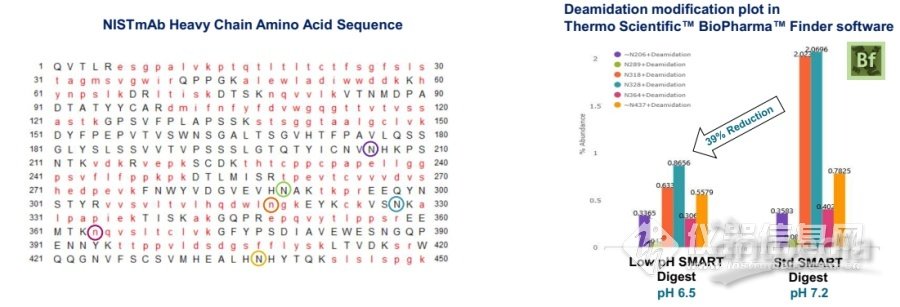
低pH Trypsin酶解条件显著降低翻译后修饰的含量,且能够实现自动化快速样品处理
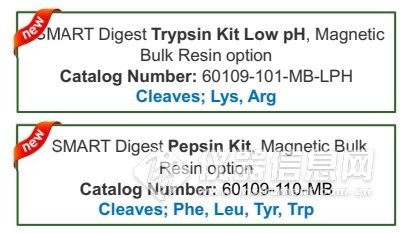
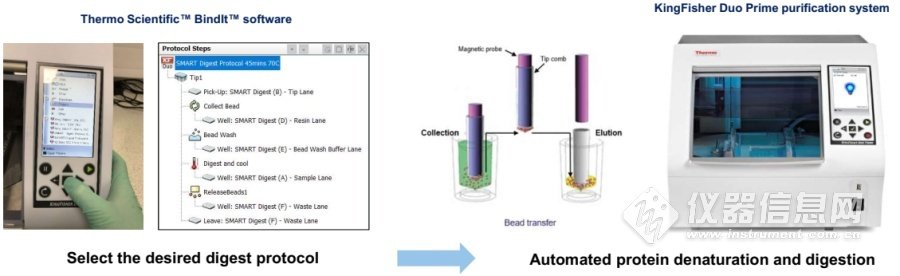
赛默飞SMART Digest自动化快速酶解创新性解决方案

赛默飞肽图分析完整解决方案
要点2
胰蛋白酶(trypsin)一直是蛋白酶解的常用酶,但其活性受限于高且窄的pH值范围,及蛋白序列中多种疏水性氨基酸,这导致酶解过程中某些翻译后修饰含量增加,对含有疏水性氨基酸较多的蛋白类药物序列覆盖不到,此次报告中将会介绍使用胃蛋白酶(SMART Digest Pepsin Kit)解决胰蛋白酶无法覆盖某一抗体CDR区的问题,从而充分验证蛋白序列中每一氨基酸正确与否。
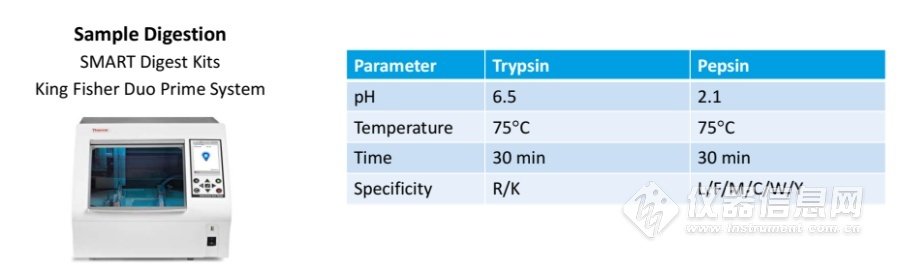
SMART Digest Pepsin Kit的实验条件
要点3
LC-MS分析方法中如何选择添加剂,既能提高液相的分离度,质谱又能兼容?酶解后疏水性多肽放置过夜后,被非特异性吸附后,怎么办?如何利用自动化技术提高酶解过程中的重复性,以确保方法的可移植性?这些问题都会在此次报告中给出答案~
扫码了解完整讲座

文末福利
赛默飞完整解决方案及讲座
生物药肽图分析相关解决方案
▇ 点击阅读原文查看
• 蓄能|2020药典系列 对标国际标准,最严中药农残有毒有害物质控制标准
• 蓄能|2020版药典系列-当新版药典遇上基因毒性杂质
• 【预告】|2020药典系列线上讲座:快来pick 5月的精彩
• 蓄能,迎接史上“最严”药典
参考文献:
1.刘昌孝院士《中国科学报》 (2019-12-30 第5版)
如需合作转载本文,请文末留言。

![]() 猛戳这里,查看福利
猛戳这里,查看福利
扫描下方二维码即可获取赛默飞全行业解决方案,或关注“赛默飞色谱与质谱中国”公众号,了解更多资讯+ 了解更多的产品及应用资讯,可至赛默飞色谱与质谱展台。https://ibook.antpedia.com/562/
了解更多的产品及应用资讯,可至赛默飞色谱与质谱展台。https://ibook.antpedia.com/562/
| 标签: | LC LCMS 蛋白类药物 |








