
诚信认证:
工商注册信息已核实! 扫一扫即可访问手机版展台
扫一扫即可访问手机版展台

动物毒腺体分泌蛋白的快速高分辨成像

了解动物组织的剧毒液的产生和储存,为其分泌组织的生态学和生物进化提供了新的视角,并让我们开发这些毒素用于疾病治疗和农用化学的目的。
很多种动物可以产生剧毒液, 其成分可以有不同的分子类型、药学作用和生物功能。近年的研究突出了剧毒液的储存和产生与其原有的生物功能存在某种关系。因此,剧毒液在其分泌组织中的空间分布,为毒液成分的生物学作用、功能和潜在靶点研究提供了重要的信息,让我们更深入的了解其生物进化过程。MALDI质谱成像是研究动物毒液成分空间分布的理想方法,timsTOF fleX质谱仪具有独特的灵敏度、质量准确度、质量分辨率和成像速度等高性能组合,可以高效的分析这些化合物。
作者:Brett R.Hamilton 1,2,Vanessa Schende1,2,Eivind A.B.Undheim 2,3,4,Janina Oetjen5,Alice Ly 5,Roger A.Wepf 1;
1澳大利亚昆士兰大学显微镜和微分析中心;2澳大利亚昆士兰大学高级成像中心;3挪威科学技术大学生物系生物多样性动态中心;4奥斯陆大学生物科学系生态和进化综合中心;5布鲁克·道尔顿
应用简介
MALDI质谱成像[1]的出现极大地改变了各种生物毒液的研究方法。MALDI质谱成像能够直接分析毒腺组织中的毒液成分和空间分布。迄今研究的大多数毒液由大量的肽和蛋白质组成,它们的分子量从1000到12000Da不等,具有代表性的分子大部分在2000-8000Da[2, 3]。这个质量范围一般使用MALDI-TOF线性质谱进行分析。
本研究显示了新型的timsTOF fleX组合质谱仪具有的高质量分辨率和质量精度,同时保持20μm的高空间分辨率和快速数据采集。从毒腺体成像得到的数据反映了高质量分辨率、空间分辨率和速度的结合在多肽和小蛋白MALDI质谱成像分析的巨大进步,特别是能够鉴定更多的毒腺体分子。在保证质量分辨率和采集速度时,timsTOF fleX能很好的分析质量范围2000-8000Da的多肽和蛋白分子。
实验方法
蜈蚣样本取自于澳大利亚昆士兰。取其腹下颚肢部位作为样本,蜈蚣特有的分泌毒液的腿部[4],用50%的RCL2/乙醇固定,再用70%、90%和100%的乙醇脱水和二甲苯清洗,并用石蜡浸渍包埋[3]。石蜡块用组织切片机切成7μm厚度的切片,放置在ITO载玻片上加热30分钟,然后用二甲苯洗涤脱蜡,干燥后对切片用扫描仪拍照。基质使用2,5-二羟基苯甲酸(DHB),采用升华法施加基质到载玻片上的组织样本上。为了更好的得到肽和蛋白质的信号,增加了分子再结晶,使用布鲁克ImagePrep基质喷雾仪和50%甲醇溶液(含0.2%三氟乙酸)完成这一步骤。
timsTOF fleX质谱成像仪器参数: QTOF正模式; 外标校准; 质量范围:m/z 800-10000; 空间分辨率: 20μm; 激光频率: 10KHz; 激光次数: 2000;激光经线束调制。图像可视化和数据分析使用SCiLS Lab MVS软件,均方根归一化和pLSA统计分析。质谱成像后再对组织标本进行H&E染色分析
结果与讨论
图1显示了在timsTOF fleX上测量的蜈蚣毒腺组织切片的平均质谱图,其中放大区域显示了不同丰度分子的空间分布。谱图中约有4643个潜在特征峰,具有很好的信噪比,其中1000个峰用于产生分子图像。
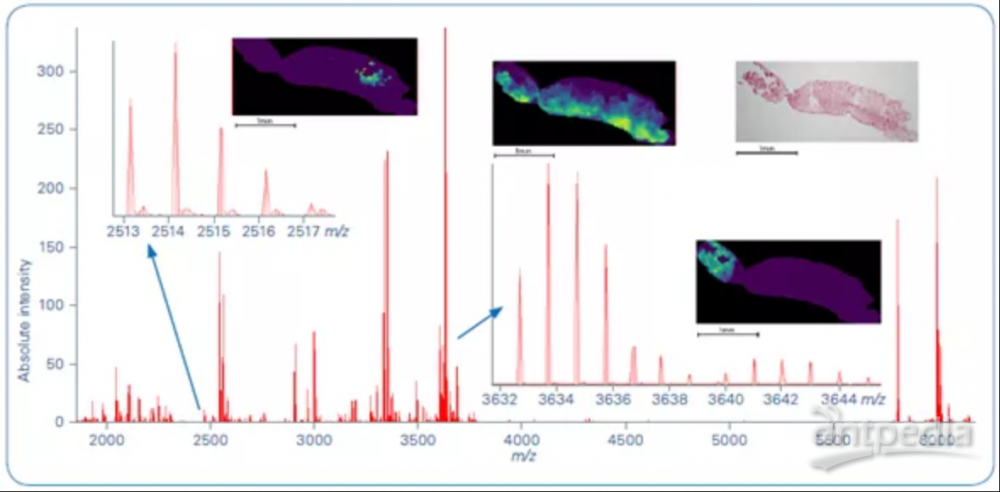
图1:timsTOF fleX采集的蜈蚣毒腺组织的平均质谱图,放大图显示了高丰度和低丰度肽的谱峰和质谱成像分析后的H&E染色图
谱图中有一些基质峰,通过高质量分辨率可以使这些信号在数据处理中被识别和剔除。大量特征分子在不同的信噪比被鉴定,作为组织分子成像数据。数据显示timsTOF fleX为质谱成像实验提供了宽动态范围。数据采集以20μm像素点为间隔;采集速度为每秒5像素(10000Hz, 2000次激光),共4657个像素。
图2显示了单同位素质量 6000.99Da的目标肽中性分子的空间分布和质量分辨率。在m/z 6000,单同位素的丰度相对较低,且A+1、A+2、A+3峰的离子比单同位素的测量结果更精确。在该质量范围内同位素簇中的其它峰都有非常好的质量精度。
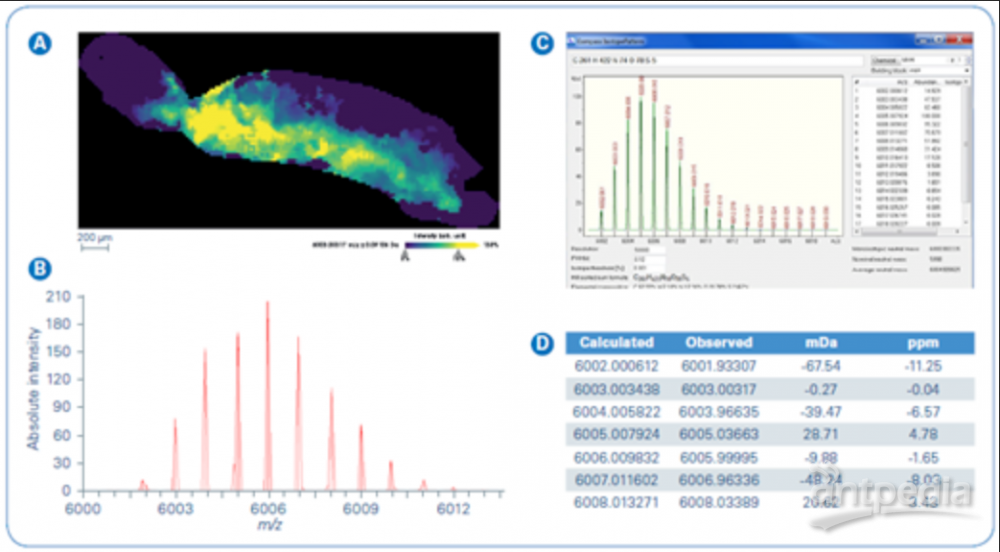
图2:A. timsTOF fleX上观察到的蛇毒肽U-SLPTX15-Sm1a的空间分布和质量分辨率;B. 平均质谱区域放大图;C. U-SLPTX15-Sm1a的模拟质谱;D. U-SLPTX15-Sm1a的质量精度。
timsTOF fleX使用正交TOF而不是同轴TOF,把分子的电离和离子传输飞行分开,使肽和蛋白离子的能量色散对时间聚焦的影响降至最低,有效提高了质量分辨率。图2所示的已知肽U-SLPTX15-Sm1a,其单同位素中性质量为6000.99 Da。图2B是4657个像素的平均质谱的区域放大图,显示了timsTOF fleX的质量稳定性。timsTOF fleX的正交TOF帮助了高质量精度和稳定性的实现。
在计算同位素簇中各个峰的质量精度时,实际偏差在0-11ppm之间(图2),这对直接从组织中测量6000Da的小蛋白是一个令人满意的结果。在质量范围 1000–6500内观察到类似的其它高质量分辨率和高质量精度数据。timsTOF fleX具有良好的动态范围,同时获得高丰度和低丰度肽的空间分布。而且仪器的分辨率可以容易地将较低的信号从基线噪声中提取出来。
使用SCiLS Lab MVS 中的pLSA算法进行成像后的主成分分析(图3),揭示了蜈蚣毒腺体中观察到的各种肽和蛋白质的区域化,这与先前发表的该物种的分析结果一致[2,3]。尽管这种毒液成分空间异质性的生物学意义尚不清楚,但有人假设它反映了较少数量的分泌细胞对毒素大量产生的生理限制[2]。这种分布不均匀性也表现在其他有毒动物谱系中,毒素的空间异质性被认为能够对分泌的毒液进行生化调节[5]。研究毒液分布和腺体区域化的实验表明,MALDI质谱成像比其他蛋白质检测方法,如缺少空间信息的Western Blot更具优势。同样,在一个组织切片中同时检测众多不同分子比基于探针技术的免疫组化或原位杂交具有更多优势。

图3: timsTOF-fleX的宽动态范围,六种具有代表性的毒液成分在组织切片中的分布和丰度
结论
1. timsTOF fleX为多肽和小蛋白的质谱成像分析提供了独特的灵敏度、质量精度、质量分辨率和速度的组合;
2. 通过这个实验,timsTOF fleX为毒液生物学研究提供了引人入胜的新方法;
3. timsTOF fleX为成像实验中观察到的肽和蛋白质提供分子注释,并建立蛋白组学与基因组学间的更密切联系。
参考文献
[1] Caprioli RM, Farmer TB, Gile J (1997). Molecular imaging of biological samples: Localization of peptides and proteins using MALDI-TOF MS. Analytical Chemistry, 69, 4751–4760.
[2] Undheim EAB, Hamilton BR, Kurniawan ND, Bowlay G, et al. (2015). Production and packaging of a biological arsenal: Evolution of centipede venoms under morphological constraint. Proceedings of the National Academy of Sciences of the United States of America, 112, 4026–4031.
[3] Undheim EAB, Sunagar K, Hamilton BR, Jones A, Venter DJ, Fry BG, King GF (2014). Multifunctional warheads: Diversification of the toxin arsenal of centipedes via novel multidomain transcripts. Journal of proteomics, 102C, 1-10.
[4] Lewis J (1981). The Biology of Centipedes, Cambridge University Press.
[5] Hamilton BR, Marshall DL, Casewell NR, Harrison RA, et al. (2019). Mapping Enzyme Activity on Tissue by Functional Mass Spectrometry Imaging. Angew Chem Int Ed Engl, 59, 1-5.
[6] Madio B, Peigneur S, Chin YKY, Hamilton BR, et al. (2018). PHAB toxins: a unique family of predatory sea anemone toxins evolving via intra-gene concerted evolution defines a new peptide fold. Cellular and Molecular Life Sciences, 75, 4511-4524.
[7] Walker AA, Mayhew ML, Jin J, Herzig V, et al. (2018). The assassin bug Pristhesancus plagipennis produces two distinct venoms in separate gland lumens. Nat Commun, 9, 755.
[8] Dutertre S, Jin AH, Vetter I, Hamilton B, et al. (2014). Evolution of separate predation -and defence-evoked venoms in carnivorous cone snails. Nat Commun, 5, 3521
| 标签: | 布鲁克,质谱,动物,毒腺体,分泌,蛋白,高分辨成像 |






