
腺病毒载体疫苗的制备与分离
通常来说,开发一种新型疫苗需要经过数年的艰苦过程,包括完整的生产工艺确定。这样的模式没办法对一些爆发性的传染疾病做出快速响应,而且面对一些商业潜力比较小的区域性疾病或者是某些定制化疫苗也是力有不逮。
在病毒载体家族里面,腺病毒的应用非常广泛,它具有诱导抗体和 T 细胞组合反应的潜能。虽然人群中广泛存在的先天免疫可能会使人源腺病毒疫苗载体的效果大打折扣,但是如果采用灵长类动物来源的腺病毒或者人源稀有型腺病毒就可以克服这一障碍,保证安全的同时免疫原性也大大提升,采用腺病毒平台的埃博拉疫苗已经在中国上市,而且很多项目处于临床阶段和临床前,针对的疾病包括疟疾、中东呼吸综合症 (MERS)、呼吸道合胞病毒和多种癌症。
图片来源:https://www.innovationtoronto.com
腺病毒 (Adenovirus) 是一种没有包膜的直径为 70~90nm 的颗粒,由 252 个壳粒呈廿面体排列构成。
虽然非复制性腺病毒载体 (Ad) 的 GMP 级别生产方法并不少见,但是依然存在很多挑战。面临突发疫情,如何快速为临床前实验生产匹配 GMP 要求的腺病毒疫苗变的尤为重要,该工艺需要具有可放大性、简洁性,尽可能采用一次性技术,能够很快的进行生产场地转移与调整。
最近,默克技术团队联合牛津大学 Jenner 研究所对基于灵长类来源的三种腺病毒载体疫苗 (ChAdOx2,针对狂犬病;ChAd63,针对疟疾;ChAdOx1,针对裂谷热) 的工艺开发进行了系统研究,结果表明:该方案具有非常好的平台性,少许改动便可以在不同的腺病毒血清型疫苗中进行切换,面对突发疫情可以在短时间内完成临床前样品工艺开发工作 1。
特地摘录,以飨读者
一、上游技术
1、细胞株与发酵罐
悬浮培养 HEK293 T-rex 细胞,并逐渐降低 FBS 浓度至 0.5%,接种于 Mobius®发酵罐中,接种密度为 1.5-2.0*106 cells/mL,DO 设定为 50% 空气饱和度,pH 设置为 7.2-7.3 (CO2 或 7.5% 碳酸氢钠),采用 MOI (感染复数) 为 3 进行病毒接种,3 小时后,加入 1.5 倍体积新鲜培养基。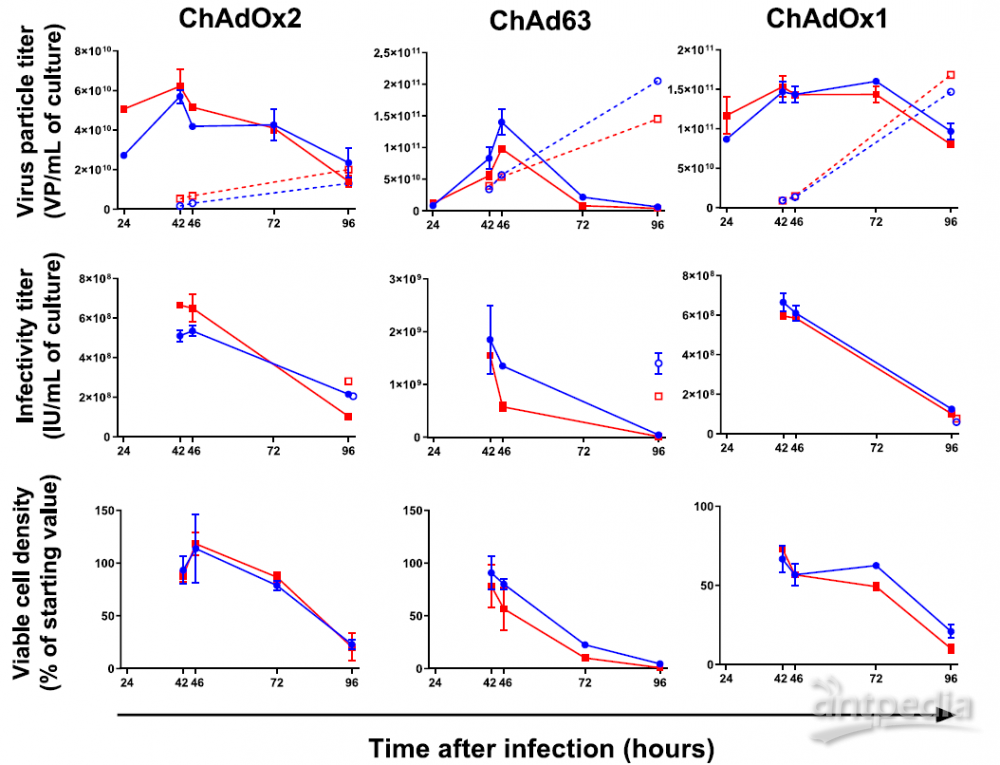
2、细胞裂解、核酸酶消化以及澄清
病毒感染 42 h 后,加入 1/9 发酵液体积的裂解缓冲液 (10% v/v 聚山梨醇酯 20,50%w/v 蔗糖,20 mM MgCl2,500 mM Tris pH8.0,Benzonase® 60 units/mL),关闭 DO 与 pH 控制,保持搅拌,37℃。2 h 后,采用 Millistak+® HC Pro C0SP 深层滤器进行澄清处理,通量为 6.6 L/min/m2。使用之前采用 1% v/v 聚山梨醇酯 20,5%w/v 蔗糖,2 mM MgCl2,50 mM Tris pH8.0 缓冲液进行滤器润洗及排气。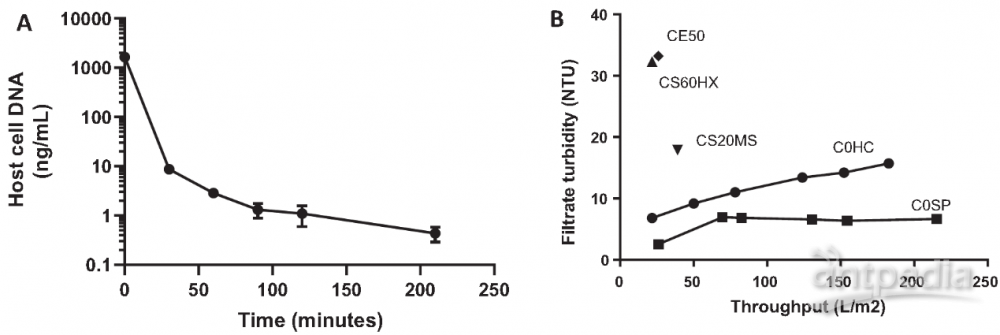
二、下游技术
1、浓缩与透析
澄清完成后采用 Pellicon® 2 BioMax 300KD (C 筛网)TFF 进行切向流浓缩换液,为下游纯化做准备,通量为 6 L/min/m2。完成 6-10 浓缩后换到层析平衡液: 100 mM NaCl、1 mM MgCl2、0.1% v/v 聚山梨醇酯 20、5% w/v 蔗糖、50 mM bis-tris、pH6.5。
2、层析
筛选了三种膜层析介质,包括 Natrix® Q 膜层析,采用过量上样纯化后的腺病毒载体的方式测定动态结合载量,用 A280 进行判定。步骤为:上样后清洗 10 个膜体积,然后 1M NaCl、1 mM MgCl2、 0.1% v/v 聚山梨醇酯 20、 5% w/v 蔗糖、 50 mM Tris-HCl、 pH 8.0。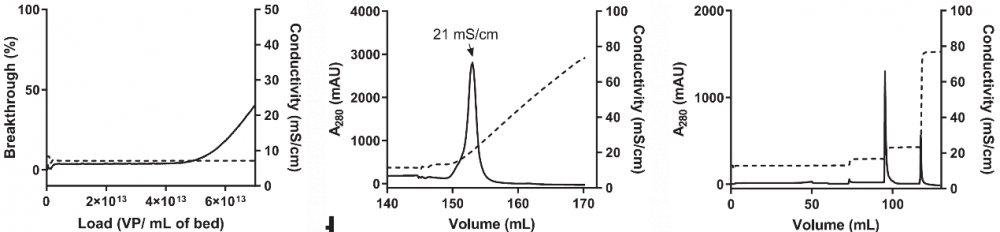

3、浓缩换液与除菌过滤
层析结束后,采用和 3 一样的 TFF 滤器进行第二次浓缩换液,通量为 0.83 L/min/m2,交换至 A438 缓冲液中 (10 mM 组氨酸、7.5% 蔗糖、35 mM NaCl、1 mM MgCl2、0.1% PS-80、0.1 mM EDTA、0.5%v/v 乙醇 pH6.6、跨膜压为 0.5bar)。最后采用 0.2um 滤器 Millipak®-20 进行除菌过滤。
4、下游收率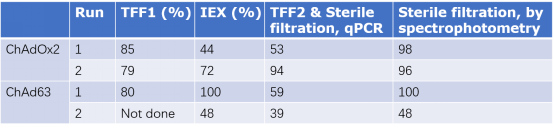
小 结
简而言之,该方案上游采用了 Mobius®一次性生物反应器技术,具有放大性好,无需验证的特点。下游采用默克全新的 Millistak® C0SP 深层过滤膜包进行料液澄清,Pellicon® 2 BioMax 300 KD TFF (C 筛网) 膜包进行浓缩换液。下游层析步骤筛选了 Natrix® Q 膜层析介质,具有高流速,高载量的特点,尤其是 um 级的开孔,比传统柱层析更有利用病毒类颗粒的结合,同时也无需验证,既用既抛。最后同样采用 Pellicon® 2 BioMax 300 KD TFF (C 筛网) 进行浓缩以及制剂缓冲液置换,最后采用 0.2um 滤器 Millipak®-20 进行除菌过滤。
整套方案流程简洁、可操作性强、平台性好,可以借鉴在多种腺病毒载体疫苗或腺病毒转基因载体工艺开发,快速应对突发疫情。
如您需要了解默克纯化产品,请点击此处。
注释及参考文献:
1.Sofiya Fedosyuk , Thomas Merritt, et, Vaccine, 2019 Nov 8;37(47):6951-6961
相关阅读:
除病毒滤器 Viresolve® NFR 在 AAV 生产中的优化,验证及应用
慢病毒收获澄清工艺开发中的考量点及滤器选择
关于细胞基因治疗加速行动
细胞基因治疗加速行动(Cell and Gene Therapy Boost,简称 CGTBoost)是默克工艺解决方案部门为了助力中国细胞基因治疗产业发展而发起的特别行动。整合默克近 30 年生产经验,集合全球细胞基因治疗专家,为您提供上游培养、下游分离、生物及病毒安全、产品检测及法规咨询等一站式解决方案,加速推动中国细胞基因治疗行业成长。



